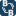Θα μπορούσατε να εξηγήσετε σε μεγαλύτερο βάθος την πλήρη διαδικασία και τα πράγματα να είναι πιο εύκολα κατανοητά για ηλίθιους όπως εγώ
Μέσο Α τι είναι. Αποτελείται από
Αν ΔΕΝ ΚΑΤΑΛΑΒΑΙΝΕΙΣ ΜΗΝ το κάνεις. ενώ η παρασκευή LPAC είναι σαν την παρασκευή μπύρας το ΕΠΟΜΕΝΟ ΒΗΜΑ
αυτή η μαλακία περιλαμβάνει ΚΥΑΝΙΔΙΟ και ΒΡΩΜΙΝΗ ΜΑΖΙ για να ΚΑΤΑΣΚΕΥΑΣΤΕΙ το βρωμίδιο του κυανογόνου είναι ΤΟΞΙΚΟ σκατό.
Το βρωμιούχο κυάνιο μπορεί να σας επηρεάσει όταν αναπνέετε και
περνώντας μέσα από το δέρμα σας.
* Η επαφή μπορεί να ερεθίσει το δέρμα και τα μάτια.
* Η αναπνοή του βρωμιούχου κυανογόνου μπορεί να ερεθίσει τη μύτη και το στόμα.
λαιμό.
* Η αναπνοή του βρωμιούχου κυανογόνου μπορεί να ερεθίσει τους πνεύμονες.
προκαλώντας βήχα ή/και δύσπνοια. Υψηλότερη
εκθέσεις μπορεί να προκαλέσουν συσσώρευση υγρού στους πνεύμονες.
(πνευμονικό οίδημα), ένα επείγον ιατρικό περιστατικό, με σοβαρή
δύσπνοια.
* Υψηλή έκθεση στο βρωμιούχο κυανούν μπορεί να προκαλέσει θανατηφόρο
Δηλητηρίαση από κυάνιο με έξαψη του προσώπου, του θώρακα
σφίξιμο στο στήθος, πονοκέφαλο, ναυτία, έμετο, αδυναμία,
σύγχυση, ζάλη και δυσκολία στον ύπνο. Υψηλά επίπεδα
μπορεί να προκαλέσουν σπασμούς και θάνατο.
Η γνωστή αντίδραση των υδραζιδίων με βρωμιούχο κυάνιο, που συνήθως πραγματοποιείται παρουσία διττανθρακικού καλίου ή νατρίου,
δίνει 2-αμινο-5-υποκατεστημένα-1,3,4-οξαδιαζόλια. Τα τελευταία 10 χρόνια, η αντίδραση αυτή έχει εφαρμοστεί αρκετές φορές, κυρίως με σκοπό τη λήψη βιολογικά δραστικών παραγώγων.....
Το παρατσούκλι μου είναι ΑΖΙΔΕΣ... AZIDES go BOOM ... Ένα
υδραζίδιο μετατρέπεται στο αντίστοιχο
αζίδιο παρουσία ενός οξέος και ενός νιτρώδους άλατος. Το υδραζικό οξύ μπορεί να παραχθεί μόνο από αζίδια και ένα οξύ (νερό).
Βλέπε
Πόσο επικίνδυνο είναι το πολύ επικίνδυνο; Μια προοπτική της χημείας των αζιδίων
Πόσο επικίνδυνο είναι το πάρα πολύ επικίνδυνο; Μια προοπτική για τα αζίδια
Χημεία
Αναφέρετε αυτό: Org. Chem. 2022, 87, 11293-11295 Read Online
ACCESS Metrics & περισσότερες συστάσεις άρθρων
Όλοι οι χημικοί θα πρέπει να γνωρίζουν τους κινδύνους που ενέχουν οι
εργασία τους και θα πρέπει να εξετάζουν πώς να προστατεύουν επαρκώς τους
τους εαυτούς τους και τους συναδέλφους τους από τους εν λόγω κινδύνους. Αυτό εγείρει
το ερώτημα: Μπορεί μια αντίδραση να είναι τόσο επικίνδυνη ώστε, σε μια γενική
εργαστήριο γενικής χρήσης, ακόμη και με την παρουσία τέτοιων προφυλάξεων,
ο υπολειπόμενος κίνδυνος εξακολουθεί να είναι πολύ υψηλός; Υποστηρίζουμε ότι ναι, ορισμένες
αντιδράσεις εμπίπτουν σε αυτή την κατηγορία: εκείνες που χρησιμοποιούν στοιχειομετρία
μετρικές ποσότητες υδραζοϊκού οξέος, εκείνες που σχηματίζουν μεταβατικές
αζίδια μετάλλων, και εκείνες που συνδυάζουν ανόργανο αζίδιο με
διχλωρομεθάνιο.
Ένα πρόσφατο άρθρο σε αυτό το περιοδικό με συγγραφείς τους Gazvoda et al.
περιγράφει μια διαδικασία για την παρασκευή τριαζολών από αλκίνια
χρησιμοποιώντας στοιχειομετρικό αζίδιο νατρίου, στοιχειομετρικό οξύ και
καταλυτικό χαλκό, ακολουθούμενη από μια επεξεργασία που μπορεί να περιλαμβάνει
διχλωρομεθάνιο.1,2 Ως βιομηχανικοί χημικοί με δεκαετίες
εμπειρία στην ασφαλή κλιμάκωση της χημείας των αζιδίων, αισθανόμαστε υποχρεωμένοι
να μοιραστούμε με την ερευνητική κοινότητα τις τρεις κύριες δικλείδες ασφαλείας μας
ανησυχίες με αυτή τη διαδικασία.
Στην πρώτη περίπτωση, ο συνδυασμός αζιδίου νατρίου και οξέος
δίνει υδραζοϊκό οξύ. Το υδραζοϊκό οξύ είναι τόσο οξεία τοξικό
(LD50 σε ποντίκια = 22 mg/kg)3 και ισχυρό εκρηκτικό.
καθαρή μορφή του, το υδραζοϊκό οξύ είναι πιο εκρηκτικό από το TNT και το
τάξεις μεγέθους λιγότερο σταθερό.4 Οι πρώτοι επιστήμονες που απομόνωσαν
υδραζοϊκό οξύ (Curtius και Radenhausen, το 1891)5 διαπίστωσαν ότι
ότι "η έκρηξη 50 mg ήταν αρκετή για να διαλύσει το
συσκευή σε σκόνη" και όταν μια επόμενη παρτίδα 700 mg
"εξερράγη αυθόρμητα", τραυμάτισε σοβαρά τον συν-συγγραφέα
(Radenhausen) και το ωστικό κύμα από την έκρηξη
έσπασε κάθε γυάλινο δοχείο που βρισκόταν κοντά. Δεν υπάρχει ασφαλής ποσότητα
όταν πρόκειται για καθαρό υδραζοϊκό οξύ.
Ενώ το αραιωμένο υδραζοϊκό οξύ είναι ασφαλέστερο από την καθαρή ένωση,
παραμένει εξαιρετικά επικίνδυνο. Στην αέρια φάση, τα μίγματα με
αζώτου που περιέχουν περισσότερο από 10% HN3 είναι εκρηκτικά.4g Σε
νερό, δεν έχει προσδιοριστεί ακριβής τιμή, αλλά είναι
γενικά αποδεκτό ότι διαλύματα με >20 κ.β. HN3 είναι
εκρηκτικά.6 Ο μοναδικός κίνδυνος που ενέχει το υδραζικό οξύ σε διάλυμα
είναι ότι λόγω του χαμηλού σημείου βρασμού του (∼36 °C), η ακούσια
εξάτμιση και επανασυμπύκνωση ενός αραιού, μη εκρηκτικού
διάλυμα μπορεί να οδηγήσει σε ένα πυκνό, εκρηκτικό διάλυμα (βλ.
Σχήμα 1).7 Είναι κρίσιμο να γίνει κατανοητό ότι τα συμπυκνωμένα σταγονίδια
του πυκνού υδραζοϊκού οξέος δεν απαιτούν ούτε οξυγόνο ούτε
σπινθήρα προκειμένου να εκραγούν (δηλαδή, το λεγόμενο "τρίγωνο της φωτιάς" δεν
δεν ισχύει).4β Η παραμικρή τριβή ή κρούση μπορεί να
να οδηγήσει σε έκρηξη. Έχουν αναφερθεί πολυάριθμες εκρήξεις
κατά την ενασχόληση με το υδραζοϊκό οξύ σε διάλυμα, πολλές από τις οποίες
έχουν δυστυχώς οδηγήσει σε τραυματισμούς και θανάτους.8
Γενικά, όταν πρόκειται να χρησιμοποιηθούν αραιά διαλύματα υδραζοϊκού οξέος
παράγονται ή αποθηκεύονται, οι βέλτιστες πρακτικές είναι η προσθήκη ενός χαμηλού βρασμού
διαλύτη (όπως ο αιθέρας ή το πεντάνιο) για την αραίωση τυχόν ατμών ή/και
συμπυκνώματος.4f Υπολογισμοί με βάση τη θερμοκρασία και το pH
μπορεί να είναι απαραίτητοι για την κατανόηση της κατάλληλης ασφαλούς συγκέντρωσης
6b,7b Επιπλέον, εάν ένα σύστημα αντίδρασης περιέχει υδραζοϊκό
οξύ ή μπορεί να παράγει υδραζοϊκό οξύ, ένα συνεχές αζωτούχο
καθαρισμού του κεφαλοχώρου μπορεί να χρησιμοποιηθεί για την αποφυγή
συμπύκνωση, και ολόκληρη η συσκευή μπορεί να διατηρείται
πάνω από τους 37 °C για να εξασφαλιστεί ότι δεν μπορεί να συμπυκνωθεί υδραζοϊκό οξύ.
Επιστρέφοντας στη διαδικασία σύνθεσης τριαζολίου που αποκαλύπτεται
από τους Gazvoda κ.ά., η δεύτερη σημαντική ανησυχία για την ασφάλεια είναι η
Δημοσιεύθηκε: Σεπτέμβριος 2, 2022
Σχήμα 1. Εφαρμογή του νόμου του Henry και της εξίσωσης του Antoine σε μια 2,0
κ.β. διάλυμα HN3 σε νερό στους 25 °C9
Editorialpubs.acs.org/joc
Δημοσιεύθηκε το 2022 από την American Chemical
Society 11293
h
ttps://doi.org/10.1021/acs.joc.2c01402
J. Org. Chem. 2022, 87, 11293-11295Κατέβηκε μέσω 73.170.156.34 στις 19 Ιανουαρίου 2024 στις 22:51:42 (UTC).
Δείτε https://pubs.acs.org/sharingguidelines για επιλογές σχετικά με τον τρόπο νόμιμης κοινοποίησης δημοσιευμένων άρθρων.
συνδυασμός αλάτων χαλκού και αζιδίου του νατρίου. Υπήρξαν
περισσότερες από δώδεκα τεκμηριωμένες εκρήξεις που προέρχονται από
αζίδιο του χαλκού(Ι), αζίδιο του χαλκού(ΙΙ), ή άγνωστα μείγματα από
χαλκού με αζίδιο του νατρίου ή υδραζοϊκό οξύ.10 Ο αριθμός των
ατόμων που σκοτώθηκαν από αυτές τις εκρήξεις είναι τουλάχιστον 16. Δεν υπάρχει
γενική βέλτιστη πρακτική για την προσθήκη μετάλλων μετάπτωσης σε αντιδράσεις
που περιέχουν ανόργανο αζίδιο ή υδραζοϊκό οξύ, επειδή μια τέτοια
πράξη είναι εξαιρετικά επικίνδυνη. Υψηλής εκρηκτικότητας, κρούσης, τριβής,
και στατικά ευαίσθητα άλατα αζιδίου έχουν παρασκευαστεί από Al, Ca,
Ti, V, Cr, Mn, Co, Ni, Cu, Zn, Mo, Pd, Ag, Cd, Sn, Sb, Te, Ba,
Pt, Au, Hg, Tl, Pb και Bi.4b Αζίδιο χαλκού(ΙΙ), ειδικότερα,
έχει αναφερθεί ότι είναι τόσο ευαίσθητο σε κρούσεις που το
διαταραχή του κρυσταλλικού στερεού, ακόμη και κάτω από το νερό, οδηγεί σε
βίαιη έκρηξη.10b Εξαιτίας αυτού, οι βιομηχανικές εγκαταστάσεις που
παρασκευάζουν ή χρησιμοποιούν ανόργανα αζίδια καταβάλλουν μεγάλη προσπάθεια να διασφαλίσουν ότι
τα μέταλλα αποκλείονται αυστηρά (π.χ. δεν υπάρχει αντιδραστήρας μετάλλων
μεταλλικά εξαρτήματα, μεταλλικά εξαρτήματα, μεταλλικά θερμοστοιχεία, όχι
ακόμη και οι αποχετεύσεις του δαπέδου καλύπτονται για να
αποτρέπουν το αζίδιο να εισέλθει στους χάλκινους σωλήνες).4b,e
Η τελευταία σημαντική ανησυχία για την ασφάλεια που αντιμετωπίζεται κατά τη διαδικασία
από τους Gazvoda et al. είναι η χρήση διχλωρομεθανίου στην
επεξεργασία. Όπως έχει αναφερθεί πολλές φορές, το
συνδυασμός ανόργανου αζιδίου και διχλωρομεθανίου μπορεί να
να οδηγήσει σε ιδιαίτερα εκρηκτικό, ευαίσθητο σε κρούση διαζιδωμεθάνιο. Όπως
με το υδραζοϊκό οξύ και το αζίδιο του χαλκού, αυτό το επικίνδυνο
ένωση έχει εμπλακεί σε πολλές εκρήξεις
συμπεριλαμβανομένων εκείνων που έχουν οδηγήσει σε σοβαρούς τραυματισμούς.11
Θα θέλαμε να κλείσουμε με μια ειλικρινή υπενθύμιση προς όλους
εργαστηριακούς χημικούς ότι η εργασία με ανόργανο αζίδιο απαιτεί
επιμέλεια. Κατά γενικό κανόνα, τα οξέα, οι αλογονωμένοι διαλύτες και τα
μέταλλα πρέπει να αποφεύγονται αυστηρά. Συνιστούμε περαιτέρω ότι
τόσο οι συγγραφείς όσο και οι αναθεωρητές να διατηρούν αυτές τις σοβαρές ανησυχίες για την ασφάλεια
κατά την προετοιμασία και την αξιολόγηση των χειρογράφων. Όλοι μας
πρέπει να κάνουμε το χρέος μας για να διαδώσουμε την ευαισθητοποίηση σχετικά με τους ακραίους κινδύνους για
να αποφύγουμε την επανάληψη των τραγικών λαθών του παρελθόντος.
Daniel S. Treitler orcid.org/0000-0001-5375-4920
Simon Leung
■ ΠΛΗΡΟΦΟΡΊΕΣ ΓΙΑ ΤΟΝ ΣΥΓΓΡΑΦΈΑ
Πλήρη στοιχεία επικοινωνίας είναι διαθέσιμα στη διεύθυνση:
h
ttps://pubs.acs.org/10.1021/acs.joc.2c01402
Σημειώσεις
Οι απόψεις που εκφράζονται σε αυτό το κύριο άρθρο είναι αυτές των συγγραφέων και
όχι απαραίτητα οι απόψεις του ACS.
Και οι δύο συγγραφείς είναι υπάλληλοι της Bristol Myers Squibb. Bristol
Myers Squibb συμμετείχε στην ανασκόπηση και έγκριση του παρόντος
χειρόγραφου.
■ ΕΥΧΑΡΙΣΤΙΕΣ
Οι συγγραφείς θα ήθελαν να ευχαριστήσουν θερμά τους Andrej Shemet και
Vladislav Lisnyak για τη βοήθεια στη μετάφραση των μη αγγλικών
δημοσιεύσεων. Επιπλέον, οι συγγραφείς οφείλουν ευχαριστίες στον Michael
Dummeldinger για τη βοήθεια που παρείχε με το νόμο του Henry/Antoine's
εξίσωση για το υδραζοϊκό οξύ στην αέρια φάση.
Οι συγγραφείς θα ήθελαν επίσης να ευχαριστήσουν τους Gregg Feigelson, Lakshmi
Narasimhan, Zachary Garlets, και Trevor Sherwood για τη βοήθειά τους.
την προσεκτική εξέταση του χειρογράφου.
■ ΑΝΑΦΟΡΕΣ
(1) Jankovič , D., Virant, M., Gazvoda, M. Copper-Catalyzed Azide-
Alkyne Cycloaddition of Hydrazoic Acid Formed In Situ from Sodium
Αζίδιο δίνει 4-μονοϋποκατεστημένα-1,2,3-τριαζόλια. J. Org. Chem. 2022,
87, 4018.
(2) Η επικοινωνία μας με τον καθηγητή Gazvoda προκάλεσε μια
διόρθωση της αρχικής δημοσίευσης: Jankovič , D., Virant, M,
Gazvoda, M. Διόρθωση στο "Copper-Catalyzed Azide-Alkyne Cyclo-
προσθήκη υδραζοϊκού οξέος που σχηματίζεται επιτόπου από αζίδιο του νατρίου
Αποδίδει 4-μονοϋποκατεστημένα-1,2,3-τριαζόλια". J. Org. Chem. 2022, 87,
8277.
(3) (α) Trout, D., Esswein, E. J., Hales, T., Brown, K., Solomon, G,
Miller, M. Εκθέσεις και επιπτώσεις στην υγεία: αξιολόγηση των εργαζομένων σε ένα
εργοστάσιο παραγωγής αζιδίου του νατρίου. Am. J. Ind. Med. 1996, 30, 343. (b)
Lewis, R. J., Sr. Sax's Dangerous Properties of Industrial Materials,
Wiley & Sons, Inc: Hoboken, 2004.
(4) (α) Fedoroff, B. T., Aaronson, H. A., Sheffield, O. E., Reese, E.
F., Clift, G. D. Encyclopedia of Explosives and Related Items.
Arsenal: Dover, 1960. (β) Fair, H. D., Walker, R. F., Ed. Energetic
Materials Vol 1: Physics and Chemistry of the Inorganic Azides- Plenum
Press: New York, 1977. (γ) Pepekin, V. I. Παράμετρος πυροδότησης
για εκρηκτικές ύλες. Polym. J. Chem. 1981, 55, 1405. (δ) Patnaik,
P. Ολοκληρωμένος οδηγός για τις επικίνδυνες ιδιότητες των χημικών
Van Nostrand Reinhold, 1992. (ε) Peer, M. Dangerous
αντιδράσεις. Αζίδιο του νατρίου στη βιομηχανική οργανική σύνθεση. Πληροφορίες
Chimie. 1997, 98. (στ) Urben, P. G., Ed. Bretherick's Handbook of
Reactive Chemical Hazards- Academic Press: Boston, 2007. (ζ) Wiss,
J., Fleury, C., Heuberger, C., Onken, U. Explosion and Decom-
position Characteristics of Hydrazoic Acid in Gas Phase. Org.
Process Res. Dev. 2007, 11, 1096.
(5) Curtius, T., Radenhausen, R. Για τη γνώση σχετικά με το
Αζίδιο του υδρογόνου. J. Prakt. Chem. 1891, 43, 207.
(6) (α) Kurbangalina, R. K., Patskov, E. A., Stesik, L. N., Yakovleva,
G. S. Detonation of liquid hydrazoic acid and its aqueous solutions.
Prikladnaya Mekhanika i Tekhnicheskaya Fizika 1970, 160. (β) Ertel,
D., Schmieder, H., Stollenwerk, A. H. Η συμπεριφορά του υδραζοϊκού οξέος.
σε διαλύματα διεργασίας PUREX υπό το πρίσμα της ασφάλειας. Nukleare Entsorgung
1989, 107. (γ) Ullman's Encyclopedia of Industrial Chemistry- VCH:
Νέα Υόρκη, 1989- τόμος Α13 "Hydrazoic Acid and Azides".
(7) (α) Betterton, E. A., Robinson, J. L. Συντελεστής του νόμου του Henry.
Υδραζοϊκού οξέος. J. Air Waste Manage. Assoc. 1997, 47, 1216.
(β) González-Bobes, F., Kopp, N., Li, L., Deerberg, J., Sharma, P.,
Leung, S., Davies, M., Bush, J., Hamm, J., Hrytsak, M. Scale-up of
Χημεία αζιδίων: Μια μελέτη περίπτωσης. Org. Process Res. Dev. 2012, 16, 2051.
(γ) Treitler, D. S., Leung, S., Lindrud, M. Ανάπτυξη και
επίδειξης ενός ασφαλέστερου πρωτοκόλλου για τη σύνθεση 5-
Aryltetrazoles από αρυλνιτρίλια. Org. Process Res. Dev. 2017, 21, 460.
(8) (α) Curtius, T. Abstracts: Σχετικά με το υδραζοϊκό οξύ (αζοϊμίδιο). J. Am.
Chem. Soc. 1890, 12, 472. (β) Browne, A. W., Lundell, G. E. F.
Άνυδρο υδρονιτρικό οξύ. Ι. Ηλεκτρόλυση διαλύματος καλίου
τρινιτριδίου σε υδρονιτρικό οξύ. J. Am. Chem. Soc. 1909, 31, 435.
(γ) Cooper-Key, A., Crozier, T. H., Thomas, R. A., Watts, H. E,
Malcolm, C. R. Fiftieth Annual Report of His Majesty's Inspectors of
Explosives- His Majesty's Stationary Office: Λονδίνο, 1926. (δ) Sha-
piro, E. L. Έκρηξη υδραζοϊκού οξέος. Chemical & Engineering News
(Bloomfield, NJ) 1974, Νο. Jan, 14. (ε) Sood, R. K., Nya, A. E. Short
σημείωση σχετικά με τη μη εκρηκτική απόσταξη του HN3. J. Therm. Anal. 1981, 20,
491. (στ) Υπουργείο Εργασίας των Ηνωμένων Πολιτειών της Αμερικής: Ασφάλεια στην εργασία και
Health Administration. Ατύχημα: 699603 - Θάνατος εργαζομένου σε βαρέλι
έκρηξη. Επιθεώρηση #102595436. Ημερομηνία συμβάντος 7 Οκτωβρίου 1995.
h
ttps://www.osha.gov/pls/imis/accidentsearch.accident_detail?id=
699603 (πρόσβαση 2022-05-27). (ζ) Crabbe, N. Γυαλί ενσωματωμένο σε
στην κοιλιά φοιτητή σε έκρηξη στο εργαστήριο. Gainesville Sun (Gainesville, FL)
2012, 18 Ιανουαρίου
https://www.gainesville.com/story/sports/college/
2012/01/18/glass-embedded-in-students-chest-abdomen-in-lab-
explosion/64271845007/ (πρόσβαση 2022-05-27). (η) Taton, T. A,
Partlo, W. E. Chemical Safety: Κίνδυνος έκρηξης στη σύνθεση
Chemical & Engineering News (Twin Cities, MN)
2014, 27 Οκτωβρίου.
(9) Σημείωση: Αυτή η φωτογραφία στήθηκε για σκοπούς επίδειξης- η
φιάλη δεν περιέχει στην πραγματικότητα διάλυμα υδραζοϊκού οξέος.
The Journal of Organic Chemistry pubs.acs.org/joc Editorial
h
ttps://doi.org/10.1021/acs.joc.2c01402
J. Org. Chem. 2022, 87, 11293-11295
11294
(10) α) Dennis, L. M., Isham, H. Hydronitric Acid, V. J. Am. Chem.
Soc. 1907, 29, 18. (β) Turrentine, J. W. Contributions to the
Ηλεκτροχημεία του υδρονιτρικού οξέος και των αλάτων του. Ι. Η διάβρωση του
ορισμένων μετάλλων σε διάλυμα τρινιτριδίου του νατρίου. J. Am. Chem. Soc. 1911, 33,
803. (γ) Hitch, A. R. Θερμική αποσύνθεση ορισμένων ανόργανων
Τρινιτρίδια. J. Am. Chem. Soc. 1918, 40, 1195. (δ) Cirulis, A. Χαλκός
αζίδιο και τα σύμπλοκά του. Naturwissenschaften 1939, 27, 583. (ε) Cirulis,
A. Οι εκρηκτικές ιδιότητες του Cu(N3)2. Zeitschrift fuer das Gesamte
Sciess- und Sprengstoffwesen 1943, 38, 42. (στ) Becher, H. H.
αζιδίου του νατρίου είναι επικίνδυνη. Naturwissenschaften 1970, 57, 671.
(ζ) Kabik, I., Urman, S. Κίνδυνοι του αζιδίου του χαλκού σε πυροκροτητές. Στο
Πρακτικά των πρακτικών του 14ου σεμιναρίου ασφάλειας εκρηκτικών υλών, Νέα Υόρκη.
Ορλεάνη, Λουιζιάνα - Συμβούλιο Ασφάλειας Εκρηκτικών του Υπουργείου Άμυνας,
1973. (η) Cowely, B. R., Oughton, J. F. Πυροδότηση βαρέων μετάλλων.
αζιδίων. Chemistry & Industry 1973, 444. (θ) Wear, J. O. CXX. Αζίδιο
Κίνδυνοι με αυτόματους μετρητές κυττάρων αίματος. Journal of Chemical
Education (Safety in the Chemical Laboratory Supplement) 1975, 52,
A23. ι) Pobiner, H. Chemical Safety (Χημική ασφάλεια): Αζίδιο του νατρίου.
Chemical & Engineering News (Princeton, NJ) 1982, αριθ. Απριλίου, 12.
(ια) Bentur, Y., Koren, G., McGuigan, M., Spielberg, S. P. An unusual
κλινική και φαρμακοκινητική αξιολόγηση.
Journal of Toxicology: 1988, 26, 371. (l) Sood, R.
K., Alobi, N. O. Cupric Azide - A New Detonator for Mining. Global
Journal of Pure & Applied Sciences 1997, 3, 69. (ιγ) Ατύχημα με όλμο
Μάλι- Ολλανδικό Συμβούλιο Ασφαλείας: Χάγη, 2017.
(11) (α) Bretherick, L. Azide-halosolvent hazards. Chemical &
Engineering News (Dorset, Ηνωμένο Βασίλειο) 1986, αριθ. Δεκεμβρίου, 22. (β) Peet, N.
P., Weintraub, P. M. Explosion with sodium azide in DMSO-CH2Cl2.
Chemical & Engineering News (Cincinatti, OH) 1993, Νο Απρίλιος, 19.
(γ) Hruby, V. J., Boteju, L., Li, G. Chemical Safety: Έκρηξη με
αζίδιο του νατρίου. Chemical & Engineering News (Tucson, AZ) 1993,
(δ) Conrow, R. E., Dean, W. D., Diazidomethane (Διαζιδομεθάνιο).
έκρηξη. Org. Process Res. Dev. 2008, 12, 1285.
The Journal of Organic Chemistry pubs.acs.org/joc Editorial
h
ttps://doi.org/10.1021/acs.joc.2c01402
J. Org. Chem. 2022, 87, 11293-11295
11295
Τώρα, λοιπόν, βγαίνει νόημα από όλα αυτά; Καταλαβαίνετε τους κινδύνους. Εάν όχι, αυτή η διαδρομή δεν είναι για τη μέση μέλισσα.