- Joined
- Apr 29, 2023
- Messages
- 78
- Reaction score
- 43
- Points
- 18
PPA HIPOFOSFORO Y YODO =D ANFETAMINA O USARLO PARA HACER 4 METILAMINOREX
InformaciónbásicaSeguridadPrecioUsoPreparaciónProductos Y MateriasprimasEspectroRelacionado

ChemicalBook CAS DataBase List Fenilpropanolamina
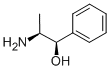
La fenilpropanolamina (PPA) es una amina simpaticomimética de acción mixta similar a la efedrina. Su principal mecanismo de acción es el agonismo a-adrenérgico directo, pero también se produce una estimulación indirecta de la liberación de norepinefrina. En noviembre de 2000, el Comité Asesor sobre Medicamentos de Venta sin Receta de la Administración de Alimentos y Medicamentos de EE.UU. (FDA) determinó que existe una asociación significativa entre la PPA y el ictus hemorrágico y recomendó que la PPA no se considerara segura para su uso sin receta. En ese momento, se envió una carta a los fabricantes solicitando la retirada voluntaria del PPA de sus productos. Más tarde, en 2005, la FDA publicó una monografía final provisional para los productos que contienen PPA en la que se proponía la categoría II (no reconocido generalmente como seguro y eficaz). Hasta la fecha, no se ha publicado ninguna monografía final; sin embargo, todos los fabricantes han eliminado el PPA de sus productos.
Autor
Propadrine, MSD ,US ,1941
Usos
La norefedrina, también llamada fenilpropanolamina (PPA), es una forma sintética del alcaloide efedrina. Se utiliza en el tratamiento de la incontinencia urinaria en perros y gatos; descongestionante nasal. Tras los informes sobre la aparición de hemorragias intracraneales y otros efectos adversos, incluidas varias muertes, la PPA ya no se vende en EE.UU. y Canadá.
Usos
Excitación nerviosa central
Usos
El PPA se utilizaba como descongestionante nasal y como anorexígeno. Los estudios han demostrado beneficios en humanos para la incontinencia urinaria, y el PPA se sigue utilizando en medicina veterinaria para este fin.
Definición
ChEBI: (-)-norefedrina es una anfetamina que es propilbenceno sustituido por un grupo hidroxi en la posición 1 y por un grupo amino en la posición 2 (el 1R,2S-estereoisómero). Es un alcaloide vegetal. Tiene una función como metabolito vegetal. Es un miembro de las anfetaminas y un alcaloide de la fenetilamina.
Proceso de fabricación
En una ruta descrita en la patente estadounidense 2.151.517, se agitan vigorosamente 10,7 kg de benzaldehído técnico con una solución de 11,0 kg de bisulfito sódico en 50,0 litros de agua hasta que se completa la formación del producto de adición. Simultáneamente, se disuelven 8,25 kg de nitroetano en una solución de 4,5 kg de sosa cáustica en 20,0 litros de agua y la solución caliente resultante se añade con agitación vigorosa al magma de bisulfito sódico de benzaldehído. La mezcla se agita durante 30 minutos y luego se deja reposar toda la noche.
La porción acuosa de la mezcla se separa ahora con un sifón de la capa sobrenadante de fenilnitropropanol aceitoso y se sustituye por una solución fresca de 11,0 kg de bisulfito sódico en 50,0 litros de agua. La mezcla de fenilnitropropanol y solución de bisulfito se agita enérgicamente durante 15 minutos para eliminar y recuperar pequeñas cantidades de benzaldehído sin reaccionar, y se deja estratificar de nuevo. Esta vez, el fenilnitropropanol se separa con un sifón y se filtra para eliminar una pequeña cantidad de material resinoso. La solución acuosa de bisulfito sódico que queda se hace reaccionar con benzaldehído, como se ha descrito anteriormente, con lo que el proceso es continuo.
El 1-fenil-2-nitropropanol así obtenido es un aceite incoloro, de gravedad específica 1,14 a 20°C, inodoro cuando es puro, volátil con vapor y que hierve entre 150° y 165°C bajo una presión de 5 mm de mercurio. Es soluble en alcohol, éter, acetona, cloroformo, tetracloruro de carbono, benceno y ácido acético glacial. El rendimiento del 1-fenil-2-nitropropanol obtenido por este procedimiento es de 17,1 a 17,7 kg.
Se hidrogenará y se convertirá en clorhidrato en los pasos siguientes. El cloruro de hidrógeno tiene un punto de fusión de 192°-194°C.
En una ruta alternativa descrita en la patente estadounidense 3.028.429, la propiofenona puede hacerse reaccionar con un nitrito de alquilo para dar isonitrosopropiofenona, que luego se hidrogenará y finalmente se convertirá en el clorhidrato.
nombre comercial
Ej.multix;Acutrim;Adistop-f;Amertuss;Amplisiex;Am-tuss liq;Anorexin;Antiadipositum;Apoephedrin;e Aridose;Arm;Bifed-20;Biphetane;Biphetap;Blu-hist;Brocon cr;Bromanate;Bromepaph;Brometapp;Bronco-quintoxil;Cenadex;Chlor-rest;Cinturex;Cletanol;Codimal;Cofpac;Cold cap;Coldecon;Col-decon;Conex-grippe;Contop;Coricidin f;Corsym;Coryztime;Cremacoat;Dalca;Decidex;Decomine;Demazine;Deprecstop;Dexatrim;D-sinus;Efed ii;Eficol;Endal;Endecon;Endex;E-son;Espornade spansule;E-tapp 3;Exyphen;Factus;Fornagest;Fugoa n;Gardax;Ginsopan;Headway;Histade;Histatapp;Hsp 540;Ipercron;Kol-tac;Kontexin;Koryza;Leder;Lipo-sinahist;Lunerin;Mardram;Minus-x;Monatuss;Mucolyt-expecto;Nd-hist;Nectatussin;Neosoldana;Nexaam;Nobese;Norefedrina;Nornatane;Ornacol;Ornatos;Ornex;Pabron nose;Panacorn;Panadyl;Parhist;Partapp;Pholcolix spansule;Pneumidex;Polcimut;Profenade;Propagest;Reduzin;Rhindecon;Rhinergal;Rhinervert;Rhinicept;Rhinidrin;Rhinocap;Rinexin;Rinomar;Rinotussal;Rinurel lictus;Rinurel comprimidos;Rinutan;Rotabromophen;Rupton;Rynatapp;Rynex;Ryza-gesic;Sacietyl;Scotuss;Secron;Sinacin;Sinudan;Sinu-lets;Sinutab cough l;Spandecon;Srda;Sto-caps;Sulfa-probocon;Symptrol;Taviset;Tinaroc;Totolin;Tricon;Tri-congestic;Triogesic elixir;Triominic;Triotussic;Turbispan;Tussilene-dm;V cold;Veltane;Veltap;Vernate;Vistaminic;Voxin-pg;W 58;X 112 antiadipo;Zerinol;Partuss;Permatrim;Phenapap.
Función Terapéutica
Descongestionante nasal, Anorexígeno
Organización Mundial de la Salud (OMS)
La fenilpropanolamina, una amina simpaticomimética, está ampliamente disponible en preparados de venta libre desde 1941. Es uno de los descongestionantes nasales más utilizados y es un ingrediente habitual en preparados para la reducción de peso, aunque se han planteado dudas sobre su utilidad en esta indicación. También se utiliza en la incontinencia de esfuerzo. Su uso se ha asociado a una elevación ocasional excesiva de la presión arterial, especialmente en individuos hipersensibles.
Descripción general
La fenilpropanolamina es el N-desmetilanálogo de la efedrina y, por tanto, tiene muchas propiedades similares. Al carecer del grupo N-metilo, la fenilpropanolamina es ligeramente más polar y, por tanto, no penetra en el SNC tan bien como la efedrina. Esta modificación le confiere una acción vasopresora ligeramente superior y una acción estimulante central inferior a la de la efedrina. Su acción como descongestionante nasal es más prolongada que la de la efedrina. La fenilpropanolamina era un componente activo común en los supresores del apetito y los medicamentos para la tos y el resfriado hasta 2001, cuando la Food and Drug Administration (FDA) recomendó su retirada de tales medicamentos, porque los estudios mostraron un mayor riesgo de accidente cerebrovascular hemorrágico en mujeres jóvenes que tomaban el fármaco.
Perfil de seguridad
Moderadamente tóxico por vía subcutánea. Cuando se calienta hasta descomponerse emite humos muy tóxicos de NOx.
Evaluación de la toxicidad
La acción primaria del PPA es el agonismo a-adrenérgico directo, aunque también provoca la liberación indirecta de norepinefrina en las terminales nerviosas simpáticas postganglionares. La PPA también tiene propiedades agonistas β débiles. La hipertensión es el resultado de la vasoconstricción de los vasos sanguíneos periféricos mediada por α adrenérgicos. Es frecuente la bradicardia refleja. Los efectos simpaticomiméticos pueden producir ansiedad, insomnio, agitación, temblor, taquicardia y midriasis.
FDS|CAS|Base de datos CAS|Nuevosproductos
Contacto|Versiónpara ordenador
Libro químico
InformaciónbásicaSeguridadPrecioUsoPreparaciónProductos Y MateriasprimasEspectroRelacionado

ChemicalBook CAS DataBase List Fenilpropanolamina

Fenilpropanolamina
- Nombre del productoFenilpropanolamina
- CAS14838-15-4
- Número CBNCB22131029
- MFC9H13NO
- MW151.21
- EINECS238-900-2
- Archivo MOL14838-15-4.mol
Propiedades químicas
| Punto de fusión | 101-101.5° |
| Punto de ebullición | 273,23°C (estimación aproximada) |
| Densidad | 1,0406 (estimación aproximada) |
| Índice de refracción | 1,5380 (estimación) |
| pka | pKa 9.19(H2O,t =25±0.5,I=0.01)(aproximado) |
| color | Placas de H2O |
| FDA UNII | 33RU150WUN |
| Referencia química NIST | Benzenemethanol, «alpha»-(1-aminoethyl)-, (r*,s*)-(.+/-.)-(14838-15-4) |
| Código ATC | R01BA01,R01BA51 |
| Sistema de registro de sustancias de la EPA | Phenylpropanolamine (14838-15-4) |
Seguridad
| Datos sobre sustancias peligrosas | 14838-15-4(Datos sobre sustancias peligrosas) |
| Toxicidad | DL50 scu-rata: 850 mg/kg JPETAB 85,199,45 |
Fenilpropanolamina Precio
Fenilpropanolamina Propiedades químicas,Uso,Producción
DescripciónLa fenilpropanolamina (PPA) es una amina simpaticomimética de acción mixta similar a la efedrina. Su principal mecanismo de acción es el agonismo a-adrenérgico directo, pero también se produce una estimulación indirecta de la liberación de norepinefrina. En noviembre de 2000, el Comité Asesor sobre Medicamentos de Venta sin Receta de la Administración de Alimentos y Medicamentos de EE.UU. (FDA) determinó que existe una asociación significativa entre la PPA y el ictus hemorrágico y recomendó que la PPA no se considerara segura para su uso sin receta. En ese momento, se envió una carta a los fabricantes solicitando la retirada voluntaria del PPA de sus productos. Más tarde, en 2005, la FDA publicó una monografía final provisional para los productos que contienen PPA en la que se proponía la categoría II (no reconocido generalmente como seguro y eficaz). Hasta la fecha, no se ha publicado ninguna monografía final; sin embargo, todos los fabricantes han eliminado el PPA de sus productos.
Autor
Propadrine, MSD ,US ,1941
Usos
La norefedrina, también llamada fenilpropanolamina (PPA), es una forma sintética del alcaloide efedrina. Se utiliza en el tratamiento de la incontinencia urinaria en perros y gatos; descongestionante nasal. Tras los informes sobre la aparición de hemorragias intracraneales y otros efectos adversos, incluidas varias muertes, la PPA ya no se vende en EE.UU. y Canadá.
Usos
Excitación nerviosa central
Usos
El PPA se utilizaba como descongestionante nasal y como anorexígeno. Los estudios han demostrado beneficios en humanos para la incontinencia urinaria, y el PPA se sigue utilizando en medicina veterinaria para este fin.
Definición
ChEBI: (-)-norefedrina es una anfetamina que es propilbenceno sustituido por un grupo hidroxi en la posición 1 y por un grupo amino en la posición 2 (el 1R,2S-estereoisómero). Es un alcaloide vegetal. Tiene una función como metabolito vegetal. Es un miembro de las anfetaminas y un alcaloide de la fenetilamina.
Proceso de fabricación
En una ruta descrita en la patente estadounidense 2.151.517, se agitan vigorosamente 10,7 kg de benzaldehído técnico con una solución de 11,0 kg de bisulfito sódico en 50,0 litros de agua hasta que se completa la formación del producto de adición. Simultáneamente, se disuelven 8,25 kg de nitroetano en una solución de 4,5 kg de sosa cáustica en 20,0 litros de agua y la solución caliente resultante se añade con agitación vigorosa al magma de bisulfito sódico de benzaldehído. La mezcla se agita durante 30 minutos y luego se deja reposar toda la noche.
La porción acuosa de la mezcla se separa ahora con un sifón de la capa sobrenadante de fenilnitropropanol aceitoso y se sustituye por una solución fresca de 11,0 kg de bisulfito sódico en 50,0 litros de agua. La mezcla de fenilnitropropanol y solución de bisulfito se agita enérgicamente durante 15 minutos para eliminar y recuperar pequeñas cantidades de benzaldehído sin reaccionar, y se deja estratificar de nuevo. Esta vez, el fenilnitropropanol se separa con un sifón y se filtra para eliminar una pequeña cantidad de material resinoso. La solución acuosa de bisulfito sódico que queda se hace reaccionar con benzaldehído, como se ha descrito anteriormente, con lo que el proceso es continuo.
El 1-fenil-2-nitropropanol así obtenido es un aceite incoloro, de gravedad específica 1,14 a 20°C, inodoro cuando es puro, volátil con vapor y que hierve entre 150° y 165°C bajo una presión de 5 mm de mercurio. Es soluble en alcohol, éter, acetona, cloroformo, tetracloruro de carbono, benceno y ácido acético glacial. El rendimiento del 1-fenil-2-nitropropanol obtenido por este procedimiento es de 17,1 a 17,7 kg.
Se hidrogenará y se convertirá en clorhidrato en los pasos siguientes. El cloruro de hidrógeno tiene un punto de fusión de 192°-194°C.
En una ruta alternativa descrita en la patente estadounidense 3.028.429, la propiofenona puede hacerse reaccionar con un nitrito de alquilo para dar isonitrosopropiofenona, que luego se hidrogenará y finalmente se convertirá en el clorhidrato.
nombre comercial
Ej.multix;Acutrim;Adistop-f;Amertuss;Amplisiex;Am-tuss liq;Anorexin;Antiadipositum;Apoephedrin;e Aridose;Arm;Bifed-20;Biphetane;Biphetap;Blu-hist;Brocon cr;Bromanate;Bromepaph;Brometapp;Bronco-quintoxil;Cenadex;Chlor-rest;Cinturex;Cletanol;Codimal;Cofpac;Cold cap;Coldecon;Col-decon;Conex-grippe;Contop;Coricidin f;Corsym;Coryztime;Cremacoat;Dalca;Decidex;Decomine;Demazine;Deprecstop;Dexatrim;D-sinus;Efed ii;Eficol;Endal;Endecon;Endex;E-son;Espornade spansule;E-tapp 3;Exyphen;Factus;Fornagest;Fugoa n;Gardax;Ginsopan;Headway;Histade;Histatapp;Hsp 540;Ipercron;Kol-tac;Kontexin;Koryza;Leder;Lipo-sinahist;Lunerin;Mardram;Minus-x;Monatuss;Mucolyt-expecto;Nd-hist;Nectatussin;Neosoldana;Nexaam;Nobese;Norefedrina;Nornatane;Ornacol;Ornatos;Ornex;Pabron nose;Panacorn;Panadyl;Parhist;Partapp;Pholcolix spansule;Pneumidex;Polcimut;Profenade;Propagest;Reduzin;Rhindecon;Rhinergal;Rhinervert;Rhinicept;Rhinidrin;Rhinocap;Rinexin;Rinomar;Rinotussal;Rinurel lictus;Rinurel comprimidos;Rinutan;Rotabromophen;Rupton;Rynatapp;Rynex;Ryza-gesic;Sacietyl;Scotuss;Secron;Sinacin;Sinudan;Sinu-lets;Sinutab cough l;Spandecon;Srda;Sto-caps;Sulfa-probocon;Symptrol;Taviset;Tinaroc;Totolin;Tricon;Tri-congestic;Triogesic elixir;Triominic;Triotussic;Turbispan;Tussilene-dm;V cold;Veltane;Veltap;Vernate;Vistaminic;Voxin-pg;W 58;X 112 antiadipo;Zerinol;Partuss;Permatrim;Phenapap.
Función Terapéutica
Descongestionante nasal, Anorexígeno
Organización Mundial de la Salud (OMS)
La fenilpropanolamina, una amina simpaticomimética, está ampliamente disponible en preparados de venta libre desde 1941. Es uno de los descongestionantes nasales más utilizados y es un ingrediente habitual en preparados para la reducción de peso, aunque se han planteado dudas sobre su utilidad en esta indicación. También se utiliza en la incontinencia de esfuerzo. Su uso se ha asociado a una elevación ocasional excesiva de la presión arterial, especialmente en individuos hipersensibles.
Descripción general
La fenilpropanolamina es el N-desmetilanálogo de la efedrina y, por tanto, tiene muchas propiedades similares. Al carecer del grupo N-metilo, la fenilpropanolamina es ligeramente más polar y, por tanto, no penetra en el SNC tan bien como la efedrina. Esta modificación le confiere una acción vasopresora ligeramente superior y una acción estimulante central inferior a la de la efedrina. Su acción como descongestionante nasal es más prolongada que la de la efedrina. La fenilpropanolamina era un componente activo común en los supresores del apetito y los medicamentos para la tos y el resfriado hasta 2001, cuando la Food and Drug Administration (FDA) recomendó su retirada de tales medicamentos, porque los estudios mostraron un mayor riesgo de accidente cerebrovascular hemorrágico en mujeres jóvenes que tomaban el fármaco.
Perfil de seguridad
Moderadamente tóxico por vía subcutánea. Cuando se calienta hasta descomponerse emite humos muy tóxicos de NOx.
Evaluación de la toxicidad
La acción primaria del PPA es el agonismo a-adrenérgico directo, aunque también provoca la liberación indirecta de norepinefrina en las terminales nerviosas simpáticas postganglionares. La PPA también tiene propiedades agonistas β débiles. La hipertensión es el resultado de la vasoconstricción de los vasos sanguíneos periféricos mediada por α adrenérgicos. Es frecuente la bradicardia refleja. Los efectos simpaticomiméticos pueden producir ansiedad, insomnio, agitación, temblor, taquicardia y midriasis.
Productos de preparación y materias primas
Materias primasFenilpropanolamina Espectro
14838-15-4, FenilpropanolaminaBúsqueda relacionada
Enviar consultaFDS|CAS|Base de datos CAS|Nuevosproductos
Contacto|Versiónpara ordenador
Libro químico
