Agilent1100DAD
Newbie
No niin, kaverit! Aika jakaa hieman tietoa kanssanne. Kuvaan psilosiinille tekemäni synteesin, joka on varustettu valokuvilla. Käytin tuotettua psilosiinia ja kehitin yksinkertaisen liimalaastarin. Jotta voisimme testata psilosiinin läpäisevyyttä laastarissa, käytimme kokoamaani diffuusiolaitteistoa. Siihen kuuluu useita kalvoja, ja 1 cm^2 laastari asetetaan 1 cm^2 :n palan 400 um:n paksuisen tuoreen ihmisen ihon päälle (lahjoitettu vatsanpoistokirurgisesta keskuksesta). Ihon alla on jatkuva virtaus vettä, jonka pH on 7,4 ja ruumiinlämpötila. Diffuusiolaitteisto pystyy keräämään 1 ml:n fraktion tunnissa, joka analysoidaan sitten LC-MS:llä. Psilosiinin määrä 1 ml:n injektiopullossa antaa virtauksen (mg/h/cm^2). Tämä kertoo, kuinka paljon psilosiinia kulkee tunnissa, kun laastarin koko on cm^2.
Tämä menee syvemmälle, koska psilosiini on erittäin epävakaa. seuraavassa julkaisussa Structure Elucidation and Spectroscopic Analysis of Chromophores Produced by Oxidative Psilocin Dimerization käsitellään asiaa. Kun dimeeri muodostuu, sitä ei voida havaita HPLC-analyysin ja ATR-FTIR-analyysin avulla, mikä on outoa. Tämä antaa tutkimusryhmille vääriä positiivisia tuloksia psilosiinin puhtaudesta. Olen löytänyt tavan stabiloida psilosiini laastarissa.
Joka tapauksessa, aloitetaan! Tein kaikki vaiheet itse, ja apunani oli kumppanini, joka on kemiantekniikan insinööri. Tämä tapahtui silloin, kun minulla oli schedule1- ja 3 DEA-lupa paitsi tutkimukseen myös valmistukseen.
Osa I (Psilosiinisynteesi)
Vaihe 1: 3-[2-(2-(dimetyyliamino)-2-oksoasetyyli]-1H-indoli-4-yyliasetaatin synteesi.
1a. 2000 ml:n nelikaulainen, pyöreäpohjainen pullo varustettiin yläpuolisella sekoittimella, J-Kem-lämpötilan säätimellä, 250 ml:n tippusuppilolla ja kumiseinällä, jonka läpi johdettiin ylipaineista kuivaaN2:ta. Septumi poistettiin ja kolviin annosteltiin yhtä paljon 1H-indoli-4-yyliasetaattia (5; 50,1 g, 285 mmol, 1 ekvivalentti).
ja anhyd Et2O (700 ml). Pullo suljettiin uudelleen septumilla ja huuhdellaan N2:lla. Suspensiota sekoitettiin 10 min ja sitten
jäähdytettiin 0 °C:seen jäävesihauteessa 30 min. ajan.

1b. Tippusuppiloon annettiin oksalyylikloridin (37,1 ml, 428 mmol, 1,5 ekvivalenttia) liuos Et2O:ssa (60 ml). Oksalyylikloridiliuosta lisättiin pisaroittain riittävällä nopeudella, jotta lämpötila pysyi 5 °C:ssa tai sen alapuolella, jotta minimoitiin dimeerin ja muun mahdollisen sivutuotteen muodostuminen. Lisäyksen edetessä muodostui keltaista lietettä 10, ja kun lisäys oli saatu päätökseen, seosta sekoitettiin 4 tuntia.

1c. Tämän jälkeen lisättiin heptaania (400 ml) ja seosta sekoitettiin 30 minuuttia 0 °C:ssa. Saatu keltainen kiinteä aine suodatettiin nopeasti ja huuhdeltiin peräkkäin heptaanilla (2 × 300 ml), joka käytettiin nopeasti seuraavassa vaiheessa. . Dimetyyliamiinin 2,0 M:n liuos THF:ssä (175 ml) lisättiin pisaroittain riittävällä nopeudella pitämään lämpötila alle 5 °C:ssa sivureaktioiden minimoimiseksi. Kun
Kun lisäys oli valmis, lisättiin pyridiini (46 ml) THF:ään (100 ml) pisaroittain ja seosta sekoitettiin hyvin 60 minuutin ajan. Heptaania (600 ml) lisättiin ja pullon sisältö imusuodatettiin Büchnerin suppilon kautta. Suodatettu jäännös siirrettiin pyöreäpohjaiseen kolviin ja lisättiin deionisoitua H2O:ta (1000 ml), sekoitettiin 30 min ja suodatettiin Büchner-suppilon kautta. Luonnonvalkoinen kiinteä aine trituroitiin peräkkäin 40 minuutin ajan EtOAc:ssa (600 ml) ja heptaanissa (400 ml). Liete suodatettiin Büchner-suppilon kautta ja kiinteä aine kuivattiin uunissa 40 °C:ssa yön yli, jolloin saatiin 6 vaaleankeltaisena kiinteänä aineena; saanto: 66,1 g (81 %); mp 205-207 °C.



ATR-FTIR vahvisti 3-[2-(dimetyyliamino)-2-oksoasetyyli]-1H-indoli-4-yyliasetaatin synteesin. Tämä yhdiste voidaan säilyttää 4C:ssa useita kuukausia!
Vaihe 2: Psilosiinin synteesi
Vaihe 2A: 2000 ml:n nelikaulainen, pyöreäpohjainen pullo varustettiin yläpuolisella sekoittimella, J-Kem-lämpötilansäätimellä, a
250 ml:n tippusuppilo ja kuminen septumi, jonka läpi johdettiin ylipaineista kuivaa N2:ta. Septumi poistettiin ja
pulloon annosteltiin peräkkäin 3-[2-(2-(dimetyyliamino)-2-oksoasetyyli]-1H-indoli-4-yyliasetaattia (6; 31,5 g, 115 mmol) ja 2-CH3-THF:ää (1000 mg).
ml). Kolvi upotettiin 0 °C:n jäähauteeseen ja lisättiin 2,3 M LiAlH4:n liuos 2-CH3-THF:ssä (140 ml, 322 mmol) 2-CH3-THF:n kautta.
250 ml:n tippusuppilon kautta. Tippusuppilo huuhdeltiin ylimääräisellä 2-CH3-THF:llä (20 ml). LiAlH4-liuosta lisättiin pisaroittain seuraavasti
niin, että lämpötila pysyi alle 20 °C:n. Lisäyksen jälkeen jäävesihaute poistettiin ja seosta sekoitettiin 30 minuuttia.
Vaaleankeltainen liuos kuumennettiin refluksiliuokseen (80 °C) kuumennusvaipan avulla, ja se muuttui norsunluun väriseksi 3 tunnin kuluttua.
havaittiin keltaisen kiintoaineen kertymistä pyöreäpohjaisen pullon sivuille.



Vaihe 2C. Lämmitysvaippa poistettiin, ja pullon annettiin jäähtyä 50 °C:seen. Kolvi jäähdytettiin jälleen
jäähdytettiin jälleen 20 °C:seen. Reaktio sammutettiin lisäämällä peräkkäin 3 tippaa 1 M NaOH:ta ja 3 tippaa deionisoitua H2O:ta. Seos
laimennettiin THF:llä (500 ml) ja sekoitettiin 20 minuuttia. Seos suodatettiin Büchner-suppilon kautta ja suodos säilytettiin N2:ssa.
Suodatinkakku huuhdottiin nopeasti uudelleen 200 ml:lla [10 % liuosta (7 % ammoniakkia MeOH:ssa) CH2Cl2:ssa] ja THF:llä (500 ml). Suodokset
yhdistettiin ja konsentroitiin, jolloin saatiin vihreää kiinteää ainetta. Kiinteä aine tritratoitiin 1:1 EtOAc/heptaani (50 ml) ja suodatettiin sitten suodattimen kautta.
Büchner-suppilon läpi. Tummanvihreä kiinteä aine kuivattiin uunissa 40 °C:ssa yön yli, jolloin saatiin kuivaa psilosiinia (7) tummanvihreänä kiinteänä aineena; saanto: 20,7 %.
g (91 %); mp 167-169 °C.
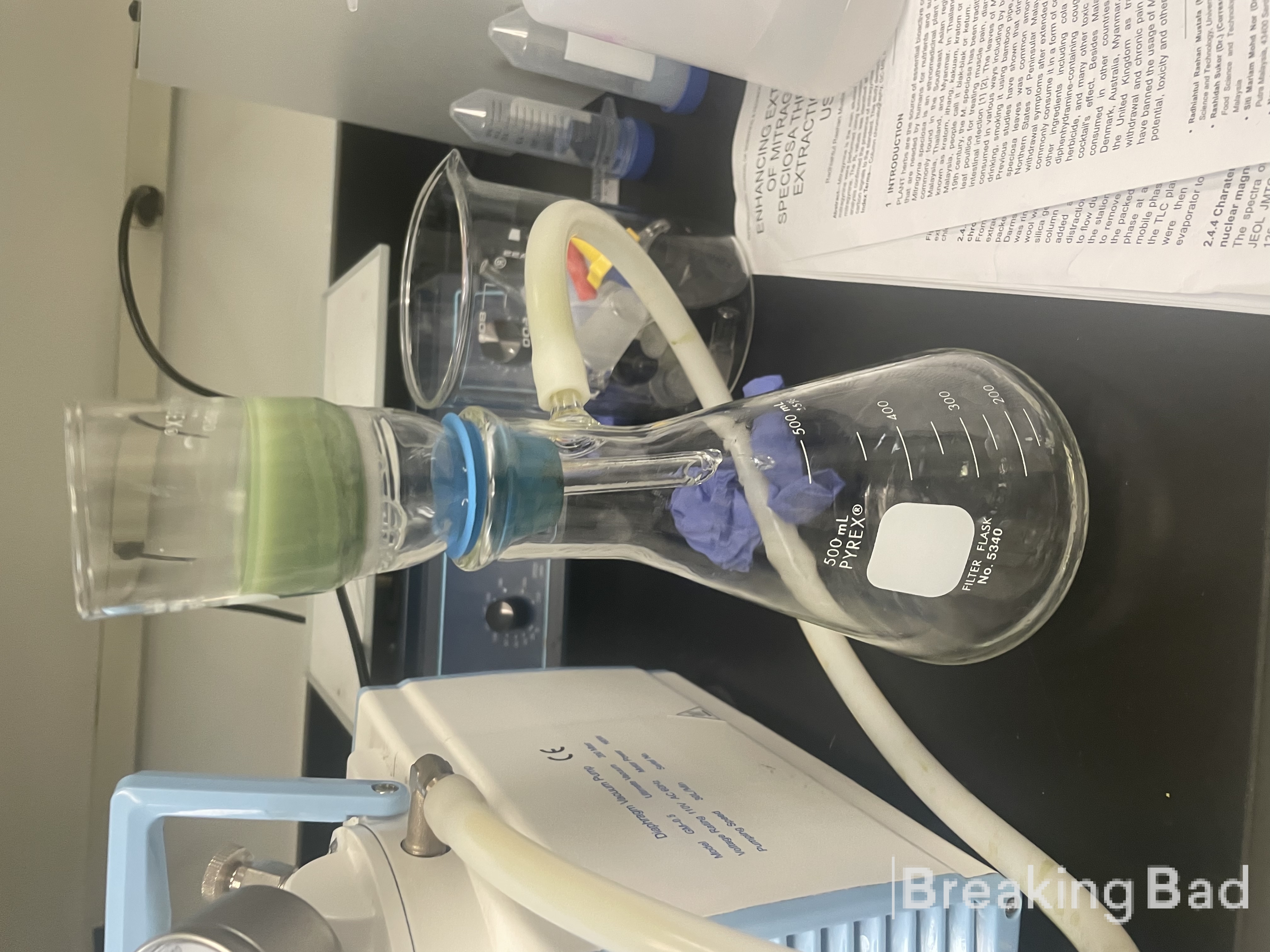


Psilosiini on syntetisoitu.
Osa II: Transdermaalisen psilosiinilaastarin kehittäminen ja In-Vitro-tutkimus (VAROITUS: NÄET TUOREEN IHMISEN ELÄIMEN, SEN RASKAAN
Liuotan sitten psilosiinin omaan akrylaattipolymeeriseokseen (heptaanissa), valan liuoksen irrotuslinjaan ja käytän valuveitsiä saadakseni liimakerroksen 100 um:iin. Kun se on kuivunut, levitän taustakerroksen ja rei'itän 1 cm^2 kokoisen laastarin. Tätä laastaria käytetään in vitro -tutkimuksessa.
Seuraavassa kuvassa on tilannekuva diffuusiolaitteesta (laastari ihon päällä, kun vesi valuu sen alla).

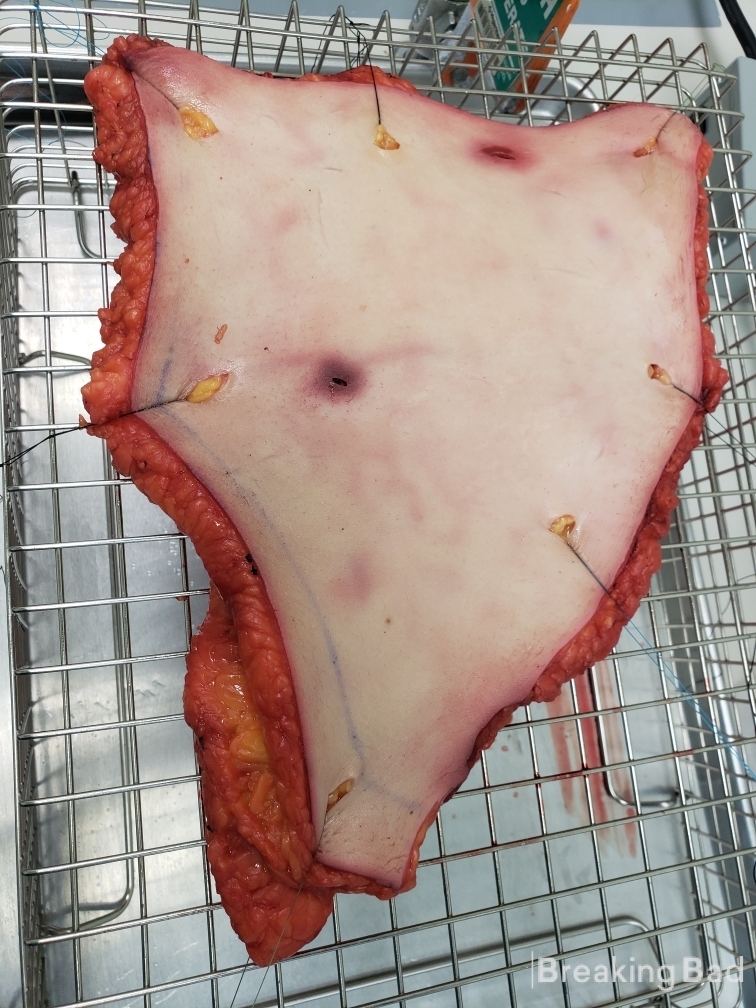
Toivottavasti nautitte!
Tämä menee syvemmälle, koska psilosiini on erittäin epävakaa. seuraavassa julkaisussa Structure Elucidation and Spectroscopic Analysis of Chromophores Produced by Oxidative Psilocin Dimerization käsitellään asiaa. Kun dimeeri muodostuu, sitä ei voida havaita HPLC-analyysin ja ATR-FTIR-analyysin avulla, mikä on outoa. Tämä antaa tutkimusryhmille vääriä positiivisia tuloksia psilosiinin puhtaudesta. Olen löytänyt tavan stabiloida psilosiini laastarissa.
Joka tapauksessa, aloitetaan! Tein kaikki vaiheet itse, ja apunani oli kumppanini, joka on kemiantekniikan insinööri. Tämä tapahtui silloin, kun minulla oli schedule1- ja 3 DEA-lupa paitsi tutkimukseen myös valmistukseen.
Osa I (Psilosiinisynteesi)
Vaihe 1: 3-[2-(2-(dimetyyliamino)-2-oksoasetyyli]-1H-indoli-4-yyliasetaatin synteesi.
1a. 2000 ml:n nelikaulainen, pyöreäpohjainen pullo varustettiin yläpuolisella sekoittimella, J-Kem-lämpötilan säätimellä, 250 ml:n tippusuppilolla ja kumiseinällä, jonka läpi johdettiin ylipaineista kuivaaN2:ta. Septumi poistettiin ja kolviin annosteltiin yhtä paljon 1H-indoli-4-yyliasetaattia (5; 50,1 g, 285 mmol, 1 ekvivalentti).
ja anhyd Et2O (700 ml). Pullo suljettiin uudelleen septumilla ja huuhdellaan N2:lla. Suspensiota sekoitettiin 10 min ja sitten
jäähdytettiin 0 °C:seen jäävesihauteessa 30 min. ajan.
1b. Tippusuppiloon annettiin oksalyylikloridin (37,1 ml, 428 mmol, 1,5 ekvivalenttia) liuos Et2O:ssa (60 ml). Oksalyylikloridiliuosta lisättiin pisaroittain riittävällä nopeudella, jotta lämpötila pysyi 5 °C:ssa tai sen alapuolella, jotta minimoitiin dimeerin ja muun mahdollisen sivutuotteen muodostuminen. Lisäyksen edetessä muodostui keltaista lietettä 10, ja kun lisäys oli saatu päätökseen, seosta sekoitettiin 4 tuntia.
1c. Tämän jälkeen lisättiin heptaania (400 ml) ja seosta sekoitettiin 30 minuuttia 0 °C:ssa. Saatu keltainen kiinteä aine suodatettiin nopeasti ja huuhdeltiin peräkkäin heptaanilla (2 × 300 ml), joka käytettiin nopeasti seuraavassa vaiheessa. . Dimetyyliamiinin 2,0 M:n liuos THF:ssä (175 ml) lisättiin pisaroittain riittävällä nopeudella pitämään lämpötila alle 5 °C:ssa sivureaktioiden minimoimiseksi. Kun
Kun lisäys oli valmis, lisättiin pyridiini (46 ml) THF:ään (100 ml) pisaroittain ja seosta sekoitettiin hyvin 60 minuutin ajan. Heptaania (600 ml) lisättiin ja pullon sisältö imusuodatettiin Büchnerin suppilon kautta. Suodatettu jäännös siirrettiin pyöreäpohjaiseen kolviin ja lisättiin deionisoitua H2O:ta (1000 ml), sekoitettiin 30 min ja suodatettiin Büchner-suppilon kautta. Luonnonvalkoinen kiinteä aine trituroitiin peräkkäin 40 minuutin ajan EtOAc:ssa (600 ml) ja heptaanissa (400 ml). Liete suodatettiin Büchner-suppilon kautta ja kiinteä aine kuivattiin uunissa 40 °C:ssa yön yli, jolloin saatiin 6 vaaleankeltaisena kiinteänä aineena; saanto: 66,1 g (81 %); mp 205-207 °C.
ATR-FTIR vahvisti 3-[2-(dimetyyliamino)-2-oksoasetyyli]-1H-indoli-4-yyliasetaatin synteesin. Tämä yhdiste voidaan säilyttää 4C:ssa useita kuukausia!
Vaihe 2: Psilosiinin synteesi
Vaihe 2A: 2000 ml:n nelikaulainen, pyöreäpohjainen pullo varustettiin yläpuolisella sekoittimella, J-Kem-lämpötilansäätimellä, a
250 ml:n tippusuppilo ja kuminen septumi, jonka läpi johdettiin ylipaineista kuivaa N2:ta. Septumi poistettiin ja
pulloon annosteltiin peräkkäin 3-[2-(2-(dimetyyliamino)-2-oksoasetyyli]-1H-indoli-4-yyliasetaattia (6; 31,5 g, 115 mmol) ja 2-CH3-THF:ää (1000 mg).
ml). Kolvi upotettiin 0 °C:n jäähauteeseen ja lisättiin 2,3 M LiAlH4:n liuos 2-CH3-THF:ssä (140 ml, 322 mmol) 2-CH3-THF:n kautta.
250 ml:n tippusuppilon kautta. Tippusuppilo huuhdeltiin ylimääräisellä 2-CH3-THF:llä (20 ml). LiAlH4-liuosta lisättiin pisaroittain seuraavasti
niin, että lämpötila pysyi alle 20 °C:n. Lisäyksen jälkeen jäävesihaute poistettiin ja seosta sekoitettiin 30 minuuttia.
Vaaleankeltainen liuos kuumennettiin refluksiliuokseen (80 °C) kuumennusvaipan avulla, ja se muuttui norsunluun väriseksi 3 tunnin kuluttua.
havaittiin keltaisen kiintoaineen kertymistä pyöreäpohjaisen pullon sivuille.
Vaihe 2C. Lämmitysvaippa poistettiin, ja pullon annettiin jäähtyä 50 °C:seen. Kolvi jäähdytettiin jälleen
jäähdytettiin jälleen 20 °C:seen. Reaktio sammutettiin lisäämällä peräkkäin 3 tippaa 1 M NaOH:ta ja 3 tippaa deionisoitua H2O:ta. Seos
laimennettiin THF:llä (500 ml) ja sekoitettiin 20 minuuttia. Seos suodatettiin Büchner-suppilon kautta ja suodos säilytettiin N2:ssa.
Suodatinkakku huuhdottiin nopeasti uudelleen 200 ml:lla [10 % liuosta (7 % ammoniakkia MeOH:ssa) CH2Cl2:ssa] ja THF:llä (500 ml). Suodokset
yhdistettiin ja konsentroitiin, jolloin saatiin vihreää kiinteää ainetta. Kiinteä aine tritratoitiin 1:1 EtOAc/heptaani (50 ml) ja suodatettiin sitten suodattimen kautta.
Büchner-suppilon läpi. Tummanvihreä kiinteä aine kuivattiin uunissa 40 °C:ssa yön yli, jolloin saatiin kuivaa psilosiinia (7) tummanvihreänä kiinteänä aineena; saanto: 20,7 %.
g (91 %); mp 167-169 °C.
Psilosiini on syntetisoitu.
Osa II: Transdermaalisen psilosiinilaastarin kehittäminen ja In-Vitro-tutkimus (VAROITUS: NÄET TUOREEN IHMISEN ELÄIMEN, SEN RASKAAN
Liuotan sitten psilosiinin omaan akrylaattipolymeeriseokseen (heptaanissa), valan liuoksen irrotuslinjaan ja käytän valuveitsiä saadakseni liimakerroksen 100 um:iin. Kun se on kuivunut, levitän taustakerroksen ja rei'itän 1 cm^2 kokoisen laastarin. Tätä laastaria käytetään in vitro -tutkimuksessa.
Seuraavassa kuvassa on tilannekuva diffuusiolaitteesta (laastari ihon päällä, kun vesi valuu sen alla).
Toivottavasti nautitte!


