- Joined
- Apr 29, 2023
- Messages
- 78
- Reaction score
- 43
- Points
- 18
PPA HIPOFOSFOROSO E IODO =D ANFETAMINA OU USÁ-LO PARA FAZER 4 METILAMINOREX
InformaçõesbásicasSegurançaPreçoUsoPreparaçãoProdutos ematérias-primasEspectroRelacionados

ChemicalBook CAS DataBase List Phenylpropanolamine
A fenilpropanolamina (PPA) é uma amina simpaticomimética de ação mista semelhante à efedrina. Seu principal mecanismo de ação é por meio do agonismo a-adrenérgico direto, mas também há estimulação indireta da liberação de norepinefrina. Em novembro de 2000, o Comitê Consultivo de Medicamentos Isentos de Prescrição da Administração de Alimentos e Medicamentos dos EUA (FDA) determinou que há uma associação significativa entre o PPA e o derrame hemorrágico e recomendou que o PPA não fosse considerado seguro para uso sem prescrição médica. Nessa ocasião, foi emitida uma carta aos fabricantes solicitando a remoção voluntária do PPA de seus produtos. Posteriormente, em 2005, a FDA publicou uma Monografia Final Provisória para produtos contendo PPA, propondo o status de Categoria II (geralmente não reconhecido como seguro e eficaz). Até o momento, nenhuma monografia final foi publicada; entretanto, todos os fabricantes removeram o PPA de seus produtos.
Origem
Propadrine, MSD, EUA, 1941
Usos
A norefedrina, também chamada de fenilpropanolamina (PPA), é uma forma sintética do alcaloide efedrina. Usada no tratamento de incontinência urinária em cães e gatos; descongestionante nasal. Após relatos de ocorrência de hemorragia intracraniana e outros efeitos adversos, incluindo várias mortes, o PPA não é mais vendido nos EUA e no Canadá.
Usos
Excitação do sistema nervoso central
Usos
O PPA era usado como descongestionante nasal e como anorexígeno. Estudos demonstraram benefícios em humanos para incontinência urinária, e o PPA ainda é usado na medicina veterinária para essa finalidade.
Definição
ChEBI: a (-)-norefedrina é uma anfetamina que é propilbenzeno substituído por um grupo hidroxi na posição 1 e por um grupo amino na posição 2 (o estereoisômero 1R,2S). É um alcaloide vegetal. Tem um papel como metabólito vegetal. É um membro das anfetaminas e um alcaloide de fenetilamina.
Processo de fabricação
Em uma rota descrita na Patente dos EUA 2.151.517, 10,7 kg de benzaldeído técnico são vigorosamente agitados com uma solução de 11,0 kg de bissulfito de sódio em 50,0 litros de água até que a formação do produto de adição esteja completa. Simultaneamente, 8,25 kg de nitroetano são dissolvidos em uma solução de 4,5 kg de soda cáustica em 20,0 litros de água e a solução quente resultante é adicionada com agitação vigorosa ao magma de bissulfito de sódio de benzaldeído. A mistura é agitada por 30 minutos e depois deixada em repouso durante a noite.
A porção aquosa da mistura é agora extraída da camada sobrenadante de fenilnitropropanol oleoso e substituída por uma nova solução de 11,0 kg de bissulfito de sódio em 50,0 litros de água. A mistura de fenilnitropropanol e solução de bissulfito é agitada vigorosamente por 15 minutos para remover e recuperar pequenas quantidades de benzaldeído que não reagiu e, em seguida, é novamente deixada estratificar. Dessa vez, o fenilnitropropanol é sifonado e filtrado para remover uma pequena quantidade de material resinoso. A solução aquosa de bissulfito de sódio remanescente é reagida com benzaldeído, conforme descrito acima, tornando o processo contínuo.
O 1-fenil-2-nitropropanol assim obtido é um óleo incolor, com gravidade específica de 1,14 a 20°C, inodoro quando puro, volátil com vapor e ebulição de 150° a 165°C sob uma pressão de 5 mm de mercúrio. É solúvel em álcool, éter, acetona, clorofórmio, tetracloreto de carbono, benzeno e ácido acético glacial. O rendimento do 1-fenil-2-nitropropanol obtido por esse procedimento é de 17,1 a 17,7 kg.
Ele é hidrogenado e convertido em cloridrato nas etapas subsequentes. O cloreto de hidrogênio tem um ponto de fusão de 192° a 194°C.
Em uma rota alternativa descrita na Patente dos EUA 3.028.429, a propiofenona pode ser reagida com um nitrito de alquila para dar isonitrosopropiofenona, que é então hidrogenada e finalmente convertida em cloridrato.
nome comercial
A.g.multix;Acutrim;Adistop-f;Amertuss;Amplisiex;Am-tuss liq;Anorexin;Antiadipositum;Apoephedrin;e Aridose;Arm;Bifed-20;Biphetane;Biphetap;Blu-hist;Brocon cr;Bromanate;Bromepaph;Brometapp;Bronco-quintoxil;Cenadex;Chlor-rest;Cinturex;Cletanol;Codimal;Cofpac;Cold cap;Coldecon;Col-decon;Conex-grippe;Contop;Coricidin f;Corsym;Coryztime;Cremacoat;Dalca;Decidex;Decomine;Demazine;Deprecstop;Dexatrim;D-sinus;Efed ii;Eficol;Endal;Endecon;Endex;E-son;Espornade spansule;E-tapp 3;Exyphen;Factus;Fornagest;Fugoa n;Gardax;Ginsopan;Headway;Histade;Histatapp;Hsp 540;Ipercron;Kol-tac;Kontexin;Koryza;Leder;Lipo-sinahist;Lunerin;Mardram;Minus-x;Monatuss;Mucolyt-expecto;Nd-hist;Nectatussin;Neosoldana;Nexaam;Nobese;Norephedrine;Nornatane;Ornacol;Ornatos;Ornex;Pabron nose;Panacorn;Panadyl;Parhist;Partapp;Pholcolix spansule;Pneumidex;Polcimut;Profenade;Propagest;Reduzin;Rhindecon;Rhinergal;Rhinervert;Rhinicept;Rhinidrin;Rhinocap;Rinexin;Rinomar;Rinotussal;Rinurel lictus;Rinurel comprimidos;Rinutan;Rotabromophen;Rupton;Rynatapp;Rynex;Ryza-gesic;Sacietyl;Scotuss;Secron;Sinacin;Sinudan;Sinu-lets;Sinutab cough l;Spandecon;Srda;Sto-caps;Sulfa-probocon;Symptrol;Taviset;Tinaroc;Totolin;Tricon;Tri-congestic;Triogesic elixir;Triominic;Triotussic;Turbispan;Tussilene-dm;V cold;Veltane;Veltap;Vernate;Vistaminic;Voxin-pg;W 58;X 112 antiadipo;Zerinol;Partuss;Permatrim;Phenapap.
Função terapêutica
Descongestionante nasal, anorexígeno
Organização Mundial da Saúde (OMS)
A fenilpropanolamina, uma amina simpaticomimética, está amplamente disponível em preparações de venda livre desde 1941. É um dos descongestionantes nasais mais usados e é um ingrediente comum em preparações para redução de peso, embora tenham sido levantadas dúvidas sobre sua utilidade nessa indicação. Também é usado na incontinência de estresse. Seu uso tem sido associado à elevação excessiva ocasional da pressão arterial, especialmente em indivíduos hipersensíveis.
Descrição geral
A fenilpropanolamina é o N-desmetilanalógico da efedrina e, portanto, tem muitas propriedades semelhantes. Sem o grupo N-metil, a fenilpropanolamina é ligeiramente mais polar e, portanto, não entra no SNC tão bem quanto a efedrina. Essa modificação resulta em um agente com ação vasopressora ligeiramente maior e ação estimuladora central menor do que a da efedrina. Sua ação como descongestionante nasal é mais prolongada do que a da efedrina. A fenilpropanolamina era um componente ativo comum em inibidores de apetite e medicamentos para tosse e resfriado da OTC até 2001, quando a Food and Drug Administration (FDA) recomendou sua remoção desses medicamentos, pois estudos mostraram um risco maior de derrame hemorrágico em mulheres jovens que tomavam o medicamento.
Perfil de segurança
Moderadamente tóxico por via subcutânea. Quando aquecido até a decomposição, emite fumaça muito tóxica de NOx.
Avaliação da toxicidade
A ação primária do PPA é o agonismo a-adrenérgico direto, embora também cause a liberação indireta de norepinefrina nos terminais nervosos simpáticos pós-ganglionares. O PPA também tem propriedades agonistas β fracas. A hipertensão resulta da vasoconstrição mediada por α adrenérgicos dos vasos sanguíneos periféricos. A bradicardia reflexa é comum. Os efeitos simpaticomiméticos podem produzir ansiedade, insônia, agitação, tremor, taquicardia e midríase.
MSDS|CAS|CASDataBase|Novosprodutos
Entre em contatoconosco|Versãopara computador
Livro de Química
InformaçõesbásicasSegurançaPreçoUsoPreparaçãoProdutos ematérias-primasEspectroRelacionados

ChemicalBook CAS DataBase List Phenylpropanolamine

Fenilpropanolamina
- Nome do produtoFenilpropanolamina
- CAS14838-15-4
- Número CBCB22131029
- MFC9H13NO
- MW151.21
- EINECS238-900-2
- Arquivo MOL14838-15-4.mol
Propriedades químicas
| Ponto de fusão | 101-101.5° |
| Ponto de ebulição | 273,23°C (estimativa aproximada) |
| Densidade | 1,0406 (estimativa aproximada) |
| Índice de refração | 1,5380 (estimativa) |
| pka | pKa 9,19(H2O,t =25±0,5,I=0,01)(aproximado) |
| cor | Placas de H2O |
| FDA UNII | 33RU150WUN |
| Referência química NIST | Benzenemethanol, «alpha»-(1-aminoethyl)-, (r*,s*)-(.+/-.)-(14838-15-4) |
| Código ATC | R01BA01,R01BA51 |
| Sistema de Registro de Substâncias da EPA | Phenylpropanolamine (14838-15-4) |
Segurança
| Dados de substâncias perigosas | 14838-15-4(Dados de Substâncias Perigosas) |
| Toxicidade | LD50 scu-rat: 850 mg/kg JPETAB 85,199,45 |
Preço da fenilpropanolamina
Fenilpropanolamina Propriedades químicas, uso e produção
DescriçãoA fenilpropanolamina (PPA) é uma amina simpaticomimética de ação mista semelhante à efedrina. Seu principal mecanismo de ação é por meio do agonismo a-adrenérgico direto, mas também há estimulação indireta da liberação de norepinefrina. Em novembro de 2000, o Comitê Consultivo de Medicamentos Isentos de Prescrição da Administração de Alimentos e Medicamentos dos EUA (FDA) determinou que há uma associação significativa entre o PPA e o derrame hemorrágico e recomendou que o PPA não fosse considerado seguro para uso sem prescrição médica. Nessa ocasião, foi emitida uma carta aos fabricantes solicitando a remoção voluntária do PPA de seus produtos. Posteriormente, em 2005, a FDA publicou uma Monografia Final Provisória para produtos contendo PPA, propondo o status de Categoria II (geralmente não reconhecido como seguro e eficaz). Até o momento, nenhuma monografia final foi publicada; entretanto, todos os fabricantes removeram o PPA de seus produtos.
Origem
Propadrine, MSD, EUA, 1941
Usos
A norefedrina, também chamada de fenilpropanolamina (PPA), é uma forma sintética do alcaloide efedrina. Usada no tratamento de incontinência urinária em cães e gatos; descongestionante nasal. Após relatos de ocorrência de hemorragia intracraniana e outros efeitos adversos, incluindo várias mortes, o PPA não é mais vendido nos EUA e no Canadá.
Usos
Excitação do sistema nervoso central
Usos
O PPA era usado como descongestionante nasal e como anorexígeno. Estudos demonstraram benefícios em humanos para incontinência urinária, e o PPA ainda é usado na medicina veterinária para essa finalidade.
Definição
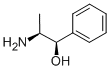
ChEBI: a (-)-norefedrina é uma anfetamina que é propilbenzeno substituído por um grupo hidroxi na posição 1 e por um grupo amino na posição 2 (o estereoisômero 1R,2S). É um alcaloide vegetal. Tem um papel como metabólito vegetal. É um membro das anfetaminas e um alcaloide de fenetilamina.
Processo de fabricação
Em uma rota descrita na Patente dos EUA 2.151.517, 10,7 kg de benzaldeído técnico são vigorosamente agitados com uma solução de 11,0 kg de bissulfito de sódio em 50,0 litros de água até que a formação do produto de adição esteja completa. Simultaneamente, 8,25 kg de nitroetano são dissolvidos em uma solução de 4,5 kg de soda cáustica em 20,0 litros de água e a solução quente resultante é adicionada com agitação vigorosa ao magma de bissulfito de sódio de benzaldeído. A mistura é agitada por 30 minutos e depois deixada em repouso durante a noite.
A porção aquosa da mistura é agora extraída da camada sobrenadante de fenilnitropropanol oleoso e substituída por uma nova solução de 11,0 kg de bissulfito de sódio em 50,0 litros de água. A mistura de fenilnitropropanol e solução de bissulfito é agitada vigorosamente por 15 minutos para remover e recuperar pequenas quantidades de benzaldeído que não reagiu e, em seguida, é novamente deixada estratificar. Dessa vez, o fenilnitropropanol é sifonado e filtrado para remover uma pequena quantidade de material resinoso. A solução aquosa de bissulfito de sódio remanescente é reagida com benzaldeído, conforme descrito acima, tornando o processo contínuo.
O 1-fenil-2-nitropropanol assim obtido é um óleo incolor, com gravidade específica de 1,14 a 20°C, inodoro quando puro, volátil com vapor e ebulição de 150° a 165°C sob uma pressão de 5 mm de mercúrio. É solúvel em álcool, éter, acetona, clorofórmio, tetracloreto de carbono, benzeno e ácido acético glacial. O rendimento do 1-fenil-2-nitropropanol obtido por esse procedimento é de 17,1 a 17,7 kg.
Ele é hidrogenado e convertido em cloridrato nas etapas subsequentes. O cloreto de hidrogênio tem um ponto de fusão de 192° a 194°C.
Em uma rota alternativa descrita na Patente dos EUA 3.028.429, a propiofenona pode ser reagida com um nitrito de alquila para dar isonitrosopropiofenona, que é então hidrogenada e finalmente convertida em cloridrato.
nome comercial
A.g.multix;Acutrim;Adistop-f;Amertuss;Amplisiex;Am-tuss liq;Anorexin;Antiadipositum;Apoephedrin;e Aridose;Arm;Bifed-20;Biphetane;Biphetap;Blu-hist;Brocon cr;Bromanate;Bromepaph;Brometapp;Bronco-quintoxil;Cenadex;Chlor-rest;Cinturex;Cletanol;Codimal;Cofpac;Cold cap;Coldecon;Col-decon;Conex-grippe;Contop;Coricidin f;Corsym;Coryztime;Cremacoat;Dalca;Decidex;Decomine;Demazine;Deprecstop;Dexatrim;D-sinus;Efed ii;Eficol;Endal;Endecon;Endex;E-son;Espornade spansule;E-tapp 3;Exyphen;Factus;Fornagest;Fugoa n;Gardax;Ginsopan;Headway;Histade;Histatapp;Hsp 540;Ipercron;Kol-tac;Kontexin;Koryza;Leder;Lipo-sinahist;Lunerin;Mardram;Minus-x;Monatuss;Mucolyt-expecto;Nd-hist;Nectatussin;Neosoldana;Nexaam;Nobese;Norephedrine;Nornatane;Ornacol;Ornatos;Ornex;Pabron nose;Panacorn;Panadyl;Parhist;Partapp;Pholcolix spansule;Pneumidex;Polcimut;Profenade;Propagest;Reduzin;Rhindecon;Rhinergal;Rhinervert;Rhinicept;Rhinidrin;Rhinocap;Rinexin;Rinomar;Rinotussal;Rinurel lictus;Rinurel comprimidos;Rinutan;Rotabromophen;Rupton;Rynatapp;Rynex;Ryza-gesic;Sacietyl;Scotuss;Secron;Sinacin;Sinudan;Sinu-lets;Sinutab cough l;Spandecon;Srda;Sto-caps;Sulfa-probocon;Symptrol;Taviset;Tinaroc;Totolin;Tricon;Tri-congestic;Triogesic elixir;Triominic;Triotussic;Turbispan;Tussilene-dm;V cold;Veltane;Veltap;Vernate;Vistaminic;Voxin-pg;W 58;X 112 antiadipo;Zerinol;Partuss;Permatrim;Phenapap.
Função terapêutica
Descongestionante nasal, anorexígeno
Organização Mundial da Saúde (OMS)
A fenilpropanolamina, uma amina simpaticomimética, está amplamente disponível em preparações de venda livre desde 1941. É um dos descongestionantes nasais mais usados e é um ingrediente comum em preparações para redução de peso, embora tenham sido levantadas dúvidas sobre sua utilidade nessa indicação. Também é usado na incontinência de estresse. Seu uso tem sido associado à elevação excessiva ocasional da pressão arterial, especialmente em indivíduos hipersensíveis.
Descrição geral
A fenilpropanolamina é o N-desmetilanalógico da efedrina e, portanto, tem muitas propriedades semelhantes. Sem o grupo N-metil, a fenilpropanolamina é ligeiramente mais polar e, portanto, não entra no SNC tão bem quanto a efedrina. Essa modificação resulta em um agente com ação vasopressora ligeiramente maior e ação estimuladora central menor do que a da efedrina. Sua ação como descongestionante nasal é mais prolongada do que a da efedrina. A fenilpropanolamina era um componente ativo comum em inibidores de apetite e medicamentos para tosse e resfriado da OTC até 2001, quando a Food and Drug Administration (FDA) recomendou sua remoção desses medicamentos, pois estudos mostraram um risco maior de derrame hemorrágico em mulheres jovens que tomavam o medicamento.
Perfil de segurança
Moderadamente tóxico por via subcutânea. Quando aquecido até a decomposição, emite fumaça muito tóxica de NOx.
Avaliação da toxicidade
A ação primária do PPA é o agonismo a-adrenérgico direto, embora também cause a liberação indireta de norepinefrina nos terminais nervosos simpáticos pós-ganglionares. O PPA também tem propriedades agonistas β fracas. A hipertensão resulta da vasoconstrição mediada por α adrenérgicos dos vasos sanguíneos periféricos. A bradicardia reflexa é comum. Os efeitos simpaticomiméticos podem produzir ansiedade, insônia, agitação, tremor, taquicardia e midríase.
Produtos de preparação e matérias-primas
Matérias-primasEspectro da fenilpropanolamina
14838-15-4, FenilpropanolaminaPesquisa relacionada
Enviar ConsultaMSDS|CAS|CASDataBase|Novosprodutos
Entre em contatoconosco|Versãopara computador
Livro de Química
