Brain
Expert Pharmacologist
- Joined
- Jul 6, 2021
- Messages
- 290
- Reaction score
- 304
- Points
- 63
Каннабис сатива - природный источник каннабиноидов. Это двудомное растение, имеющее отдельные экземпляры с мужскими и женскими цветками. Каннабис достаточно неприхотлив, чтобы выращивать его в промышленных масштабах. Она издавна служила источником материала для тканей и веревок: знаменитые пеньковые канаты изготавливались из конопляных волокон. Кроме того, различные части конопли использовались в качестве косметических средств и корма. Психоактивные свойства конопли также были известны людям, но в таком виде она использовалась редко. Промышленная эксплуатация конопли была серьезно ограничена в 1961 году в связи с вступлением в силу "Единой конвенции о наркотических средствах". Несмотря на то, что во многих странах были приняты законы, запрещающие использование производных конопли, в настоящее время ее употребляют в качестве наркотика 130-230 миллионов человек.
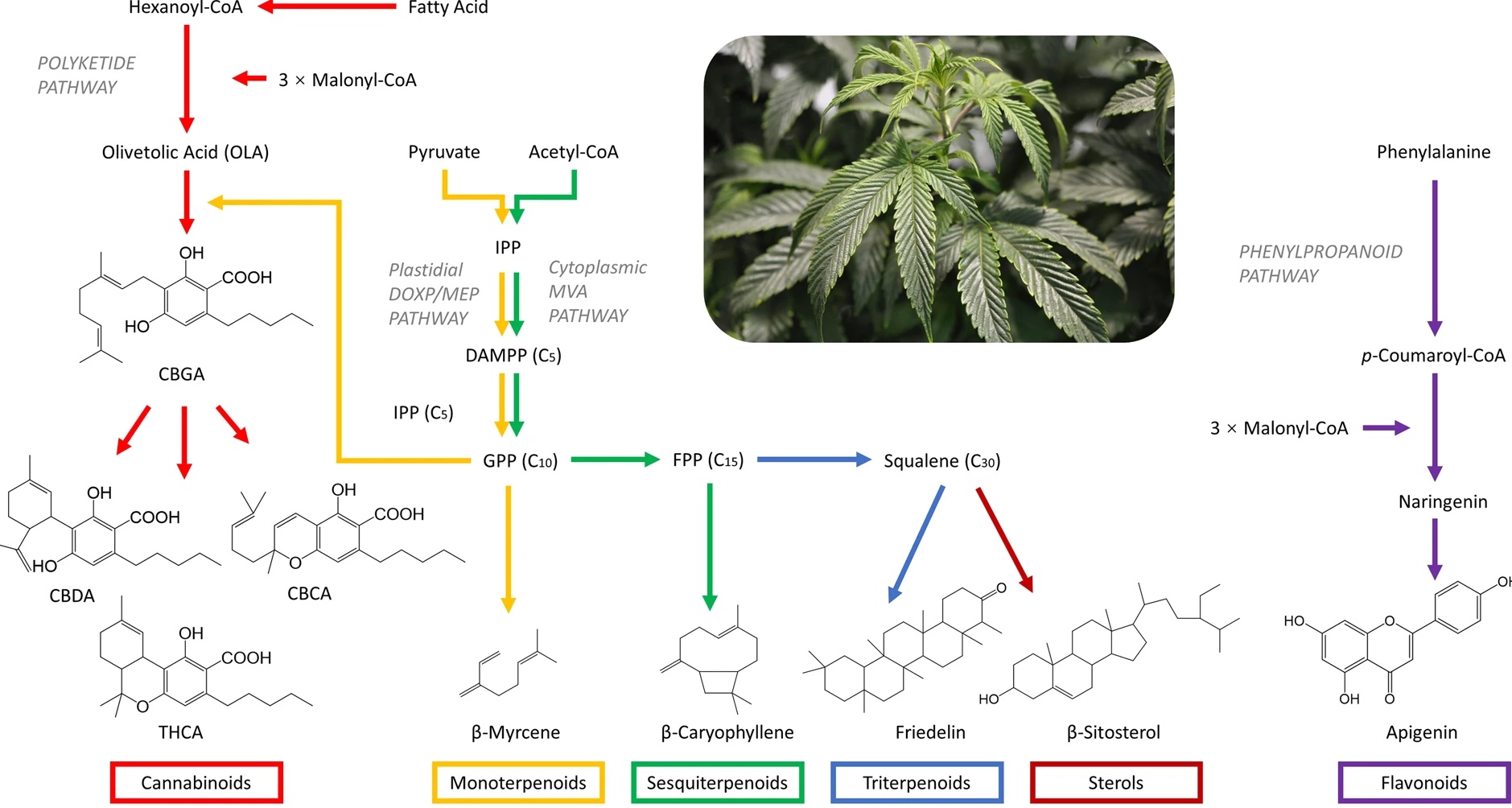
Психоактивное действие каннабиса обусловлено каннабиноидами - группой терпенфенольных соединений растительного происхождения. Известны десятки каннабиноидов, но самым мощным по психоактивному воздействию является Δ9-тетрагидроканнабиол. Другие представители семейства каннабиноидов обладают ими в меньшей степени. Каннабиноиды образуются в растениях двумя путями. Поликетидный путь предполагает их синтез из оливетоловой кислоты. Второй путь более сложный: он основан на производстве геранилдифосфата с последующим синтезом монотерпенов. Интересно, зачем конопле вообще нужна эта группа веществ? Скорее всего, как и в случае с никотином, каннабиноиды являются защитным фактором от насекомых. Не совсем понятно, оказывают ли они прямое воздействие на центральную нервную систему насекомых или влияют на них каким-то другим способом, но их эффективность в этой роли не может быть оспорена.
В недавнем исследовании, проведенном Институтом молекулярной медицины в Лиссабоне совместно с учеными из британского Ланкастерского университета, было заявлено, что длительное употребление каннабиса ухудшает память. Этот вывод, как утверждается, верен как для людей, употребляющих его рекреационно, так и для тех, кто принимает каннабиносодержащие препараты для лечения некоторых форм эпилепсии, хронической боли и рассеянного склероза. Специалисты Ланкастерского университета изучили действие особого препарата под названием WIN-55,212 и обнаружили у подопытных животных серьезные нарушения памяти. В результате длительного применения препарата во время этологического эксперимента мыши не могли отличить знакомый объект от нового. Кроме того, в ходе функциональных исследований мозга животных были визуализированы определенные нарушения в некоторых областях, задействованных в памяти и обучении. Все это, собственно, и лежит в основе негативного влияния каннабиса на процесс запоминания.
Еще в 2012 году исследователи под руководством Абуша доказали, что длительное употребление каннабиса статистически значимо связано с когнитивной дисфункцией и повышенным риском развития симптомов психических расстройств, включая спектр шизофренических расстройств. На животных моделях было выявлено, что негативное влияние каннабиноидов на обучение и память связано с дисфункцией долговременного потенцирования синаптической передачи. Также с уменьшением модификации нейронных колебаний, моделируемых габаергическими интернейронами, и с изменением активности в моноаминергических и холинергических путях гиппокампа, играющих важную роль в пластичности и других важных процессах.
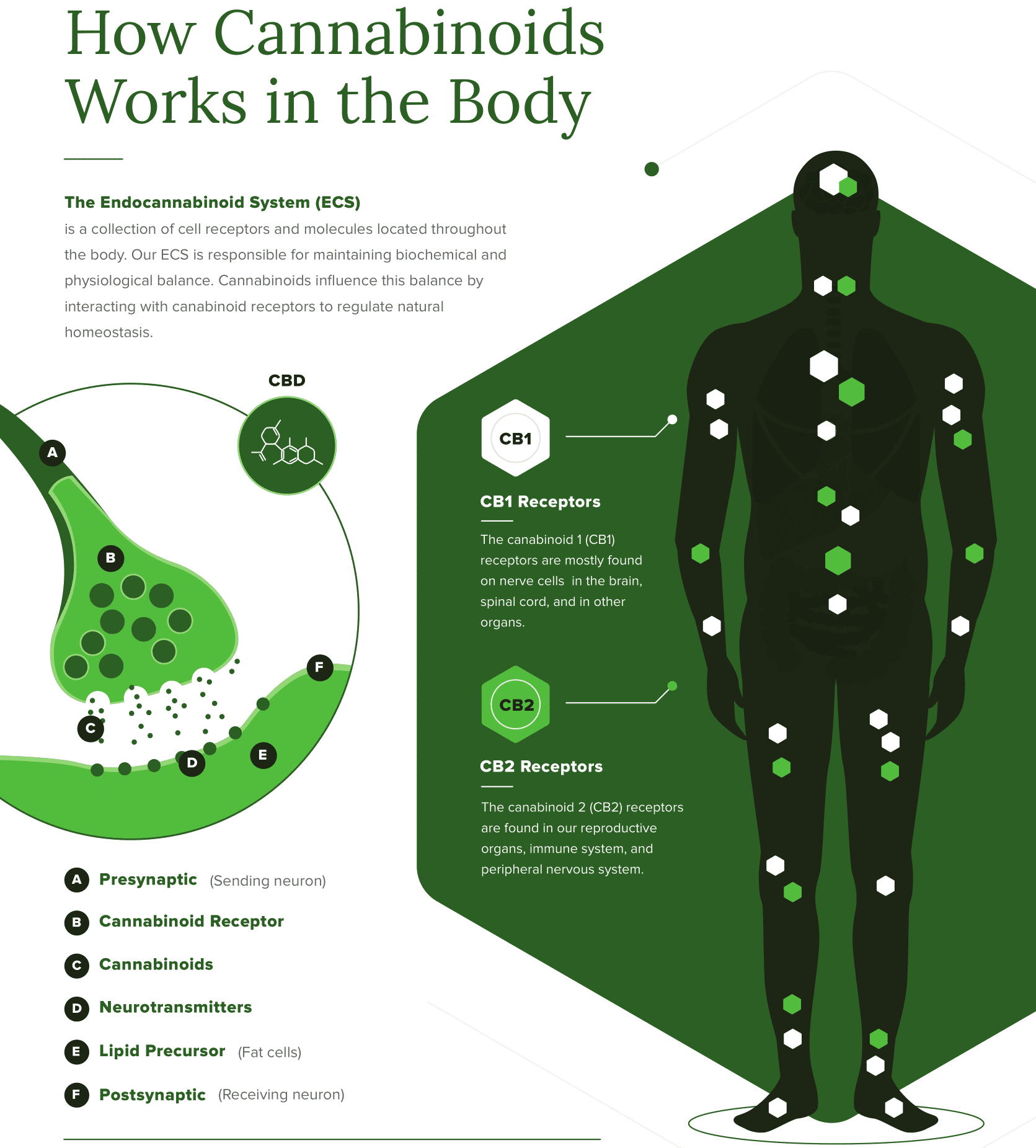
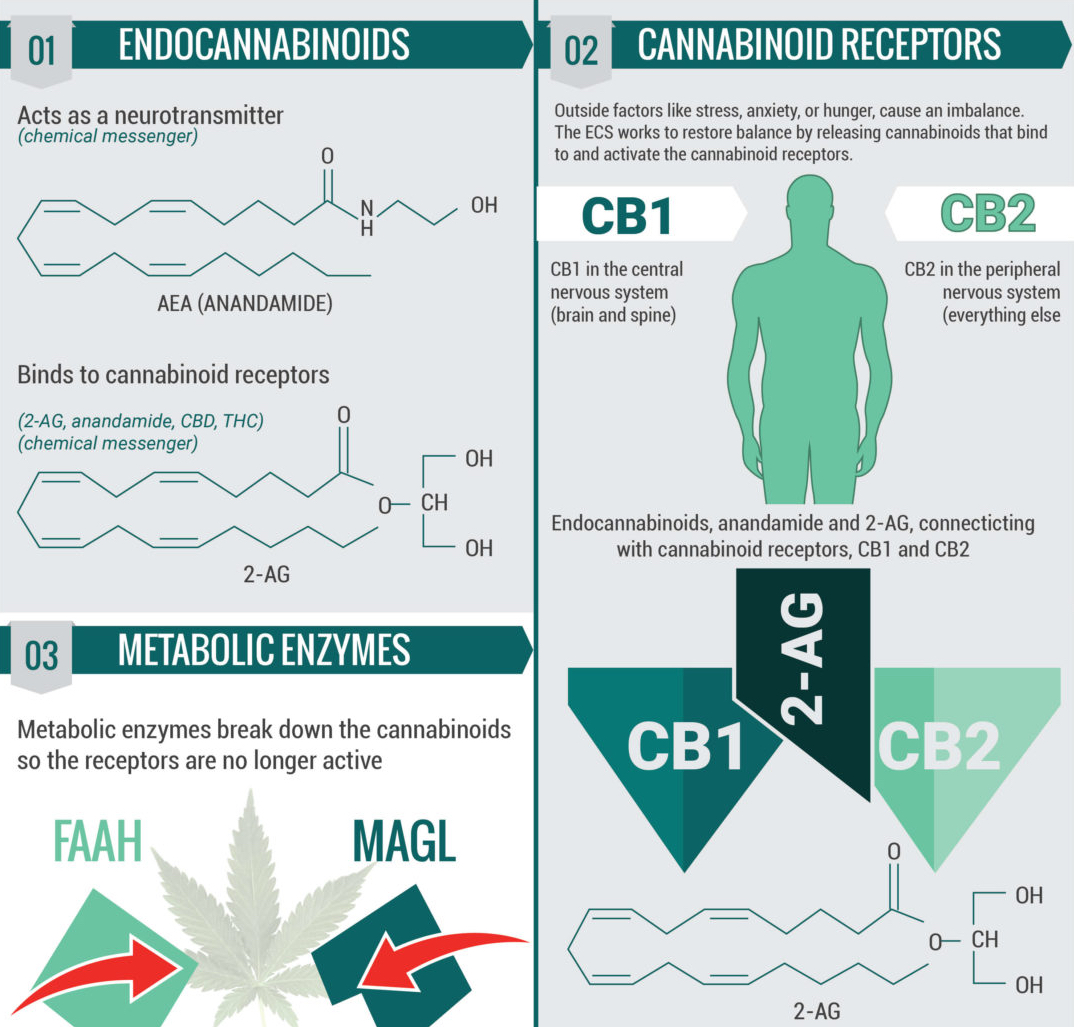
Ученые уже давно пытались найти цель действия каннабиноидов. Это было сделано в 1988 году, когда был описан первый тип каннабиноидных рецепторов (CB1-рецепторы). В 1993 году был открыт и второй тип рецепторов (CB2-рецепторы). CB1-рецепторы расположены в центральной нервной системе. Активация и блокировка CB1 влияет на процессы памяти, нейропротекции, ноцицепции. Помимо мозга, их можно обнаружить в печени, миокарде, почках, желудочно-кишечном тракте, легких, а также в эндотелиальной выстилке и мышечной стенке кровеносных сосудов. CB2 широко представлен в иммунных и эндотелиальных клетках. Синтетические каннабиноиды, входящие в состав курительных смесей, в основном стимулируют CB1-рецепторы, поэтому эти вещества изменяют психическое состояние человека.
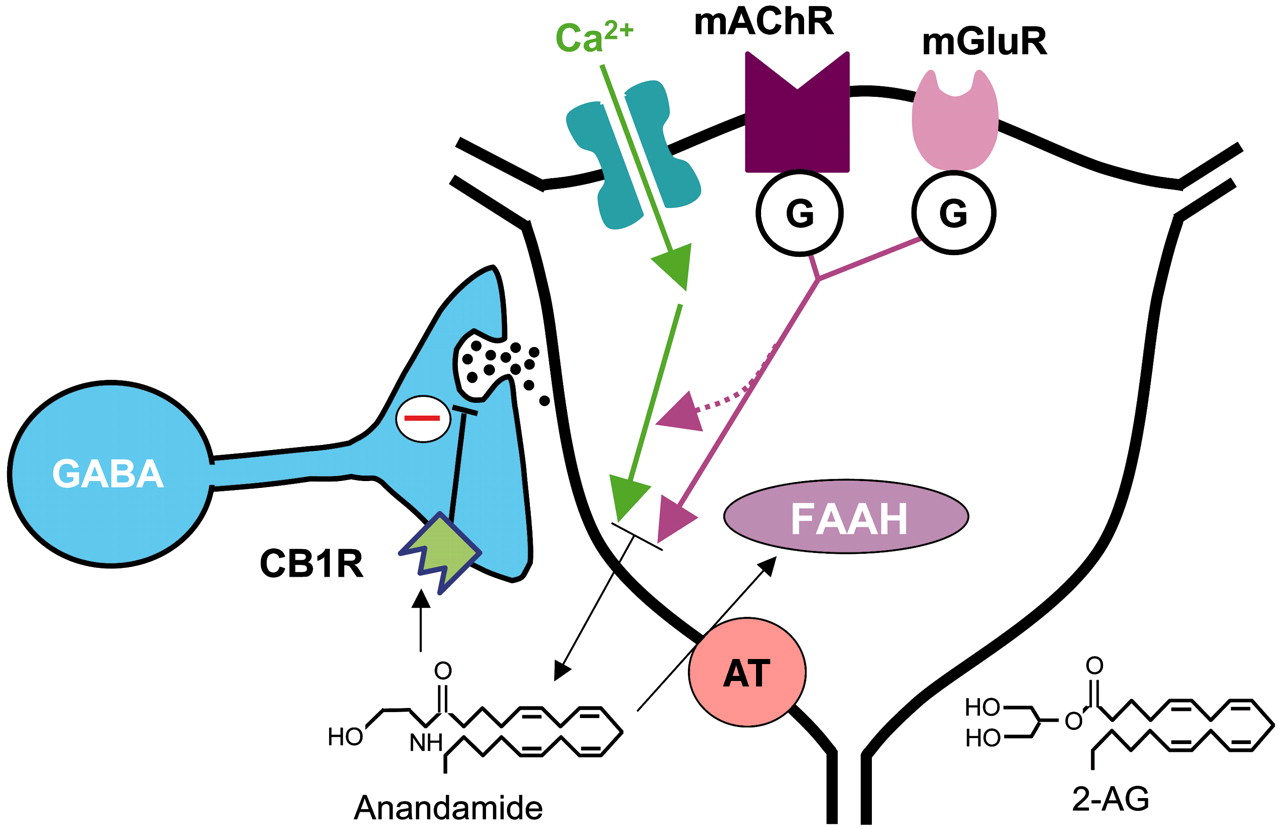
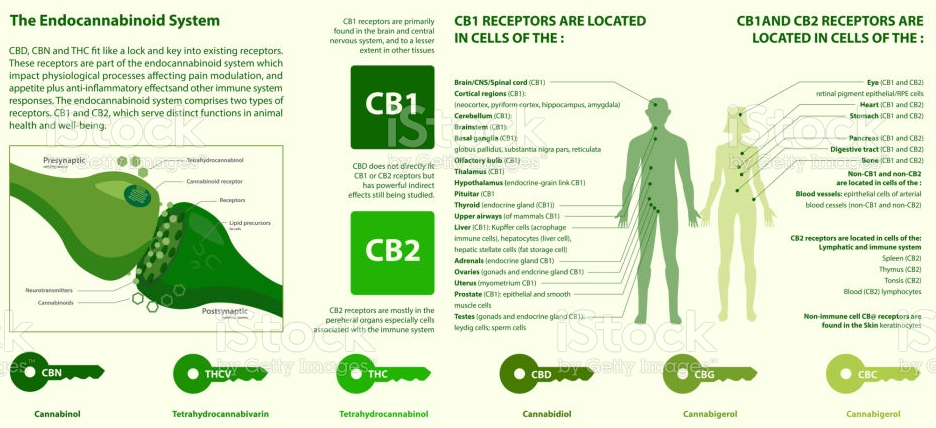
CB1- и CB2-рецепторы на 44 % идентичны по аминокислотной последовательности. Оба типа рецепторов относятся к классу рецепторов с G-белковой связью. Сейчас ученым известна высокоточная кристаллическая структура каннабиноидного рецептора. Более того, в последние годы стало возможным понять, как изменяются рецепторы при взаимодействии с ТГК и другим каннабиноидом - гексагидроканнабиолом. Интересно, что с помощью фармакологических методов можно блокировать рецепторы CB1 и CB2 по отдельности, но в то же время нельзя стимулировать их по отдельности. Возникает вопрос: зачем вообще нужны рецепторы к каннабису в нашем организме? За год до описания второго типа рецепторов в журнале Science была опубликована работа, в которой рассматривалась другая часть эндоканнабиноидной системы - анандамид. Другими словами, это молекула, вырабатываемая в организме человека, которая действует на те же рецепторы, что и каннабиноиды. Помимо анандамида, к эндогенным каннабиноидам относится 2-арахидоноилглицерин. CB1-рецепторы находятся в нейронах коры головного мозга, базальных ганглиев, мозжечка и гиппокампа. Функция этих рецепторов заключается в снижении высвобождения нейротрансмиттеров - ГАМК или глутамата.
Несмотря на ограничение в применении, марихуана и выделенные из нее вещества нашли применение в медицине. Выращивание каннабиса в медицинских целях и производство лекарств из каннабиса строго регулируются государством. Маловероятно, что какие-либо научные исследования на данный момент могут рассматриваться как аргумент в пользу легализации марихуаны и ее безопасности. Когда речь заходит о каннабисе и его применении в медицине, на ум приходит другой пример "натурального" лекарства - пенициллин. Изобретение пенициллина было связано с тем, что определенный вид плесени подавлял рост бактерий в лаборатории. Нобелевский лауреат Александр Флеминг, сделавший это открытие, впоследствии планировал выделить действующее вещество, синтезировать его в промышленных масштабах и использовать в качестве лекарства. С каннабисом и каннабиноидами ситуация похожая: зачем заставлять людей курить марихуану, если можно определить действующее вещество, синтезировать или выделить его из растений и использовать для лечения болезней? Применение каннабиноидов в медицине напоминает то, как артемизинин, выделенный из однолетней полыни, начали использовать для лечения малярии. Китайский исследователь Ю Ту получил за это открытие Нобелевскую премию по физиологии и медицине в 2015 году.
В метаанализе 2013 года было установлено, что употребление ТГК и самой марихуаны повышало аппетит у пациентов этой группы и способствовало увеличению веса. В более ранних работах дронабинол (синтетический аналог ТГК) сравнивали по эффективности с мегестрола ацетатом в плане набора веса у пациентов с онкологической кахексией. Оказалось, что мегестрол превосходит своего конкурента в этой задаче. Другое направление применения каннабиноидов - лечение тошноты и рвоты у пациентов, проходящих химиотерапию при онкологических заболеваниях. Область мозга, отвечающая за рвотную реакцию (area postrema), богата CB1-рецепторами. Эти же рецепторы в большом количестве присутствуют в ядре солитарного тракта и ядрах блуждающего нерва, которые также вовлечены в процессы тошноты и рвоты. Стимуляция каннабиноидных рецепторов в этих нервных структурах приводит к уменьшению чувства тошноты и прекращению рвоты. Исследования показали, что каннабиноиды справляются с тошнотой и рвотой, вызванными химиотерапией, лучше, чем нейролептики, но они все равно являются худшим вариантом, чем ондансетрон. Обычно каннабиноиды не являются препаратами первой линии и используются, когда другие методы лечения неэффективны.
Интересно, что каннабиноиды потенциально могут быть противораковыми препаратами. Накоплен большой объем лабораторных данных о том, что стимуляция каннабиноидных рецепторов приводит к гибели раковых клеток. Подобные исследования проводились на раке груди, простаты, легких и поджелудочной железы. Эти виды опухолей широко распространены среди населения и дают высокий уровень смертности, а существующие методы лечения часто не дают удовлетворительного результата. Если нам удастся найти способ стимулировать каннабиноидные рецепторы раковых клеток без участия рецепторов центральной нервной системы, то в наших руках окажется хорошее лекарство для лечения рака. Помимо применения каннабиноидов в лечении рака и СПИДа, их можно использовать в терапии рассеянного склероза. Они способны справиться со спастичностью лучше, чем плацебо (но разница не очень велика). Кроме того, они весьма полезны при невропатической боли различного происхождения, что является еще одним их преимуществом.
Некоторые препараты на основе каннабиноидов .
Психоактивное действие каннабиса обусловлено каннабиноидами - группой терпенфенольных соединений растительного происхождения. Известны десятки каннабиноидов, но самым мощным по психоактивному воздействию является Δ9-тетрагидроканнабиол. Другие представители семейства каннабиноидов обладают ими в меньшей степени. Каннабиноиды образуются в растениях двумя путями. Поликетидный путь предполагает их синтез из оливетоловой кислоты. Второй путь более сложный: он основан на производстве геранилдифосфата с последующим синтезом монотерпенов. Интересно, зачем конопле вообще нужна эта группа веществ? Скорее всего, как и в случае с никотином, каннабиноиды являются защитным фактором от насекомых. Не совсем понятно, оказывают ли они прямое воздействие на центральную нервную систему насекомых или влияют на них каким-то другим способом, но их эффективность в этой роли не может быть оспорена.
В недавнем исследовании, проведенном Институтом молекулярной медицины в Лиссабоне совместно с учеными из британского Ланкастерского университета, было заявлено, что длительное употребление каннабиса ухудшает память. Этот вывод, как утверждается, верен как для людей, употребляющих его рекреационно, так и для тех, кто принимает каннабиносодержащие препараты для лечения некоторых форм эпилепсии, хронической боли и рассеянного склероза. Специалисты Ланкастерского университета изучили действие особого препарата под названием WIN-55,212 и обнаружили у подопытных животных серьезные нарушения памяти. В результате длительного применения препарата во время этологического эксперимента мыши не могли отличить знакомый объект от нового. Кроме того, в ходе функциональных исследований мозга животных были визуализированы определенные нарушения в некоторых областях, задействованных в памяти и обучении. Все это, собственно, и лежит в основе негативного влияния каннабиса на процесс запоминания.
Еще в 2012 году исследователи под руководством Абуша доказали, что длительное употребление каннабиса статистически значимо связано с когнитивной дисфункцией и повышенным риском развития симптомов психических расстройств, включая спектр шизофренических расстройств. На животных моделях было выявлено, что негативное влияние каннабиноидов на обучение и память связано с дисфункцией долговременного потенцирования синаптической передачи. Также с уменьшением модификации нейронных колебаний, моделируемых габаергическими интернейронами, и с изменением активности в моноаминергических и холинергических путях гиппокампа, играющих важную роль в пластичности и других важных процессах.
Ученые уже давно пытались найти цель действия каннабиноидов. Это было сделано в 1988 году, когда был описан первый тип каннабиноидных рецепторов (CB1-рецепторы). В 1993 году был открыт и второй тип рецепторов (CB2-рецепторы). CB1-рецепторы расположены в центральной нервной системе. Активация и блокировка CB1 влияет на процессы памяти, нейропротекции, ноцицепции. Помимо мозга, их можно обнаружить в печени, миокарде, почках, желудочно-кишечном тракте, легких, а также в эндотелиальной выстилке и мышечной стенке кровеносных сосудов. CB2 широко представлен в иммунных и эндотелиальных клетках. Синтетические каннабиноиды, входящие в состав курительных смесей, в основном стимулируют CB1-рецепторы, поэтому эти вещества изменяют психическое состояние человека.
CB1- и CB2-рецепторы на 44 % идентичны по аминокислотной последовательности. Оба типа рецепторов относятся к классу рецепторов с G-белковой связью. Сейчас ученым известна высокоточная кристаллическая структура каннабиноидного рецептора. Более того, в последние годы стало возможным понять, как изменяются рецепторы при взаимодействии с ТГК и другим каннабиноидом - гексагидроканнабиолом. Интересно, что с помощью фармакологических методов можно блокировать рецепторы CB1 и CB2 по отдельности, но в то же время нельзя стимулировать их по отдельности. Возникает вопрос: зачем вообще нужны рецепторы к каннабису в нашем организме? За год до описания второго типа рецепторов в журнале Science была опубликована работа, в которой рассматривалась другая часть эндоканнабиноидной системы - анандамид. Другими словами, это молекула, вырабатываемая в организме человека, которая действует на те же рецепторы, что и каннабиноиды. Помимо анандамида, к эндогенным каннабиноидам относится 2-арахидоноилглицерин. CB1-рецепторы находятся в нейронах коры головного мозга, базальных ганглиев, мозжечка и гиппокампа. Функция этих рецепторов заключается в снижении высвобождения нейротрансмиттеров - ГАМК или глутамата.
Несмотря на ограничение в применении, марихуана и выделенные из нее вещества нашли применение в медицине. Выращивание каннабиса в медицинских целях и производство лекарств из каннабиса строго регулируются государством. Маловероятно, что какие-либо научные исследования на данный момент могут рассматриваться как аргумент в пользу легализации марихуаны и ее безопасности. Когда речь заходит о каннабисе и его применении в медицине, на ум приходит другой пример "натурального" лекарства - пенициллин. Изобретение пенициллина было связано с тем, что определенный вид плесени подавлял рост бактерий в лаборатории. Нобелевский лауреат Александр Флеминг, сделавший это открытие, впоследствии планировал выделить действующее вещество, синтезировать его в промышленных масштабах и использовать в качестве лекарства. С каннабисом и каннабиноидами ситуация похожая: зачем заставлять людей курить марихуану, если можно определить действующее вещество, синтезировать или выделить его из растений и использовать для лечения болезней? Применение каннабиноидов в медицине напоминает то, как артемизинин, выделенный из однолетней полыни, начали использовать для лечения малярии. Китайский исследователь Ю Ту получил за это открытие Нобелевскую премию по физиологии и медицине в 2015 году.
В метаанализе 2013 года было установлено, что употребление ТГК и самой марихуаны повышало аппетит у пациентов этой группы и способствовало увеличению веса. В более ранних работах дронабинол (синтетический аналог ТГК) сравнивали по эффективности с мегестрола ацетатом в плане набора веса у пациентов с онкологической кахексией. Оказалось, что мегестрол превосходит своего конкурента в этой задаче. Другое направление применения каннабиноидов - лечение тошноты и рвоты у пациентов, проходящих химиотерапию при онкологических заболеваниях. Область мозга, отвечающая за рвотную реакцию (area postrema), богата CB1-рецепторами. Эти же рецепторы в большом количестве присутствуют в ядре солитарного тракта и ядрах блуждающего нерва, которые также вовлечены в процессы тошноты и рвоты. Стимуляция каннабиноидных рецепторов в этих нервных структурах приводит к уменьшению чувства тошноты и прекращению рвоты. Исследования показали, что каннабиноиды справляются с тошнотой и рвотой, вызванными химиотерапией, лучше, чем нейролептики, но они все равно являются худшим вариантом, чем ондансетрон. Обычно каннабиноиды не являются препаратами первой линии и используются, когда другие методы лечения неэффективны.
Интересно, что каннабиноиды потенциально могут быть противораковыми препаратами. Накоплен большой объем лабораторных данных о том, что стимуляция каннабиноидных рецепторов приводит к гибели раковых клеток. Подобные исследования проводились на раке груди, простаты, легких и поджелудочной железы. Эти виды опухолей широко распространены среди населения и дают высокий уровень смертности, а существующие методы лечения часто не дают удовлетворительного результата. Если нам удастся найти способ стимулировать каннабиноидные рецепторы раковых клеток без участия рецепторов центральной нервной системы, то в наших руках окажется хорошее лекарство для лечения рака. Помимо применения каннабиноидов в лечении рака и СПИДа, их можно использовать в терапии рассеянного склероза. Они способны справиться со спастичностью лучше, чем плацебо (но разница не очень велика). Кроме того, они весьма полезны при невропатической боли различного происхождения, что является еще одним их преимуществом.
Некоторые препараты на основе каннабиноидов .
- Набиксимол - спрей, содержащий смесь 2 каннабиноидов: ТГК и каннабидиола. Используется для лечения спастичности и боли как симптома рассеянного склероза. Также используется для лечения болевого синдрома при онкологических заболеваниях.
- Дронабинол - синтетический ТГК, который обладает противорвотным действием и повышает аппетит. Применяется для лечения истощенных больных СПИДом и пациентов с тошнотой и рвотой во время химиотерапии.
- Набилон - лекарство, в основе которого лежит каннабиноид, структурно схожий с ТГК. Он используется для лечения рвоты и тошноты, вызванных химиотерапией.
При исследовании мозга людей, употреблявших каннабис в течение длительного времени (более года ежедневно или не менее 3 раз в неделю) методом функциональной магнитно-резонансной томографии, были показаны значительные изменения функциональных связей структур мозга, связанных с "самосознанием" и некоторыми видами памяти, а также функциональные изменения в структурах медиальной височной доли и префронтальной коры. Факультет биомедицинских и биологических наук Ланкастерского университета проделал большую работу по изучению влияния хронического употребления каннабиса на некоторые метаболические процессы мозга, его функциональные связи и память на распознавание. Результаты эксперимента продемонстрировали нарушение метаболизма головного мозга и аномальные функциональные связи с кортико-таламо-гиппокампальными цепями, лежащими в основе процессов запоминания.
При этом был выявлен дефицит памяти на узнавание без признаков изменения двигательных способностей и тревожного поведения. Именно CB1-r в синапсах ингибирует глутаматергическую и ГАМК-ергическую передачу с моделированием различных форм синаптической пластичности и нейронных осцилляций, поддерживающих различные когнитивные функции, включая поведение и память. Также были нарушены функциональные связи субикулума (основания гиппокампа). Он является частью памяти распознавания и получает прямые аксонные связи от других частей мозга, отвечающих за долговременную память. Изменения в работе серотониновой системы подтверждаются изменением функциональных связей части мозга, называемой хабенулой, ядрами рафы с изменением индукции уровня серотонина в синапсах и плотности серотониновых рецепторов. Все это приводит к развитию дефицита функции памяти. Интересным фактом является то, что при использовании антагониста CB1r (AM-251) негативное влияние каннабиноидов на память нивелируется, а при высоких дозах каннабиса и AM-251 не наблюдается выраженного снижения поглощения глюкозы и митохондриального дыхания.
При этом был выявлен дефицит памяти на узнавание без признаков изменения двигательных способностей и тревожного поведения. Именно CB1-r в синапсах ингибирует глутаматергическую и ГАМК-ергическую передачу с моделированием различных форм синаптической пластичности и нейронных осцилляций, поддерживающих различные когнитивные функции, включая поведение и память. Также были нарушены функциональные связи субикулума (основания гиппокампа). Он является частью памяти распознавания и получает прямые аксонные связи от других частей мозга, отвечающих за долговременную память. Изменения в работе серотониновой системы подтверждаются изменением функциональных связей части мозга, называемой хабенулой, ядрами рафы с изменением индукции уровня серотонина в синапсах и плотности серотониновых рецепторов. Все это приводит к развитию дефицита функции памяти. Интересным фактом является то, что при использовании антагониста CB1r (AM-251) негативное влияние каннабиноидов на память нивелируется, а при высоких дозах каннабиса и AM-251 не наблюдается выраженного снижения поглощения глюкозы и митохондриального дыхания.
Таким образом, было предложено определить стратегию лечения для восстановления явных нарушений памяти, коррекции когнитивных расстройств у людей, длительно употребляющих каннабис. Рекомендуется следующий алгоритм терапевтической коррекции когнитивных нарушений:
- Физические нагрузки умеренной интенсивности, интеллектуальные упражнения и смена "привычной среды": ежедневное плавание, лечебная физкультура, настольные игры (шахматы и др.), смена рук при чистке зубов, чтение вслух, изучение иностранных языков, соблюдение цикла сон-бодрствование.
- "Наменда" - 5 мг в день во время еды в течение двух недель, затем 5 мг раз в три дня в течение полутора месяцев.
- "Тебокан" (EGb 761) - по одной таблетке раз в день в течение месяца (NB! Не имеет доказанной эффективности).
- "Мельдоний Олайнфарм" - одна таблетка (250 мг) утром, во время еды, в течение 1,5 месяцев.
- Мультивитамины - курсом.
- "Ацетил-L-карнитин" - по 500 мг два раза в день в течение 1,5 месяцев.
- "Ницербиум" или "Сермион" - курс 14 дней.
Last edited by a moderator:
