- Joined
- Dec 27, 2022
- Messages
- 30
- Reaction score
- 81
- Points
- 18
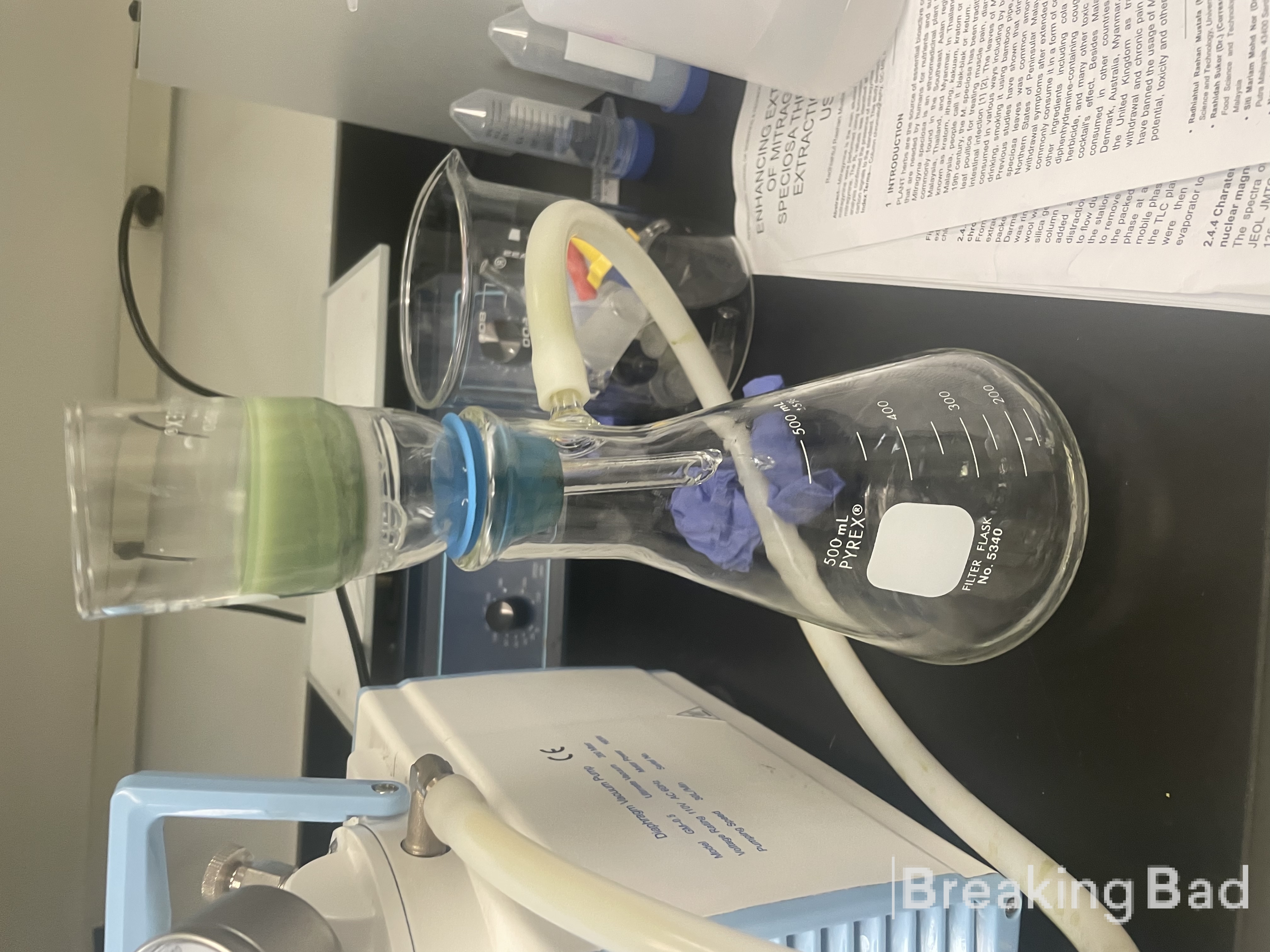
Добре, момчета! Време е да споделя с вас малко знания. Ще опиша синтеза, който направих за псилоцин, придружен със снимки. Използвах получения псилоцин и разработих проста лепенка за залепване. За да тестваме проникването на псилоцина в лепенката, използвахме дифузионен апарат, който сглобих. Той включва няколко мембрани, като лепенка с размер 1 cm^2 се поставя върху парче прясна човешка кожа с размер 1 cm^2 и дебелина 400 um (дарена от хирургически център за коремни операции). Под кожата има постоянен поток от вода с рН 7,4 и телесна температура. Дифузионният апарат може да събира фракция от 1 ml на час, която след това се анализира чрез LC-MS. Количеството на псилоцин във флакона от 1 ml ще даде потока (mg/час/cm^2). Това определя колко псилоцин преминава за час при размер на лепенката cm^2.
Това се задълбочава, тъй като псилоцинът е силно нестабилен. в следващата публикация, Structure Elucidation and Spectroscopic Analysis of Chromophores Produced by Oxidative Psilocin Dimerization (Изясняване на структурата и спектроскопски анализ на хромофори, получени при оксидативна димеризация на псилоцин), се разглежда този въпрос. Когато се образува димер, той е неоткриваем чрез HPLC анализ и ATR-FTIR, което е странно. Това дава на изследователските групи фалшиви положителни резултати за чистотата на псилоцина. Намерих начин да стабилизирам псилоцина в пластира.
Както и да е, нека започнем! Направих всяка стъпка сам, с помощта на партньора ми, който е инженер-химик. Това беше по времето, когато имах лиценз на DEA по списък1 и 3 не само за изследвания, но и за производство.
Част I (Синтез на псилоцин)
стъпка 1: синтез на 3-[2-(диметиламино)-2-оксоацетил]-1H-индол-4-ил ацетат
1a. Колба с кръгло дъно с обем 2000 ml и четири гърла е оборудвана с горна бъркалка, температурен регулатор J-Kem, капкова фуния с обем 250 ml и гумена преграда, през която се вкарва сухN2 под положително налягане. Преградата се отстранява и колбата се зарежда равномерно с 1Н-индол-4-ил ацетат (5; 50,1 g, 285 mmol, 1 еквивалент)
и безводен Et2O (700 ml). Колбата се затваря отново с преградата и се промива с N2. Суспензията се разбърква в продължение на 10 min и след това
се охлажда до 0 °С на водна баня с лед в продължение на 30 min.

1b. Капковата фуния се зарежда с разтвор на оксалилхлорид (37,1 ml, 428 mmol, 1,5 еквивалента) в Et2O (60 mL). Разтворът на оксалилхлорид се прибавя по капки със скорост, достатъчна за поддържане на температурата на или под 5 °C, за да се сведе до минимум образуването на димер и други възможни странични продукти. С напредването на добавянето се образува жълта суспензия от 10 и когато добавянето приключи, сместа се разбърква в продължение на 4 часа.

1c. След това е добавен хептан (400 ml) и сместа е разбърквана в продължение на 30 min при 0 °C. Полученото жълто твърдо вещество бързо се филтрира и се изплаква последователно с хептан (2 × 300 ml), който бързо се използва в следващата стъпка. . Добавя се 2,0 М разтвор на диметиламин в THF (175 mL) по капки със скорост, достатъчна за поддържане на температура под 5 °C, за да се сведат до минимум страничните реакции. След
пиридин (46 ml) в THF (100 ml) и сместа се разбърква добре в продължение на 60 min. Добавя се хептан (600 mL) и съдържанието на колбата се филтрира чрез засмукване през фуния на Бюхнер. Филтрираният остатък е прехвърлен в кръглодънна колба и е добавена дейонизирана H2O (1000 ml), разбърква се в продължение на 30 min и се филтрира през Büchner фуния. Белезникавото твърдо вещество се тритира последователно в продължение на 40 min в EtOAc (600 mL) и хептан (400 mL). Суспензията се филтрира през фуния на Бюхнер и твърдото вещество се изсушава във фурна при 40 °C за една нощ, за да се получи 6 като светложълто твърдо вещество; добив: 66,1 g (81 %); mp 205-207 °C.



ATR-FTIR потвърди синтеза на синтеза на 3-[2-(диметиламино)-2-оксоацетил]-1H-индол-4-ил ацетат. Това съединение може да се съхранява при 4С в продължение на няколко месеца!
Стъпка 2: Синтез на псилоцин
Стъпка 2А: Колба с кръгло дъно с обем 2000 ml и четири гърла е оборудвана с горна бъркалка, температурен регулатор J-Kem
250 mL капеща фуния и гумена преграда, през която се вкарва сух N2 под положително налягане. Преградата се отстранява и
колбата се зарежда последователно с 3-[2-(диметиламино)-2-оксоацетил]-1H-индол-4-ил ацетат (6; 31,5 g, 115 mmol) и 2-CH3-THF (1000
ml). Колбата е потопена в ледена баня при 0 °C и е добавен разтвор на 2,3 M LiAlH4 в 2-CH3-THF (140 ml, 322 mmol) през
250 ml капковата фуния. Капковата фуния е изплакната допълнително с 2-CH3-THF (20 mL). Разтворът на LiAlH4 е добавен на капки
със скорост, която да поддържа температура под 20 °C. След добавянето ледено-водната баня се отстранява и сместа се разбърква в продължение на 30 min.
Светложълтият разтвор се нагрява до рефлукс (80 °C) с помощта на нагревателна мантия и става с цвят на слонова кост след 3 h. Натрупването на
жълто твърдо вещество по стените на кръглодънната колба



Стъпка 2В. Нагревателната мантия се отстранява и колбата се оставя да се охлади до 50 °C. Колбата отново се
охлажда до 20 °C. Реакцията се потушава чрез последователно добавяне на 3 капки от 1 M NaOH и 3 капки от дейонизирана H2O. Сместа
се разрежда с THF (500 ml) и се разбърква в продължение на 20 min. Сместа се филтрира през фуния на Бюхнер и филтратът се съхранява под N2.
Филтърният кек бързо се разбърква отново с 200 mL [10% разтвор на (7% амоняк в MeOH) в CH2Cl2] и THF (500 mL). Филтратите
след това се комбинират и концентрират, за да се получи зелено твърдо вещество. Твърдото вещество се тритурира с 1:1 EtOAc/хептан (50 mL), след което се филтрира през
Büchner. Тъмнозеленото твърдо вещество се изсушава в сушилня при 40 °C за една нощ, за да се получи сух псилоцин (7) като тъмнозелено твърдо вещество; добив: 20,7
(91 %); mp 167-169 °C.


Синтезиран е псилоцин.
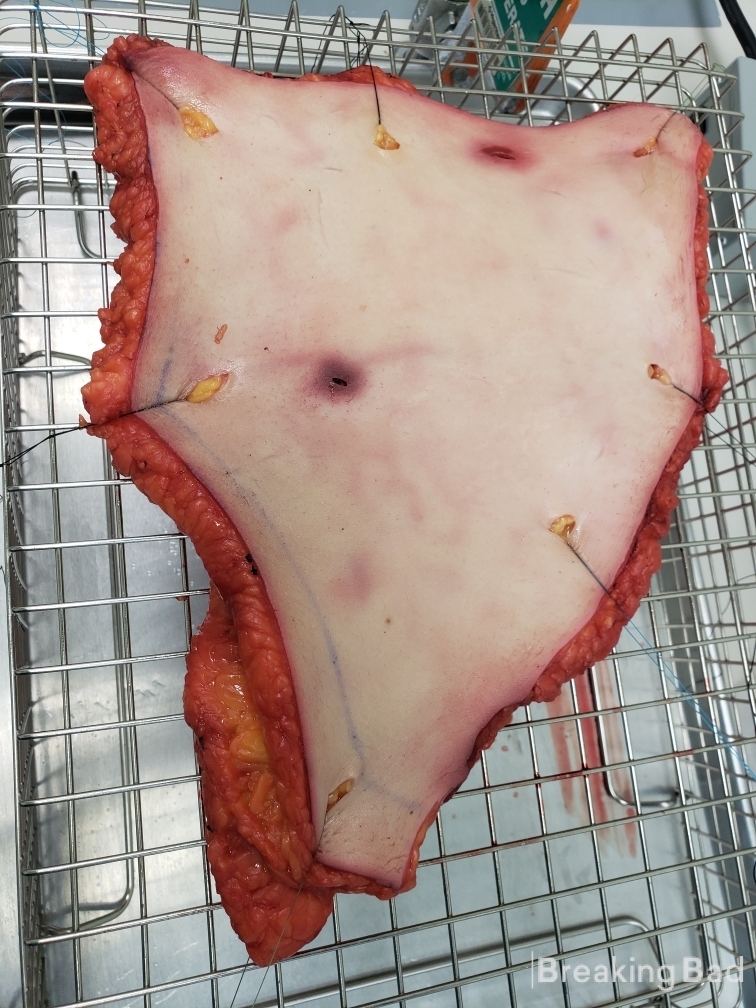
Част II: Разработване на трансдермален пластир с псилоцин и ин-витро проучване (ВНИМАНИЕ: ЩЕ ВИДИТЕ ЧУЖДА ЧОВЕШКА КОЖА, НЕЙНАТА ГРУБОСТ
След това разтварям псилоцина в патентована смес от акрилатен полимер (в хептан), след което изливам разтвора в разделителна линия и използвам леярски нож, за да достигна лепилния слой до 100 um. След като изсъхне, нанасям подложния слой и изрязвам пластир с размер 1 cm^2. Този пластир се използва за ин витро изследването.
Следващата снимка е снимка на апарата за дифузия (пластир върху кожата с течаща отдолу вода).

Надявам се, че ви е харесало!
Това се задълбочава, тъй като псилоцинът е силно нестабилен. в следващата публикация, Structure Elucidation and Spectroscopic Analysis of Chromophores Produced by Oxidative Psilocin Dimerization (Изясняване на структурата и спектроскопски анализ на хромофори, получени при оксидативна димеризация на псилоцин), се разглежда този въпрос. Когато се образува димер, той е неоткриваем чрез HPLC анализ и ATR-FTIR, което е странно. Това дава на изследователските групи фалшиви положителни резултати за чистотата на псилоцина. Намерих начин да стабилизирам псилоцина в пластира.
Както и да е, нека започнем! Направих всяка стъпка сам, с помощта на партньора ми, който е инженер-химик. Това беше по времето, когато имах лиценз на DEA по списък1 и 3 не само за изследвания, но и за производство.
Част I (Синтез на псилоцин)
стъпка 1: синтез на 3-[2-(диметиламино)-2-оксоацетил]-1H-индол-4-ил ацетат
1a. Колба с кръгло дъно с обем 2000 ml и четири гърла е оборудвана с горна бъркалка, температурен регулатор J-Kem, капкова фуния с обем 250 ml и гумена преграда, през която се вкарва сухN2 под положително налягане. Преградата се отстранява и колбата се зарежда равномерно с 1Н-индол-4-ил ацетат (5; 50,1 g, 285 mmol, 1 еквивалент)
и безводен Et2O (700 ml). Колбата се затваря отново с преградата и се промива с N2. Суспензията се разбърква в продължение на 10 min и след това
се охлажда до 0 °С на водна баня с лед в продължение на 30 min.
1b. Капковата фуния се зарежда с разтвор на оксалилхлорид (37,1 ml, 428 mmol, 1,5 еквивалента) в Et2O (60 mL). Разтворът на оксалилхлорид се прибавя по капки със скорост, достатъчна за поддържане на температурата на или под 5 °C, за да се сведе до минимум образуването на димер и други възможни странични продукти. С напредването на добавянето се образува жълта суспензия от 10 и когато добавянето приключи, сместа се разбърква в продължение на 4 часа.
1c. След това е добавен хептан (400 ml) и сместа е разбърквана в продължение на 30 min при 0 °C. Полученото жълто твърдо вещество бързо се филтрира и се изплаква последователно с хептан (2 × 300 ml), който бързо се използва в следващата стъпка. . Добавя се 2,0 М разтвор на диметиламин в THF (175 mL) по капки със скорост, достатъчна за поддържане на температура под 5 °C, за да се сведат до минимум страничните реакции. След
пиридин (46 ml) в THF (100 ml) и сместа се разбърква добре в продължение на 60 min. Добавя се хептан (600 mL) и съдържанието на колбата се филтрира чрез засмукване през фуния на Бюхнер. Филтрираният остатък е прехвърлен в кръглодънна колба и е добавена дейонизирана H2O (1000 ml), разбърква се в продължение на 30 min и се филтрира през Büchner фуния. Белезникавото твърдо вещество се тритира последователно в продължение на 40 min в EtOAc (600 mL) и хептан (400 mL). Суспензията се филтрира през фуния на Бюхнер и твърдото вещество се изсушава във фурна при 40 °C за една нощ, за да се получи 6 като светложълто твърдо вещество; добив: 66,1 g (81 %); mp 205-207 °C.
ATR-FTIR потвърди синтеза на синтеза на 3-[2-(диметиламино)-2-оксоацетил]-1H-индол-4-ил ацетат. Това съединение може да се съхранява при 4С в продължение на няколко месеца!
Стъпка 2: Синтез на псилоцин
Стъпка 2А: Колба с кръгло дъно с обем 2000 ml и четири гърла е оборудвана с горна бъркалка, температурен регулатор J-Kem
250 mL капеща фуния и гумена преграда, през която се вкарва сух N2 под положително налягане. Преградата се отстранява и
колбата се зарежда последователно с 3-[2-(диметиламино)-2-оксоацетил]-1H-индол-4-ил ацетат (6; 31,5 g, 115 mmol) и 2-CH3-THF (1000
ml). Колбата е потопена в ледена баня при 0 °C и е добавен разтвор на 2,3 M LiAlH4 в 2-CH3-THF (140 ml, 322 mmol) през
250 ml капковата фуния. Капковата фуния е изплакната допълнително с 2-CH3-THF (20 mL). Разтворът на LiAlH4 е добавен на капки
със скорост, която да поддържа температура под 20 °C. След добавянето ледено-водната баня се отстранява и сместа се разбърква в продължение на 30 min.
Светложълтият разтвор се нагрява до рефлукс (80 °C) с помощта на нагревателна мантия и става с цвят на слонова кост след 3 h. Натрупването на
жълто твърдо вещество по стените на кръглодънната колба
Стъпка 2В. Нагревателната мантия се отстранява и колбата се оставя да се охлади до 50 °C. Колбата отново се
охлажда до 20 °C. Реакцията се потушава чрез последователно добавяне на 3 капки от 1 M NaOH и 3 капки от дейонизирана H2O. Сместа
се разрежда с THF (500 ml) и се разбърква в продължение на 20 min. Сместа се филтрира през фуния на Бюхнер и филтратът се съхранява под N2.
Филтърният кек бързо се разбърква отново с 200 mL [10% разтвор на (7% амоняк в MeOH) в CH2Cl2] и THF (500 mL). Филтратите
след това се комбинират и концентрират, за да се получи зелено твърдо вещество. Твърдото вещество се тритурира с 1:1 EtOAc/хептан (50 mL), след което се филтрира през
Büchner. Тъмнозеленото твърдо вещество се изсушава в сушилня при 40 °C за една нощ, за да се получи сух псилоцин (7) като тъмнозелено твърдо вещество; добив: 20,7
(91 %); mp 167-169 °C.
Синтезиран е псилоцин.
Част II: Разработване на трансдермален пластир с псилоцин и ин-витро проучване (ВНИМАНИЕ: ЩЕ ВИДИТЕ ЧУЖДА ЧОВЕШКА КОЖА, НЕЙНАТА ГРУБОСТ
След това разтварям псилоцина в патентована смес от акрилатен полимер (в хептан), след което изливам разтвора в разделителна линия и използвам леярски нож, за да достигна лепилния слой до 100 um. След като изсъхне, нанасям подложния слой и изрязвам пластир с размер 1 cm^2. Този пластир се използва за ин витро изследването.
Следващата снимка е снимка на апарата за дифузия (пластир върху кожата с течаща отдолу вода).
Надявам се, че ви е харесало!


