@G.Patton Смятам, че един от нарисуваните междинни продукти на този синтез (и от оригиналната статия за родий) е неправилен.
(3), изображението на междинния продукт амфетамин-формалдехид имин притежава същата структура като фенилацетон-метиламиновия имин, който може да се види на друго място
това не ми се струва правилно по две причини: първо, при начертаването на стандартния механизъм за образуване на имин върху субстрата се получава имин, при който двойната връзка е между N и бъдещата метилова група на метамфетамина, а НЕ между N и алфа-въглерода, както е в посочената структура. и помислете: двойната връзка се получава, когато самотната двойка на амина отхвърли водата, образувана върху кислорода на формалдехида като напускаща група, което трябва да се извърши от страната на формалдехида (бъдещата метилова група)
Второ, синтезът е отчетен като стереоспецифичен въз основа на изходния субстрат. т.е. редукцията на d-amph ще даде d-meth и същото за l-изомера. структурата, както е показана (3), не притежава хирални центрове и редукцията ѝ е еквивалентна на стандартното редукционно аминиране на фенилацетон, при което се получава рацемичен продукт. предложената от мен структура на междинния продукт притежава хирален център, който би бил същият като този на изходния материал и следователно съответства на наблюдаваната стереоспецифичност на реакцията.
Ако съм прав, това би изяснило въпросите относно стереоспецифичността на реакцията по-рано в темата. ако някъде съм допуснал грешка, се извинявам, но ми беше интересно защо редукцията на нехиралния (3) води до нерасемична смес от продукти, когато се използва нерасемичен изходен материал амфетамин.
(3), изображението на междинния продукт амфетамин-формалдехид имин притежава същата структура като фенилацетон-метиламиновия имин, който може да се види на друго място
това не ми се струва правилно по две причини: първо, при начертаването на стандартния механизъм за образуване на имин върху субстрата се получава имин, при който двойната връзка е между N и бъдещата метилова група на метамфетамина, а НЕ между N и алфа-въглерода, както е в посочената структура. и помислете: двойната връзка се получава, когато самотната двойка на амина отхвърли водата, образувана върху кислорода на формалдехида като напускаща група, което трябва да се извърши от страната на формалдехида (бъдещата метилова група)
Второ, синтезът е отчетен като стереоспецифичен въз основа на изходния субстрат. т.е. редукцията на d-amph ще даде d-meth и същото за l-изомера. структурата, както е показана (3), не притежава хирални центрове и редукцията ѝ е еквивалентна на стандартното редукционно аминиране на фенилацетон, при което се получава рацемичен продукт. предложената от мен структура на междинния продукт притежава хирален център, който би бил същият като този на изходния материал и следователно съответства на наблюдаваната стереоспецифичност на реакцията.
Ако съм прав, това би изяснило въпросите относно стереоспецифичността на реакцията по-рано в темата. ако някъде съм допуснал грешка, се извинявам, но ми беше интересно защо редукцията на нехиралния (3) води до нерасемична смес от продукти, когато се използва нерасемичен изходен материал амфетамин.
G.Patton
Expert
- Joined
- Jul 5, 2021
- Messages
- 3,320
- Solutions
- 3
- Reaction score
- 3,799
- Points
- 113
- Deals
- 1
Здравейте. първо, а-въглеродът има по-голяма електронна плътност от метиловия въглерод. Типичният механизъм води до такъв междинен продукт (скрит под водния знак на Breaking Bad, sry):
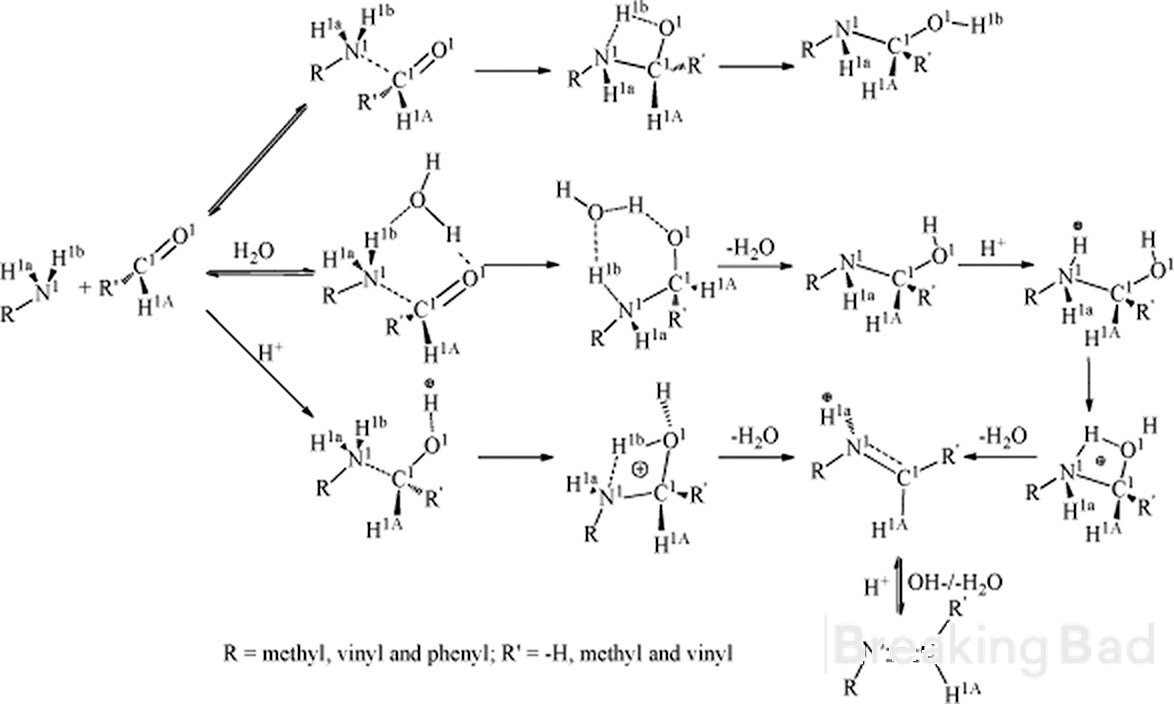
Второ, разполагате ли с надеждни данни за стереоспецифичния резултат от този синтез?
Второ, разполагате ли с надеждни данни за стереоспецифичния резултат от този синтез?
↑View previous replies…
- Language
- 🇷🇺
- Joined
- Apr 2, 2024
- Messages
- 3
- Reaction score
- 0
- Points
- 1
