- Joined
- Dec 27, 2022
- Messages
- 30
- Reaction score
- 81
- Points
- 18
Muy bien, chicos. Es hora de compartir algunos conocimientos con vosotros. Voy a describir una síntesis que hice de la psilocina, completa con fotos. Utilicé la psilocina producida y desarrollé un simple parche adhesivo. Con el fin de probar la permeabilidad de la psilocina en el parche, se utilizó un aparato de difusión que armé. Se trata de varias membranas, con un parche de 1 cm^2 colocado encima de un trozo de 1 cm^2 de piel humana fresca de 400 um de grosor (donada por un centro quirúrgico de abdominoplastia). Debajo de la piel, hay un flujo constante de agua con un pH de 7,4 y a temperatura corporal. El aparato de difusión es capaz de recoger una fracción de 1mL por hora, que luego se analiza mediante LC-MS. La cantidad de psilocina en el vial de 1mL dará el flujo (mg/hr/cm^2). Esto dicta cuánta psilocina pasa por hora con un tamaño de parche de cm^2.
En la siguiente publicación, Structure Elucidation and Spectroscopic Analysis of Chromophores Produced by Oxidative Psilocin Dimerization, se trata el tema. Cuando se forma el dímero, es indetectable mediante análisis HPLC y ATR-FTIR, lo cual es extraño. Esto da a los grupos de investigación falsos positivos en cuanto a la pureza de la psilocina. He encontrado una manera de estabilizar la psilocina en el parche.
De todos modos, ¡comencemos! Hice cada paso yo mismo, con la ayuda de mi compañero que es ingeniero químico. Esto fue cuando tenía una licencia de la DEA schedule1 y 3 no sólo para la investigación, sino también para la fabricación.
Parte I (Síntesis de Psilocina)
paso 1: síntesis de 3-[2-(Dimetilamino)-2-oxoacetíl]-1H-indol-4-il Acetato
1a. Se equipó un matraz de 2000 mL, de cuatro cuellos y fondo redondo, con un agitador superior, un controlador de temperatura J-Kem, un embudo cuentagotas de 250 mL y un septo de goma a través del cual se introdujo una presión positiva de N2 seco. Se retiró el septo y el matraz se cargó equitativamente con acetato de 1H-indol-4-ilo (5; 50,1 g, 285 mmol, 1 equiv)
y Et2O anhidro (700 mL). El matraz se volvió a cerrar con el septo y se enjuaga con N2. La suspensión se agitó durante 10 min y después se
se enfrió a 0 °C en un baño de agua helada durante 30 min.

1b. Se cargó el embudo de goteo con una disolución de cloruro de oxalilo (37,1 mL, 428 mmol, 1,5 equiv) en Et2O (60 mL). La disolución de cloruro de oxalilo se añadió gota a gota a una velocidad suficiente para mantener la temperatura a 5 °C o menos, para minimizar la formación de dímeros y otros posibles subproductos. A medida que avanzaba la adición, se formó una suspensión amarilla de 10 y cuando se completó la adición, la mezcla se agitó durante 4 h.

1c. Transcurrido este tiempo, se añadió heptano (400 mL) y la mezcla se agitó durante 30 min a 0 °C. El sólido amarillo obtenido se filtró rápidamente y se lavó sucesivamente con heptano (2 × 300 mL), que se utilizó rápidamente en el paso siguiente. . Se añadió gota a gota una disolución 2,0 M de dimetilamina en THF (175 mL) a una velocidad suficiente para mantener la temperatura por debajo de 5 °C con el fin de minimizar las reacciones secundarias. Una vez completada la
Una vez completada la adición, se añadió gota a gota piridina (46 mL) en THF (100 mL) y la mezcla se agitó bien durante 60 min. Se añadió heptano (600 mL) y el contenido del matraz se filtró por succión con un embudo Büchner. El residuo filtrado se transfirió a un matraz de fondo redondo y se añadió H2O desionizada (1000 mL), se agitó durante 30 min y se filtró con un embudo Büchner. El sólido blanquecino se trituró secuencialmente durante 40 min en EtOAc (600 mL) y heptano (400mL). La suspensión se filtró a través de un embudo Büchner y el sólido se secó en un horno a 40 °C durante la noche para obtener 6 como un sólido amarillo claro; rendimiento: 66,1 g (81%); mp 205-207 °C.



ATR-FTIR confirmó la síntesis del 3-[2-(Dimetilamino)-2-oxoacetíl]-1H-indol-4-il Acetato. Este compuesto puede almacenarse a 4C durante varios meses.
Paso 2: Síntesis de Psilocina
Paso 2A: Se equipó un matraz de 2000 mL, de cuatro cuellos y fondo redondo, con un agitador de hélice, un controlador de temperatura J-Kem, un embudo cuentagotas de 250 mL, y un agitador de hélice.
250 mL y un septo de goma a través del cual se introdujo una presión positiva de N2 seco. Se retiró el septo y el matraz se cargó
matraz se cargó secuencialmente con acetato de 3-[2-(dimetilamino)-2-oxoacetil]-1H-indol-4-ilo (6; 31,5 g, 115 mmol) y 2-CH3-THF (1000
mL). El matraz se sumergió en un baño de hielo a 0 °C y se añadió una disolución de LiAlH4 2,3 M en 2-CH3-THF (140 mL, 322 mmol) a través de un embudo cuentagotas de 250 mL.
el embudo cuentagotas de 250 mL. El embudo cuentagotas se enjuagó con 2-CH3-THF adicional (20 mL). La disolución de LiAlH4 se añadió gota a gota
a un ritmo para mantener la temperatura por debajo de 20 °C. Tras la adición, se retiró el baño de agua helada y la mezcla se agitó durante 30 min.
La solución de color amarillo claro se calentó a reflujo (80 °C) con un manto calefactor y adquirió color marfil al cabo de 3 h. Se observó acumulación de sólidos amarillos en las paredes.
de sólidos amarillos en las paredes del matraz de fondo redondo.



Paso 2C. Se retiró el manto calefactor y se dejó enfriar el matraz hasta 50 °C. El matraz se volvió a
a 20 °C. La reacción se apagó mediante la adición secuencial de 3 gotas de NaOH 1 M acuoso y 3 gotas de H2O desionizado. La mezcla
se diluyó con THF (500 mL) y se agitó durante 20 min. La mezcla se filtró con un embudo Büchner y el filtrado se mantuvo bajo N2.
La torta filtrada se volvió a filtrar rápidamente con 200 mL de [solución al 10% de (7% de amoniaco en MeOH) en CH2Cl2] y THF (500 mL). Los filtrados
se combinaron y concentraron para dar un sólido verde. El sólido se trituró con 1:1 EtOAc/heptano (50 mL), después se filtró por
embudo Büchner. El sólido verde oscuro se secó en un horno a 40 °C durante la noche para dar psilocina seca (7) como sólido verde oscuro; rendimiento: 20,7
g (91%); mp 167-169 °C.
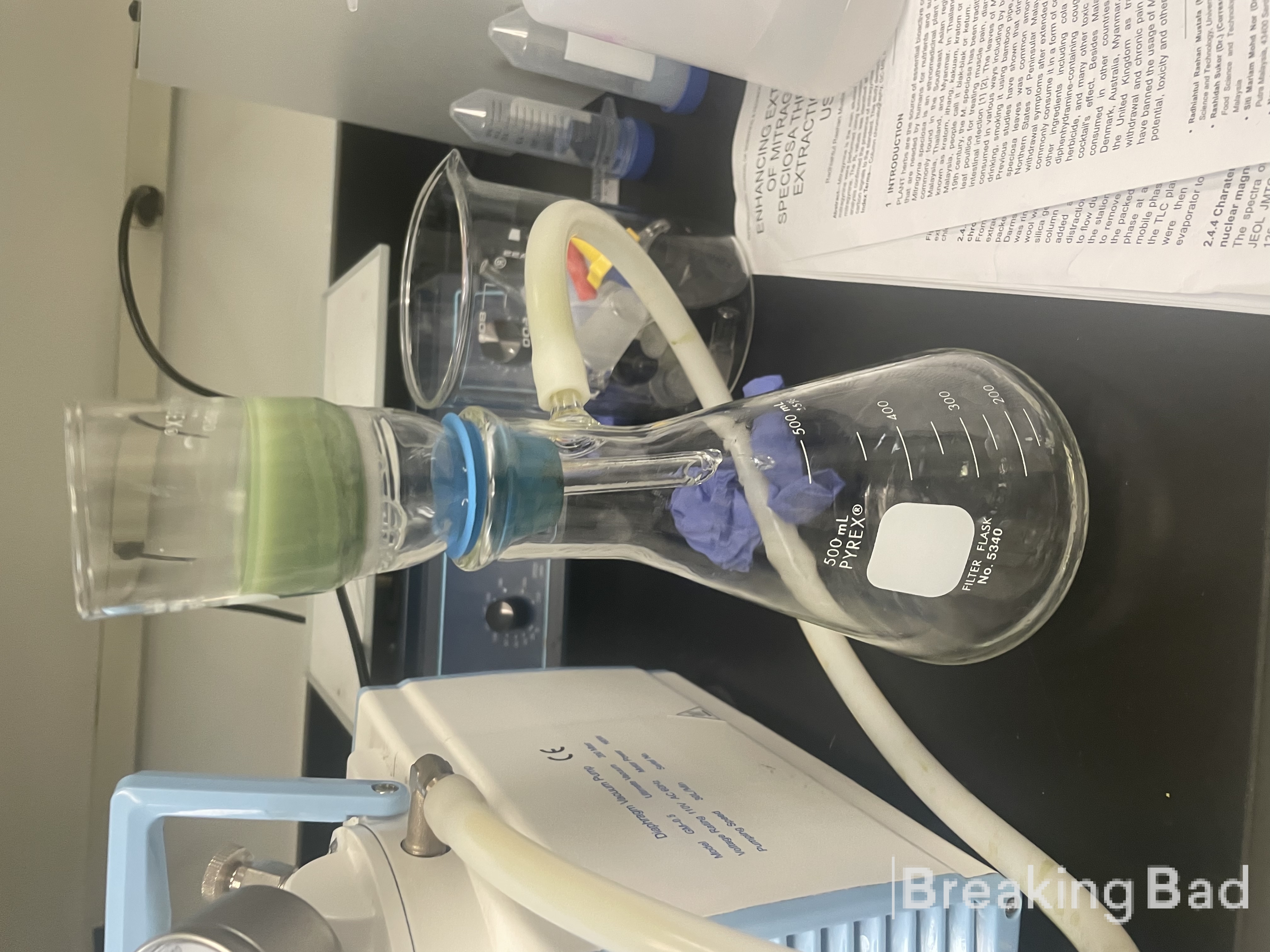


Se ha sintetizado la psilocina.
Parte II: Desarrollo del parche transdérmico de psilocina y estudio in vitro (ATENCIÓN: VERÁ CARNE HUMANA FRESCA, ES GRUESO)
A continuación, disuelvo la psilocina en una mezcla patentada de polímero de acrilato (en heptano), vierto la solución en una línea de liberación y utilizo una cuchilla de vaciado para obtener una capa adhesiva de 100 um. Una vez seca, aplico la capa de soporte y troquelo un parche de 1cm^2. Este parche se utiliza para el estudio in vitro.
La siguiente foto es una instantánea del aparato de difusión (parche encima de la piel con agua corriendo por debajo)

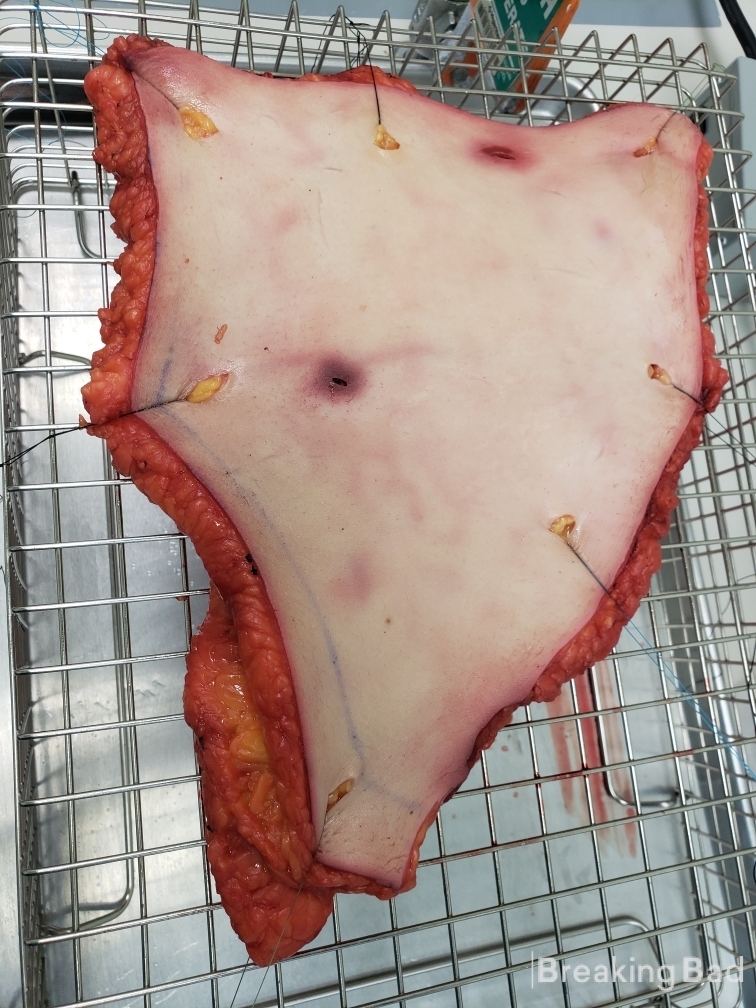
Espero que les haya gustado.
En la siguiente publicación, Structure Elucidation and Spectroscopic Analysis of Chromophores Produced by Oxidative Psilocin Dimerization, se trata el tema. Cuando se forma el dímero, es indetectable mediante análisis HPLC y ATR-FTIR, lo cual es extraño. Esto da a los grupos de investigación falsos positivos en cuanto a la pureza de la psilocina. He encontrado una manera de estabilizar la psilocina en el parche.
De todos modos, ¡comencemos! Hice cada paso yo mismo, con la ayuda de mi compañero que es ingeniero químico. Esto fue cuando tenía una licencia de la DEA schedule1 y 3 no sólo para la investigación, sino también para la fabricación.
Parte I (Síntesis de Psilocina)
paso 1: síntesis de 3-[2-(Dimetilamino)-2-oxoacetíl]-1H-indol-4-il Acetato
1a. Se equipó un matraz de 2000 mL, de cuatro cuellos y fondo redondo, con un agitador superior, un controlador de temperatura J-Kem, un embudo cuentagotas de 250 mL y un septo de goma a través del cual se introdujo una presión positiva de N2 seco. Se retiró el septo y el matraz se cargó equitativamente con acetato de 1H-indol-4-ilo (5; 50,1 g, 285 mmol, 1 equiv)
y Et2O anhidro (700 mL). El matraz se volvió a cerrar con el septo y se enjuaga con N2. La suspensión se agitó durante 10 min y después se
se enfrió a 0 °C en un baño de agua helada durante 30 min.
1b. Se cargó el embudo de goteo con una disolución de cloruro de oxalilo (37,1 mL, 428 mmol, 1,5 equiv) en Et2O (60 mL). La disolución de cloruro de oxalilo se añadió gota a gota a una velocidad suficiente para mantener la temperatura a 5 °C o menos, para minimizar la formación de dímeros y otros posibles subproductos. A medida que avanzaba la adición, se formó una suspensión amarilla de 10 y cuando se completó la adición, la mezcla se agitó durante 4 h.
1c. Transcurrido este tiempo, se añadió heptano (400 mL) y la mezcla se agitó durante 30 min a 0 °C. El sólido amarillo obtenido se filtró rápidamente y se lavó sucesivamente con heptano (2 × 300 mL), que se utilizó rápidamente en el paso siguiente. . Se añadió gota a gota una disolución 2,0 M de dimetilamina en THF (175 mL) a una velocidad suficiente para mantener la temperatura por debajo de 5 °C con el fin de minimizar las reacciones secundarias. Una vez completada la
Una vez completada la adición, se añadió gota a gota piridina (46 mL) en THF (100 mL) y la mezcla se agitó bien durante 60 min. Se añadió heptano (600 mL) y el contenido del matraz se filtró por succión con un embudo Büchner. El residuo filtrado se transfirió a un matraz de fondo redondo y se añadió H2O desionizada (1000 mL), se agitó durante 30 min y se filtró con un embudo Büchner. El sólido blanquecino se trituró secuencialmente durante 40 min en EtOAc (600 mL) y heptano (400mL). La suspensión se filtró a través de un embudo Büchner y el sólido se secó en un horno a 40 °C durante la noche para obtener 6 como un sólido amarillo claro; rendimiento: 66,1 g (81%); mp 205-207 °C.
ATR-FTIR confirmó la síntesis del 3-[2-(Dimetilamino)-2-oxoacetíl]-1H-indol-4-il Acetato. Este compuesto puede almacenarse a 4C durante varios meses.
Paso 2: Síntesis de Psilocina
Paso 2A: Se equipó un matraz de 2000 mL, de cuatro cuellos y fondo redondo, con un agitador de hélice, un controlador de temperatura J-Kem, un embudo cuentagotas de 250 mL, y un agitador de hélice.
250 mL y un septo de goma a través del cual se introdujo una presión positiva de N2 seco. Se retiró el septo y el matraz se cargó
matraz se cargó secuencialmente con acetato de 3-[2-(dimetilamino)-2-oxoacetil]-1H-indol-4-ilo (6; 31,5 g, 115 mmol) y 2-CH3-THF (1000
mL). El matraz se sumergió en un baño de hielo a 0 °C y se añadió una disolución de LiAlH4 2,3 M en 2-CH3-THF (140 mL, 322 mmol) a través de un embudo cuentagotas de 250 mL.
el embudo cuentagotas de 250 mL. El embudo cuentagotas se enjuagó con 2-CH3-THF adicional (20 mL). La disolución de LiAlH4 se añadió gota a gota
a un ritmo para mantener la temperatura por debajo de 20 °C. Tras la adición, se retiró el baño de agua helada y la mezcla se agitó durante 30 min.
La solución de color amarillo claro se calentó a reflujo (80 °C) con un manto calefactor y adquirió color marfil al cabo de 3 h. Se observó acumulación de sólidos amarillos en las paredes.
de sólidos amarillos en las paredes del matraz de fondo redondo.
Paso 2C. Se retiró el manto calefactor y se dejó enfriar el matraz hasta 50 °C. El matraz se volvió a
a 20 °C. La reacción se apagó mediante la adición secuencial de 3 gotas de NaOH 1 M acuoso y 3 gotas de H2O desionizado. La mezcla
se diluyó con THF (500 mL) y se agitó durante 20 min. La mezcla se filtró con un embudo Büchner y el filtrado se mantuvo bajo N2.
La torta filtrada se volvió a filtrar rápidamente con 200 mL de [solución al 10% de (7% de amoniaco en MeOH) en CH2Cl2] y THF (500 mL). Los filtrados
se combinaron y concentraron para dar un sólido verde. El sólido se trituró con 1:1 EtOAc/heptano (50 mL), después se filtró por
embudo Büchner. El sólido verde oscuro se secó en un horno a 40 °C durante la noche para dar psilocina seca (7) como sólido verde oscuro; rendimiento: 20,7
g (91%); mp 167-169 °C.
Se ha sintetizado la psilocina.
Parte II: Desarrollo del parche transdérmico de psilocina y estudio in vitro (ATENCIÓN: VERÁ CARNE HUMANA FRESCA, ES GRUESO)
A continuación, disuelvo la psilocina en una mezcla patentada de polímero de acrilato (en heptano), vierto la solución en una línea de liberación y utilizo una cuchilla de vaciado para obtener una capa adhesiva de 100 um. Una vez seca, aplico la capa de soporte y troquelo un parche de 1cm^2. Este parche se utiliza para el estudio in vitro.
La siguiente foto es una instantánea del aparato de difusión (parche encima de la piel con agua corriendo por debajo)
Espero que les haya gustado.


