Brain
Expert Pharmacologist
- Joined
- Jul 6, 2021
- Messages
- 320
- Reaction score
- 332
- Points
- 63
Dekstroamfetamiini (D-AMP) kuuluu keskushermoston stimulanttien luokkaan. Yhdysvaltain elintarvike- ja lääkevirasto luokittelee sen luettelossa II olevaksi aineeksi, jolla on suuri väärinkäyttöpotentiaali. FDA on hyväksynyt amfetamiinia välittömästi ja viivästetysti vapauttavia lääkkeitä ADHD:n ja narkolepsian hoitoon sekä aikuisilla että lapsilla. Dekstroamfetamiini eroaa sen heijastimesta - levoamfetamiinista - sillä se stimuloi hermostoa voimakkaammin dopamiinin ansiosta ja vähemmän noradrenaliinin ansiosta.
Dekstroamfetamiinin synteesi P2P:stä
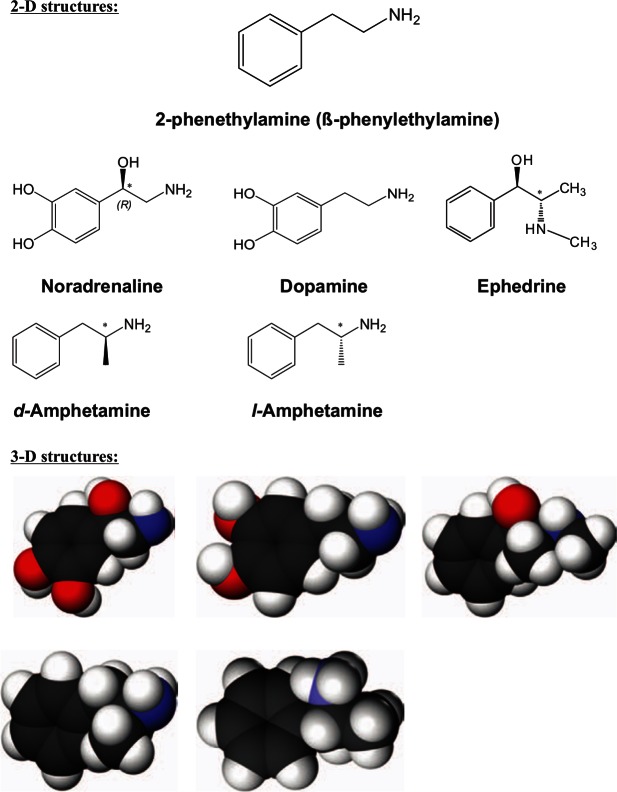
Aineen fysikaalis-kemialliset ominaisuudet ja muodot.
Pohjimmiltaan dekstroamfetamiini, samoin kuin amfetamiinirasemaatti, on väritön haihtuva öljyinen neste, jolla on tyypillinen "kalamainen" haju, ja se liukenee hyvin orgaanisiin liuottimiin. Sen kiehumispiste on 200-203 °C. Enantiomeeri voi olla jauhemaisen näköinen ja muodostaa pieniä valkoisia tai vaaleankeltaisia/kermanvärisiä "kiviä", joilla on heikko haju, heikosti hygroskooppinen, osittain veteen liukeneva, kun se on tabletin muodossa. Sitä esiintyy useimmiten sulfaatti-, hydrokloridi- ja sakkarattimuodossa ja hyvin harvoin fosfaattimuodossa. Yleensä dekstroamfetamiini on osa erilaisia lääkkeitä, kuten "Aderral" ja "Dexedrine", joissa sitä esiintyy sakkaratin ja sulfaatin muodossa pitoisuuksina 25 % kokonaistilavuudesta. Se on myös osa "Vyvanse"-, "Elvanse"- ja "Tyvense"-valmisteita, joissa se on dimesylaattilysdeksamfetamiinin proaktiivisessa tilassa; fermentointi l-lysiinin kanssa metaboloi sen d-amfetamiinin aktiiviseksi muodoksi; "Dexedrine". Muita lääkkeiden kauppanimiä ovat mm: Dexedriinisulfaatti, Afatin, d-Amfetasul, Domafate Obesedrin, Dexten, Maxiton, Sympamin, Simpamina-D, Albemap, Dadex, Ardex, Dexalone, Amsustain, Betafedrina, d-Betafedriini, Diocurb, Dextrostat.
Farmakokinetiikka.
Kun amfetamiini annetaan, se metaboloituu hydroksylaation kautta, jossa tärkein sytokromi on CYP2D6, beetahydroksylaatio (DBH) ja oksidatiivinen deaminaatio (FMO3); on olemassa muita entsyymejä, jotka osallistuvat amfetamiinin metaboliaan vähemmän, kuten butyraatti-CoA-ligaasi ja glysiini-N-asyltransferaasi. Biologinen hyötyosuus (kun ruoansulatuskanavan pH pysyy muuttumattomana) on 70-75 % rasemaatin osalta ja jopa 80-83 % dekstroamfetamiinin osalta. Sitoutuminen plasman proteiineihin on eri lähteiden mukaan 15-30 % terveillä ihmisillä, jakautumistilavuus on kohtalainen, aine läpäisee aktiivisesti veri-aivoesteen vaihtelevalla kertoimella 17p. T1/2 on noin 7-15 tuntia riippuen monista tekijöistä, kuten virtsan pH:sta (puoliintumisaika nopeutuu alhaisemmilla arvoilla). Imax - 15-70 minuuttia. Amfetamiinin d-isomeerin tappavaa annosta ei ole tutkittu; käytettävissä olevista ekstrapoloiduista tiedoista amfetamiinisulfaatin vakiorasemaatista (98-130 mg/kg) on kuitenkin teoreettisia päätelmiä suurista LD 50 -arvoista, jotka ovat 5-10 %. Amfetamiini eliminoituu lähes samoilla tunnettujen metaboliittien laadullisilla indikaattoreilla, mutta hippuriinihapon, bentsoyyliglykuronidin ja norefedriinin määrä on huomattavasti pienempi (60 % kaikista tiedoista), mikä johtuu tämän rasemaatin spesifisyydestä aineenvaihdunnan yhteydessä deaminointitasolla. Jyrsijöillä tehdyissä tutkimuksissa osoitettiin genotoksisuuden huomattava väheneminen verrattuna vakioamfetamiinirasemaattiin annoksella 4600 mg/ml.
Vaikutusmekanismi.
Farmakodynaaminen vaikutusmekanismi ei juuri poikkea amfetamiinin perusmuodosta. Serotoniinin, noradrenaliinin ja dopamiinin kuljettajien estämisen ja palautumisen kautta, vuorovaikutus TAAR1:n kanssa, mikä lopulta johtaa monoamiinien ja katekoliamiinien pitoisuuden kasvuun samanaikaisesti synaptisessa raossa (kalvojen välinen rako on 10-50 nm leveä, reunat ovat vahvistuneet solujen välisillä kontakteilla). Erityisesti dekstroamfetamiinin tärkeä ominaisuus on se, että oikeanpuoleisen enantiomeerin affiniteetti TAAR1:n kanssa on paljon suurempi (eri lähteiden mukaan 15-30 %), ja VMAT2 vangitsee pienemmän määrän tätä enantiomeeria, ja pienin affiniteetti serotoniinikuljettajalle, toisin kuin vasemmanpuoleisella, ja sellaisten järjestelmien kuten CDK5R1, DLG1 ja CAMKIIAA kuormitus on huomattavasti pienempi vastaavien kliinisten vaikutusten kanssa.
Yhtä tärkeää on Novascreen BioSciences Corporationin havaitsema tieteellinen tosiasia, jonka mukaan alhaisemman affiniteetin vuoksi useisiin reseptoreihin (a1-, a2-, b-adrenoreseptorit, mu-opioidi, histamiini, CCK, NK, GABA, ETeA ja muut) sekä ei-toivottujen kliinisten sivuvaikutusten että muiden negatiivisten seurausten vakavuus molekyylitasolla on huomattavasti vähäisempää, mikä määrittää tämän tietyn aineen muodon ensisijaisuuden vastaavien toivottujen kliinisten vaikutusten säilyttämisen kanssa. Näiden monivaikutteisten ominaisuuksien nettovaikutus on se, että d-amfetamiini lisää katekoliamiinien "saatavuutta" tai pitoisuuskykyä solunulkoisessa tilassa kääntämällä katekoliamiinien kuljetuksen hermosolun päätepisteestä, mikä on myös yksi oikealle kääntyvän enantiomeerin ominaisuuksista. Indikaattorit, joilla d-enantiomeeri estää rotan aivojen synaptosomien [3 H]-pitoisuuden ottoa, vaihtelevat ja eroavat merkittävästi amfetamiinirasemaatista. Noradrenaliinin osalta Ki = nM arvolla 45-50, dopamiinin osalta 82-200, 5-HT:n osalta indikaattorit vaihtelevat rotan aivomalleissa välillä 1840-3830. Tämän amfetamiinimuodon riippuvuussyklin "pehmeämpi" vaikutus on seurausta FosB:n suhteellisen vähäisemmästä yli-ilmentymisestä nucleus accumbensissa, positiivisten vaikutusten esiintymisestä ja CREB:n estämisen puuttumisesta proteiini- ja seriinifosfotaasien toimesta juuri alhaisemman affiniteetin ja vaikutuksen vuoksi glutamaatti- ja serotoniini-ergisiin järjestelmiin. Neurokemiallisilla vaikutuksilla on vertailussa myös erottuva kyky; Healin ja Wickensin tutkimuksissa havaittiin muutoksia motorisessa aktiivisuudessa, jossa sen enimmäisarvo oli 3-4 kertaa pienempi kuin amfetamiinihydrokloridin tai sulfaatin saannilla, mikä liittyy suoraan dopamiinin ulosvirtauksen nopeuteen ja molekyylikorjaukseen aivojen striatumissa.

Vaikka in vitro -kokeet antavat hyvän käsityksen yksittäisistä mekanismeista, amfetamiinin tehoa suhteessa muihin epäsuoriin monoamiiniagonisteihin, esimerkiksi klassisiin takaisinoton estäjiin, voidaan arvioida vain in vivo -kokeista. Olemme käyttäneet kaksoissondi-mikrodialyysiä tutkiaksemme d- ja l-amfetamiinin in vivo -vaikutuksia spontaanisti hypertensiivisellä rotalla (SHR), jota on ehdotettu ADHD:n jyrsijämalliksi. Molemmat amfetamiinin isomeerit lisäsivät annosriippuvaisesti noradrenaliinin solunulkoisia pitoisuuksia prefrontaalisessa aivokuoressa (PFC) ja dopamiinia striatumissa. Niiden vaikutusten farmakodynamiikka on tyypillistä monoamiinia vapauttavien aineiden osalta raportoiduille vaikutuksille, eli vaikutus alkaa nopeasti, jolloin noradrenaliinin ja dopamiinin ulosvirtauksen huippuarvot kasvavat 30-45 minuutissa, vaikutukset ovat suuria (400-450 % lähtötasosta noradrenaliinin osalta ja 700-1500 % lähtötasosta dopamiinin osalta) ja laskevat suhteellisen nopeasti maksimin jälkeen. Vaikka tähän katsaukseen ei ole sisällytetty vertailutuloksia, amfetamiinin isomeerien aiheuttamien lisäysten suuruusluokka on suurempi kuin klassisten takaisinoton estäjien, kuten atomoksetiinin tai bupropionin, osalta raportoidut lisäykset, eikä amfetamiinin vaikutuksilla ole annos-vaikutus-kattoa.
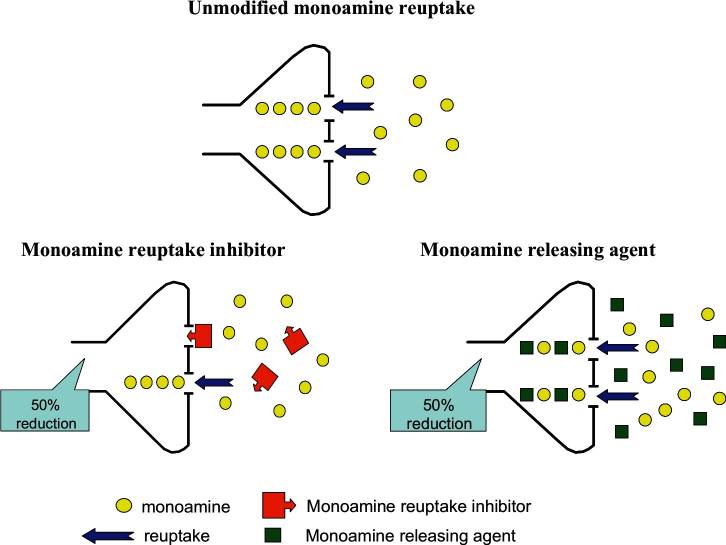
Kun verrataan lääkkeiden vaikutuksia katekoliamiinien poistumiseen PFC:ssä, on tärkeää ottaa huomioon tämän aivoalueen hyvin epätavallinen neuroanatomia. DAT-kohtien tiheys PFC:n dopaminergisissä neuroneissa on hyvin pieni, minkä vuoksi suurin osa vapautuvasta dopamiinista sekvestroituu NET:n kautta noradrenergisiin neuroneihin. Vaikka PFC:n dopaminergisissä neuroneissa on vähän DAT-kohtia, niiden takaisinottokyky riittää siihen, että amfetamiini saa aikaan merkittävän dopamiinin vapautumisen niistä, vaikka on ehdotettu, että suuri osa PFC:n dopamiinin vapautumisesta tulee noradrenergisistä neuroneista. Shire Developmentin in vivo -malleilla tehdyissä tutkimuksissa osoitettiin tilastollisesti merkitsevä ero. D-AMP vaikutti impulsiivisen kontrollin kognitiivisiin komponentteihin eri tavalla: impulsiivisen valinnan osuus väheni samalla palkkiotasolla, mikä myös vahvistaa tämän enantiomeerin tehokkuutta.
Käyttötavat ja annokset.
Amfetamiinin d-enantiomeerin virkistyskäyttöannos alkaa 40-60 mg:sta suun kautta käytettynä, jos esiintyy toleranssia, aloitusannos voidaan nostaa 120-160 mg:aan kerta-annoksena suun kautta käytettynä. Intranasaalisesti annosteltaessa suositellaan 30-50 mg:n aloitusannosta. Tämän lääkemuodon parenteraalinen anto on sallittua vain silloin, kun saadaan puhdasta liuosta. Kaikkia tabletteja tai jauheita suositellaan käytettäväksi vain suun kautta ja intranasaalisesti. Parenteraalisessa annostelussa aloitusannos on 0,15-0,24 mg/kg.
Amfetamiinimyrkytyksen kliininen kuva.
Edellä mainitut oireet ovat "lieviä", niiden vaikeusaste on jopa 40 % pienempi kuin yhdistelmämuodossa. Siksi sellaisia negatiivisia haittavaikutuksia kuin virtsaamisvaikeudet, sydämen rytmihäiriöt, kohonnut syke, kohonnut verenpaine, kohonnut hikoilu, korkea ruumiinlämpö, pahoinvointi, pupillien laajentuminen esiintyy yksinomaan suurilla annoksilla, ja ne ovat suhteessa erilaisia verrattuna raseaattiin.
1. Euforia ja lisääntyneen energian tunne;
2. Pitkittynyt valveillaolo;
3. Mahtipontiset ajatukset tai teot;
4. Väkivaltainen tai aggressiivinen käyttäytyminen;
5. Vahvistusvinouma;
6. Mielialan epävakaus;
7. Toistuvien stereotypioiden luonnehtima käyttäytyminen;
8. Kuulo-, näkö- tai tuntoharhoja;
9. Persoonallisuuden vääristymät;
10. Ruokahalun tukahduttaminen.
Lisäksi D-AMP:tä käyttävillä henkilöillä on oltava vähintään kaksi seuraavista oireista, jotta heidät voidaan diagnosoida:
1. Takykardia;
2. Arteriaalinen hypertensio;
3. Hikoilu ja kuumeiset vilunväristykset;
4. Pahoinvointi tai oksentelu;
5. Lihasheikkous;
6. Kipu tai epämukavuus rintalastan takana;
7. Psykomotorinen levottomuus;
8. Pupillin laajentuminen.
D-AMP-myrkytyksen oireisiin kuuluvat pääasiassa sydän- ja verisuoni- ja hermostokomplikaatioiden merkit. Hengityselinten häiriöt kehittyvät harvemmin.
Sydänhäiriöt: verenpainetauti ja takykardia ovat yleisimpiä, kun käytetään pieniä annoksia. Myös alkuvaiheen bradykardia on mahdollinen parasympaattisen tonuksen nousun vuoksi. Rytmihäiriöt (supraventrikulaariset ovat yleisiä) voivat johtua sympaattisesta kriisistä tai nopeiden natriumkanavien salpauksesta. Iskemia ja sydäninfarkti johtuvat sepelvaltimoiden kouristuksesta, joka on suurimmillaan 30 minuuttia intranasaalisen D-AMP:n käytön jälkeen ja osuu samaan aikaan lääkkeen huippupitoisuuden kanssa veressä. Lisää sepelvaltimoiden kouristusta voi kehittyä 90 minuutin kuluttua, mikä liittyy D-AMP-metaboliittien kertymiseen. Verihiutaleiden aggregaation lisääntyminen johtaa verihyytymien muodostumiseen sepelvaltimoissa. Lisäksi sydänlihaksen hapentarve kasvaa. Harvinainen komplikaatio on aortan repeämä.
Erityisohjeet, yhteisvaikutukset muiden aineiden kanssa.
Minkä tahansa amfetamiinimuodon käytön ehdottomia vasta-aiheita ovat: vaikea verisuonten ateroskleroosi, kaikki oireiset sydän- ja verisuonitaudit, MAO-saanti (ja 14 päivää tämän ryhmän lääkkeen viimeisen käyttökerran jälkeen), glaukooma, kilpirauhasen liikatoiminta.
"Ei-ADIOS"-sääntö:
Non-Alcohol - sitä ei suositella käytettäväksi alkoholin kanssa.
Ei-dissosiatiivit - ei suositella käytettäväksi dissosiatiivisten lääkkeiden kanssa.
Non-iMAO - sitä ei suositella käytettäväksi monoamiinioksidaasin estäjien kanssa.
Non-Opiates - ei suositella käytettäväksi opioidireseptoriagonistien kanssa.
Ei-stimulaattorit - ei suositella käytettäväksi stimulanttien kanssa.
1. Kun D-AMP:tä käytetään yhdessä PDE-5-estäjäryhmän lääkkeiden kanssa, molempien aineiden haittavaikutusten kehittymisen riski kasvaa. Yleisimmät haittavaikutukset: voimakas spastinen päänsärky, pahoinvointi. Vakavien kriittisten tilojen kehittymisen esiintyvyys on pieni.
2. Käytettäessä D-AMP:tä yhdessä marihuanan kanssa on olemassa riski kohonneen verenpaineen, päänsäryn, hienojakoisen vapinan, suun kuivumisen esiintymisestä. Vakavien kriittisten tilojen kehittymisen todennäköisyys on pieni.
3. Käytettäessä D-AMP:tä yhdessä neuroleptien/tasalääkkeiden kanssa on suuri riski D-AMP:n päävaikutusten tasoittumiseen. Vaikeiden kriittisten tilojen kehittymisen todennäköisyys on pieni (tapauksissa, joissa neuroleptien käytölle ei ole vasta-aiheita).
4. D-AMP:n käyttöä ei suositella antibakteeristen, antiviraalisten ja sienilääkkeiden, hormonien, antikoagulanttien hoidon aikana.
5. D-AMP:n käyttöä ei suositella minkään kirurgisen manipulaation aikana eikä sitä edeltävänä ja sen jälkeisenä aikana tietyn ajanjakson ajan (ajanjakso yksilöidään erikseen).
6. D-AMP:n käyttöä ei suositella, jos diagnosoitu jokin sydän- ja verisuonijärjestelmän, munuaisten, maksan, keuhkojen tai keskushermoston häiriö.
7. D-AMP:n käyttöä ei suositella raskauden ja imetyksen aikana.
Kahdessa aiemmin julkaistussa tutkimuksessa Jasinski ja Krishnan vertasivat IR-d-amfetamiinin subjektiivisia vaikutuksia huumekokemusta omaavilla vapaaehtoisilla ihmisillä, kun näitä yhdisteitä annettiin suonensisäisesti ja suun kautta. Tutkimuksessa, jossa he vertasivat näitä yhdisteitä oraalisen annostelun jälkeen, IR-d-amfetamiini (40 mg (29,6 mg d-amfetamiinipohjaa)) sai aikaan tilastollisesti merkitsevän lisäyksen suhteessa lumelääkkeeseen "Drug liking" -asteikolla (Drug Rating Questionnaire - Subject, DQRS), kun taas vastaava annos d-amfetamiinia (100 mg, oraalisesti) ei lisännyt sitä. Lisäksi d-amfetamiinin farmakologisen huippuvaikutuksen ajankohta oli huomattavasti myöhäisempi kuin IR-d-amfetamiinin: 3,0 tuntia verrattuna 1,5-2,0 tuntiin. Kun d-amfetamiinia annettiin 150 mg:n suuruisena annoksena, se lisäsi merkittävästi DQRS-mittarin "Drug liking" -pistemäärää samassa määrin kuin IR-d-amfetamiini (40 mg suun kautta). Suuremman d-amfetamiiniannoksen huippuvaikutus oli kuitenkin vieläkin myöhäisempi, 4,0 tuntia. Kun tutkittiin laskimonsisäistä annostelureittiä, IR-d-amfetamiinin (20 mg laskimonsisäisesti) huippupistemäärä "Drug liking" -pisteytyksessä saavutettiin 20 minuutin kuluttua annostelusta, mikä osui yksiin plasman Cmax-arvon kanssa. Sitä vastoin vastaava d-amfetamiiniannos (50 mg laskimonsisäisesti) ei lisännyt merkittävästi "Dug likeing" -arvoa suhteessa lumelääkkeeseen, ja plasman d-amfetamiinin Cmax-arvo saavutettiin huomattavasti myöhemmin, 2,0 h:ssa. Molemmat yhdisteet tuottivat vastaavat AUC0-24h-arvot, mutta verrattuna IR-d-amfetamiinin vastaavaan annokseen plasman d-amfetamiinin Cmax-arvo oli lisdeksamfetamiinin osalta kolme kertaa pienempi ja tmax-arvo oli kolme kertaa suurempi.
Ensiapu yliannostustapauksessa.
Toksisuuden mekanismi liittyy ensisijaisesti liialliseen solunulkoiseen dopamiiniin, noradrenaliiniin ja serotoniiniin. Ensisijaiseen kliiniseen oireyhtymään kuuluvat näkyvät neurologiset ja kardiovaskulaariset vaikutukset, mutta sekundaarisiin komplikaatioihin voi liittyä munuais-, lihas-, keuhko- ja GI-vaikutuksia. Hyperaktiivisuus, hypertermia, takykardia, takypnea, mydriaasi, vapina, kouristukset ja muuttunut psyykkinen tila ovat joitakin amfetamiinimyrkytyksen yleisimpiä oireita. Diagnoosi voidaan vahvistaa havaitsemalla amfetamiinia vatsan sisällöstä tai oksennuksesta tai positiivisella virtsan toksikologisella tutkimuksella laittomien huumausaineiden varalta. Väärän positiivinen amfetamiiniseula voi esiintyä trazodonin yliannostuksen tai bupropionin yliannostuksen jälkeen. Amfetamiinimyrkytykselle ei ole vastalääkettä, mutta aktiivihiili on hätähoito. Potilaille, jotka pystyvät juomaan turvallisesti, suositellaan annettavaksi aktiivihiiltä 1-2 g/kg, enintään 100 g suun kautta, jos nauttiminen on tapahtunut edellisen tunnin aikana. Amfetamiiniin liittyvä myrkytys vaatii hoitoa valvomalla henkeä uhkaavia keskushermosto- ja sydän- ja verisuonitauteja rauhallisessa ympäristössä.
Indikaatiot sairaalaan menolle tai ambulanssin kutsumiselle: tajunnan heikkeneminen tai puuttuminen, heikentynyt puhe, heikentynyt motoriikka, orientaation puute tilassa ja ajassa, yli puoli tuntia kestävä voimakas kipu rintalastan takana, yli 38,0 C:n ruumiinlämmön nousu tai yli puoli tuntia kestävä hypertermia, yli 180/110 mmHg:n verenpaineen nousu ilman, että verenpainetta alentavalla hoidolla on vaikutusta.
1. Potilaiden, joiden verenpaine on yli 140/95 mmHg, hoitoon kuuluu yksi tabletti beetasalpaajaa, jolla ei ole sisäistä sympatomimeettistä vaikutusta, yksi tabletti ACE:n estäjää, 30 minuutin kuluttua - yksi tabletti rauhoittavaa lääkettä (0,25 mg alpratsolaamia).
2. Potilailla, joilla on voimakas ahdistus, paniikkikohtaus, psykoosi: yksi tabletti rauhoittavaa lääkettä ja yksi tabletti rauhoittavaa neuroleptiä, psykologista apua, kiireellistä psykoterapiaa.
3. Potilailla, joilla on rintalastan kipu, epämukavuus rinnassa: yksi tabletti kolmannen sukupolven hitaita kalsiumkanavan salpaajia, jotka vähentävät refleksinomaisesti sykettä, yksi tabletti 3. sukupolven ACE-estäjää TAI yksi tabletti imidatsoliinivaikutteista agonistia TAI yksi tabletti ; jos kipuoireyhtymä ei lievene 20 minuutissa, on suositeltavaa mennä sairaalaan.
4. Kun ruumiinlämpö nousee enintään 37,5 C, määrätään dynaaminen tarkkailu puolen tunnin ajaksi. Farmakologista hoitoa ei tarvita. Jos hypertermia jatkuu yli puoli tuntia (ulkoisten syiden puuttuessa), on suositeltavaa mennä sairaalaan.
5. Potilailla, joilla on voimakasta päänsärkyä, on suositeltavaa käyttää kouristuslääkkeitä yhdessä rauhoittavien kasviperäisten lääkkeiden tai rauhoittavien lääkkeiden kanssa pieninä annoksina. Jos päänsärkyyn liittyy oksentelua, suositellaan metoklopramidin 2,0 ml:n lihaksensisäistä injektiota. Yksittäinen pahoinvointi ja toiminnallinen dyspepsia eivät vaadi farmakologista hoitoa.
6. Vapinaan, kohtalaisiin kouristuksiin tai lievään psykomotoriseen levottomuuteen suositellaan rauhoittavia lääkkeitä. Neuroleptien käyttöä näissä tapauksissa ei suositella.
Beetasalpaaja, kuten propranololi, voi auttaa hallitsemaan sydämen takyarytmioita. Harkitse laskimonsisäistä nitroprussidia (aloita 0,5-1 mcg/kg minuutissa ja titraa tarpeen mukaan) vaikean hypertension hoitoon. Suonensisäistä nestettä on annettava, koska se ehkäisee hypertermiaa, auttaa ylläpitämään munuaisten toimintaa ja edistää amfetamiinin ja sen analogien poistumista. Vakavissa levottomuustapauksissa lääkäreiden on harkittava aggressiivista hoitoa pahanlaatuisen hypertension, rabdomyolyysin, hypertermian ja kouristusten välttämiseksi. Näyttö tukee suurten bentsodiatsepiiniannosten käyttöä amfetamiinin yliannostukseen liittyvän psykoosin ja levottomuuden hoidossa. Jos levottomuus, delirium ja liikehäiriöt eivät reagoi bentsodiatsepiineihin, voidaan käyttää toisen linjan hoitomuotoja, kuten antipsykootteja, kuten ziprasidonia tai haloperidolia, keskushermostoon vaikuttavia alfa-adrenoreseptoriagonisteja, kuten deksmedetomidiinia, tai propofolia. Neuromuskulaarinen halvaus, intubaatio ja aktiiviset jäähdytystoimenpiteet voivat olla tarpeen vakavissa tapauksissa. Potilaille, joilla on takykardia, on hankittava EKG ja harkittava telemetriaa. Käytä suonensisäistä nestettä ja rauhoittavia lääkkeitä sydänoireiden hallitsemiseksi. Jos potilaalla on vaikea hypertensio, harkitse suonensisäistä nitroprussidia. 0,9-prosenttisen normaalin keittosuolaliuoksen antaminen ja kreatiinikinaasin (CK), elektrolyyttien ja kreatiniinin seuranta on paras tapa hoitaa rabdomyolyysiä.
On tapausselostuksia Takotsubo-kardiomyopatiasta (TTC), joka tunnetaan myös stressin aiheuttamana kardiomyopatiana ja jonka laukaisee amfetamiinin yliannostus. Eräässä tapauksessa potilas saapui päivystyspoliklinikalle nautittuaan 30 amfetamiinisuolaista tablettia, ja oireina oli rintakipu ja hengenahdistus. Esittelyhetkellä sydämen entsyymit olivat koholla, elektrokardiogrammi oli merkityksetön, ja ejektiofraktio (EF) oli 25-30 prosenttia ja siinä oli vaikea hypokinesia. Vuorokautta myöhemmin oireet kuitenkin hävisivät, ja kolme päivää myöhemmin tehdyssä toistetussa kaikukardiografiassa EF oli 60 %, eikä alueellisia seinämäliikkeen poikkeavuuksia ollut.
Havainto- ja tallennussäännöt.
Pääsääntöisesti amfetamiinirasemaatin sekä d-enantiomeerin varastointi on suoritettava valolta ja kosteudelta suojatussa paikassa, mieluiten huoneenlämmössä tai vähintään 5 C:n ja enintään 40 C:n lämpötilassa. Sitä voidaan säilyttää elintarvikepaperissa tai polyeteenitereftalaattipakkauksissa, joissa ei ole metallisisältöä.
Dekstroamfetamiinin kerta-annoksen intranasaalisen käytön jälkeen havaitsemisjakso virtsassa on pikatutkimusmenetelmiä käytettäessä noin 46-72 tuntia, suun kautta käytettäessä jopa 120-220 tuntia. Dekstroamfetamiinin pitkäaikaista systemaattista käyttöä ei ole tutkittu metaboliittien tunnistamisen yhteydessä, vaikka teoreettisesti tiedetään, että on suuri mahdollisuus havaita tärkeimmät metaboliitit PFIA:lla tai kromatografia-massaspektrometrialla 1,5-2 kuukauden aikana viimeisen amfetamiinin käytön jälkeen (mikä on vähemmän kuin amfetamiinirasemaatilla). Dekstroamfetamiinimetaboliittien havaitsemisjakso hiuksissa on enintään 2,5-3 kuukautta.
Dekstroamfetamiinin synteesi P2P:stä
Aineen fysikaalis-kemialliset ominaisuudet ja muodot.
Pohjimmiltaan dekstroamfetamiini, samoin kuin amfetamiinirasemaatti, on väritön haihtuva öljyinen neste, jolla on tyypillinen "kalamainen" haju, ja se liukenee hyvin orgaanisiin liuottimiin. Sen kiehumispiste on 200-203 °C. Enantiomeeri voi olla jauhemaisen näköinen ja muodostaa pieniä valkoisia tai vaaleankeltaisia/kermanvärisiä "kiviä", joilla on heikko haju, heikosti hygroskooppinen, osittain veteen liukeneva, kun se on tabletin muodossa. Sitä esiintyy useimmiten sulfaatti-, hydrokloridi- ja sakkarattimuodossa ja hyvin harvoin fosfaattimuodossa. Yleensä dekstroamfetamiini on osa erilaisia lääkkeitä, kuten "Aderral" ja "Dexedrine", joissa sitä esiintyy sakkaratin ja sulfaatin muodossa pitoisuuksina 25 % kokonaistilavuudesta. Se on myös osa "Vyvanse"-, "Elvanse"- ja "Tyvense"-valmisteita, joissa se on dimesylaattilysdeksamfetamiinin proaktiivisessa tilassa; fermentointi l-lysiinin kanssa metaboloi sen d-amfetamiinin aktiiviseksi muodoksi; "Dexedrine". Muita lääkkeiden kauppanimiä ovat mm: Dexedriinisulfaatti, Afatin, d-Amfetasul, Domafate Obesedrin, Dexten, Maxiton, Sympamin, Simpamina-D, Albemap, Dadex, Ardex, Dexalone, Amsustain, Betafedrina, d-Betafedriini, Diocurb, Dextrostat.
Farmakokinetiikka.
Kun amfetamiini annetaan, se metaboloituu hydroksylaation kautta, jossa tärkein sytokromi on CYP2D6, beetahydroksylaatio (DBH) ja oksidatiivinen deaminaatio (FMO3); on olemassa muita entsyymejä, jotka osallistuvat amfetamiinin metaboliaan vähemmän, kuten butyraatti-CoA-ligaasi ja glysiini-N-asyltransferaasi. Biologinen hyötyosuus (kun ruoansulatuskanavan pH pysyy muuttumattomana) on 70-75 % rasemaatin osalta ja jopa 80-83 % dekstroamfetamiinin osalta. Sitoutuminen plasman proteiineihin on eri lähteiden mukaan 15-30 % terveillä ihmisillä, jakautumistilavuus on kohtalainen, aine läpäisee aktiivisesti veri-aivoesteen vaihtelevalla kertoimella 17p. T1/2 on noin 7-15 tuntia riippuen monista tekijöistä, kuten virtsan pH:sta (puoliintumisaika nopeutuu alhaisemmilla arvoilla). Imax - 15-70 minuuttia. Amfetamiinin d-isomeerin tappavaa annosta ei ole tutkittu; käytettävissä olevista ekstrapoloiduista tiedoista amfetamiinisulfaatin vakiorasemaatista (98-130 mg/kg) on kuitenkin teoreettisia päätelmiä suurista LD 50 -arvoista, jotka ovat 5-10 %. Amfetamiini eliminoituu lähes samoilla tunnettujen metaboliittien laadullisilla indikaattoreilla, mutta hippuriinihapon, bentsoyyliglykuronidin ja norefedriinin määrä on huomattavasti pienempi (60 % kaikista tiedoista), mikä johtuu tämän rasemaatin spesifisyydestä aineenvaihdunnan yhteydessä deaminointitasolla. Jyrsijöillä tehdyissä tutkimuksissa osoitettiin genotoksisuuden huomattava väheneminen verrattuna vakioamfetamiinirasemaattiin annoksella 4600 mg/ml.
Vaikutusmekanismi.
Farmakodynaaminen vaikutusmekanismi ei juuri poikkea amfetamiinin perusmuodosta. Serotoniinin, noradrenaliinin ja dopamiinin kuljettajien estämisen ja palautumisen kautta, vuorovaikutus TAAR1:n kanssa, mikä lopulta johtaa monoamiinien ja katekoliamiinien pitoisuuden kasvuun samanaikaisesti synaptisessa raossa (kalvojen välinen rako on 10-50 nm leveä, reunat ovat vahvistuneet solujen välisillä kontakteilla). Erityisesti dekstroamfetamiinin tärkeä ominaisuus on se, että oikeanpuoleisen enantiomeerin affiniteetti TAAR1:n kanssa on paljon suurempi (eri lähteiden mukaan 15-30 %), ja VMAT2 vangitsee pienemmän määrän tätä enantiomeeria, ja pienin affiniteetti serotoniinikuljettajalle, toisin kuin vasemmanpuoleisella, ja sellaisten järjestelmien kuten CDK5R1, DLG1 ja CAMKIIAA kuormitus on huomattavasti pienempi vastaavien kliinisten vaikutusten kanssa.
Yhtä tärkeää on Novascreen BioSciences Corporationin havaitsema tieteellinen tosiasia, jonka mukaan alhaisemman affiniteetin vuoksi useisiin reseptoreihin (a1-, a2-, b-adrenoreseptorit, mu-opioidi, histamiini, CCK, NK, GABA, ETeA ja muut) sekä ei-toivottujen kliinisten sivuvaikutusten että muiden negatiivisten seurausten vakavuus molekyylitasolla on huomattavasti vähäisempää, mikä määrittää tämän tietyn aineen muodon ensisijaisuuden vastaavien toivottujen kliinisten vaikutusten säilyttämisen kanssa. Näiden monivaikutteisten ominaisuuksien nettovaikutus on se, että d-amfetamiini lisää katekoliamiinien "saatavuutta" tai pitoisuuskykyä solunulkoisessa tilassa kääntämällä katekoliamiinien kuljetuksen hermosolun päätepisteestä, mikä on myös yksi oikealle kääntyvän enantiomeerin ominaisuuksista. Indikaattorit, joilla d-enantiomeeri estää rotan aivojen synaptosomien [3 H]-pitoisuuden ottoa, vaihtelevat ja eroavat merkittävästi amfetamiinirasemaatista. Noradrenaliinin osalta Ki = nM arvolla 45-50, dopamiinin osalta 82-200, 5-HT:n osalta indikaattorit vaihtelevat rotan aivomalleissa välillä 1840-3830. Tämän amfetamiinimuodon riippuvuussyklin "pehmeämpi" vaikutus on seurausta FosB:n suhteellisen vähäisemmästä yli-ilmentymisestä nucleus accumbensissa, positiivisten vaikutusten esiintymisestä ja CREB:n estämisen puuttumisesta proteiini- ja seriinifosfotaasien toimesta juuri alhaisemman affiniteetin ja vaikutuksen vuoksi glutamaatti- ja serotoniini-ergisiin järjestelmiin. Neurokemiallisilla vaikutuksilla on vertailussa myös erottuva kyky; Healin ja Wickensin tutkimuksissa havaittiin muutoksia motorisessa aktiivisuudessa, jossa sen enimmäisarvo oli 3-4 kertaa pienempi kuin amfetamiinihydrokloridin tai sulfaatin saannilla, mikä liittyy suoraan dopamiinin ulosvirtauksen nopeuteen ja molekyylikorjaukseen aivojen striatumissa.
Vaikka in vitro -kokeet antavat hyvän käsityksen yksittäisistä mekanismeista, amfetamiinin tehoa suhteessa muihin epäsuoriin monoamiiniagonisteihin, esimerkiksi klassisiin takaisinoton estäjiin, voidaan arvioida vain in vivo -kokeista. Olemme käyttäneet kaksoissondi-mikrodialyysiä tutkiaksemme d- ja l-amfetamiinin in vivo -vaikutuksia spontaanisti hypertensiivisellä rotalla (SHR), jota on ehdotettu ADHD:n jyrsijämalliksi. Molemmat amfetamiinin isomeerit lisäsivät annosriippuvaisesti noradrenaliinin solunulkoisia pitoisuuksia prefrontaalisessa aivokuoressa (PFC) ja dopamiinia striatumissa. Niiden vaikutusten farmakodynamiikka on tyypillistä monoamiinia vapauttavien aineiden osalta raportoiduille vaikutuksille, eli vaikutus alkaa nopeasti, jolloin noradrenaliinin ja dopamiinin ulosvirtauksen huippuarvot kasvavat 30-45 minuutissa, vaikutukset ovat suuria (400-450 % lähtötasosta noradrenaliinin osalta ja 700-1500 % lähtötasosta dopamiinin osalta) ja laskevat suhteellisen nopeasti maksimin jälkeen. Vaikka tähän katsaukseen ei ole sisällytetty vertailutuloksia, amfetamiinin isomeerien aiheuttamien lisäysten suuruusluokka on suurempi kuin klassisten takaisinoton estäjien, kuten atomoksetiinin tai bupropionin, osalta raportoidut lisäykset, eikä amfetamiinin vaikutuksilla ole annos-vaikutus-kattoa.
Kun verrataan lääkkeiden vaikutuksia katekoliamiinien poistumiseen PFC:ssä, on tärkeää ottaa huomioon tämän aivoalueen hyvin epätavallinen neuroanatomia. DAT-kohtien tiheys PFC:n dopaminergisissä neuroneissa on hyvin pieni, minkä vuoksi suurin osa vapautuvasta dopamiinista sekvestroituu NET:n kautta noradrenergisiin neuroneihin. Vaikka PFC:n dopaminergisissä neuroneissa on vähän DAT-kohtia, niiden takaisinottokyky riittää siihen, että amfetamiini saa aikaan merkittävän dopamiinin vapautumisen niistä, vaikka on ehdotettu, että suuri osa PFC:n dopamiinin vapautumisesta tulee noradrenergisistä neuroneista. Shire Developmentin in vivo -malleilla tehdyissä tutkimuksissa osoitettiin tilastollisesti merkitsevä ero. D-AMP vaikutti impulsiivisen kontrollin kognitiivisiin komponentteihin eri tavalla: impulsiivisen valinnan osuus väheni samalla palkkiotasolla, mikä myös vahvistaa tämän enantiomeerin tehokkuutta.
Käyttötavat ja annokset.
Amfetamiinin d-enantiomeerin virkistyskäyttöannos alkaa 40-60 mg:sta suun kautta käytettynä, jos esiintyy toleranssia, aloitusannos voidaan nostaa 120-160 mg:aan kerta-annoksena suun kautta käytettynä. Intranasaalisesti annosteltaessa suositellaan 30-50 mg:n aloitusannosta. Tämän lääkemuodon parenteraalinen anto on sallittua vain silloin, kun saadaan puhdasta liuosta. Kaikkia tabletteja tai jauheita suositellaan käytettäväksi vain suun kautta ja intranasaalisesti. Parenteraalisessa annostelussa aloitusannos on 0,15-0,24 mg/kg.
Amfetamiinimyrkytyksen kliininen kuva.
Edellä mainitut oireet ovat "lieviä", niiden vaikeusaste on jopa 40 % pienempi kuin yhdistelmämuodossa. Siksi sellaisia negatiivisia haittavaikutuksia kuin virtsaamisvaikeudet, sydämen rytmihäiriöt, kohonnut syke, kohonnut verenpaine, kohonnut hikoilu, korkea ruumiinlämpö, pahoinvointi, pupillien laajentuminen esiintyy yksinomaan suurilla annoksilla, ja ne ovat suhteessa erilaisia verrattuna raseaattiin.
1. Euforia ja lisääntyneen energian tunne;
2. Pitkittynyt valveillaolo;
3. Mahtipontiset ajatukset tai teot;
4. Väkivaltainen tai aggressiivinen käyttäytyminen;
5. Vahvistusvinouma;
6. Mielialan epävakaus;
7. Toistuvien stereotypioiden luonnehtima käyttäytyminen;
8. Kuulo-, näkö- tai tuntoharhoja;
9. Persoonallisuuden vääristymät;
10. Ruokahalun tukahduttaminen.
Lisäksi D-AMP:tä käyttävillä henkilöillä on oltava vähintään kaksi seuraavista oireista, jotta heidät voidaan diagnosoida:
1. Takykardia;
2. Arteriaalinen hypertensio;
3. Hikoilu ja kuumeiset vilunväristykset;
4. Pahoinvointi tai oksentelu;
5. Lihasheikkous;
6. Kipu tai epämukavuus rintalastan takana;
7. Psykomotorinen levottomuus;
8. Pupillin laajentuminen.
D-AMP-myrkytyksen oireisiin kuuluvat pääasiassa sydän- ja verisuoni- ja hermostokomplikaatioiden merkit. Hengityselinten häiriöt kehittyvät harvemmin.
Sydänhäiriöt: verenpainetauti ja takykardia ovat yleisimpiä, kun käytetään pieniä annoksia. Myös alkuvaiheen bradykardia on mahdollinen parasympaattisen tonuksen nousun vuoksi. Rytmihäiriöt (supraventrikulaariset ovat yleisiä) voivat johtua sympaattisesta kriisistä tai nopeiden natriumkanavien salpauksesta. Iskemia ja sydäninfarkti johtuvat sepelvaltimoiden kouristuksesta, joka on suurimmillaan 30 minuuttia intranasaalisen D-AMP:n käytön jälkeen ja osuu samaan aikaan lääkkeen huippupitoisuuden kanssa veressä. Lisää sepelvaltimoiden kouristusta voi kehittyä 90 minuutin kuluttua, mikä liittyy D-AMP-metaboliittien kertymiseen. Verihiutaleiden aggregaation lisääntyminen johtaa verihyytymien muodostumiseen sepelvaltimoissa. Lisäksi sydänlihaksen hapentarve kasvaa. Harvinainen komplikaatio on aortan repeämä.
Erityisohjeet, yhteisvaikutukset muiden aineiden kanssa.
Minkä tahansa amfetamiinimuodon käytön ehdottomia vasta-aiheita ovat: vaikea verisuonten ateroskleroosi, kaikki oireiset sydän- ja verisuonitaudit, MAO-saanti (ja 14 päivää tämän ryhmän lääkkeen viimeisen käyttökerran jälkeen), glaukooma, kilpirauhasen liikatoiminta.
"Ei-ADIOS"-sääntö:
Non-Alcohol - sitä ei suositella käytettäväksi alkoholin kanssa.
Ei-dissosiatiivit - ei suositella käytettäväksi dissosiatiivisten lääkkeiden kanssa.
Non-iMAO - sitä ei suositella käytettäväksi monoamiinioksidaasin estäjien kanssa.
Non-Opiates - ei suositella käytettäväksi opioidireseptoriagonistien kanssa.
Ei-stimulaattorit - ei suositella käytettäväksi stimulanttien kanssa.
1. Kun D-AMP:tä käytetään yhdessä PDE-5-estäjäryhmän lääkkeiden kanssa, molempien aineiden haittavaikutusten kehittymisen riski kasvaa. Yleisimmät haittavaikutukset: voimakas spastinen päänsärky, pahoinvointi. Vakavien kriittisten tilojen kehittymisen esiintyvyys on pieni.
2. Käytettäessä D-AMP:tä yhdessä marihuanan kanssa on olemassa riski kohonneen verenpaineen, päänsäryn, hienojakoisen vapinan, suun kuivumisen esiintymisestä. Vakavien kriittisten tilojen kehittymisen todennäköisyys on pieni.
3. Käytettäessä D-AMP:tä yhdessä neuroleptien/tasalääkkeiden kanssa on suuri riski D-AMP:n päävaikutusten tasoittumiseen. Vaikeiden kriittisten tilojen kehittymisen todennäköisyys on pieni (tapauksissa, joissa neuroleptien käytölle ei ole vasta-aiheita).
4. D-AMP:n käyttöä ei suositella antibakteeristen, antiviraalisten ja sienilääkkeiden, hormonien, antikoagulanttien hoidon aikana.
5. D-AMP:n käyttöä ei suositella minkään kirurgisen manipulaation aikana eikä sitä edeltävänä ja sen jälkeisenä aikana tietyn ajanjakson ajan (ajanjakso yksilöidään erikseen).
6. D-AMP:n käyttöä ei suositella, jos diagnosoitu jokin sydän- ja verisuonijärjestelmän, munuaisten, maksan, keuhkojen tai keskushermoston häiriö.
7. D-AMP:n käyttöä ei suositella raskauden ja imetyksen aikana.
Kahdessa aiemmin julkaistussa tutkimuksessa Jasinski ja Krishnan vertasivat IR-d-amfetamiinin subjektiivisia vaikutuksia huumekokemusta omaavilla vapaaehtoisilla ihmisillä, kun näitä yhdisteitä annettiin suonensisäisesti ja suun kautta. Tutkimuksessa, jossa he vertasivat näitä yhdisteitä oraalisen annostelun jälkeen, IR-d-amfetamiini (40 mg (29,6 mg d-amfetamiinipohjaa)) sai aikaan tilastollisesti merkitsevän lisäyksen suhteessa lumelääkkeeseen "Drug liking" -asteikolla (Drug Rating Questionnaire - Subject, DQRS), kun taas vastaava annos d-amfetamiinia (100 mg, oraalisesti) ei lisännyt sitä. Lisäksi d-amfetamiinin farmakologisen huippuvaikutuksen ajankohta oli huomattavasti myöhäisempi kuin IR-d-amfetamiinin: 3,0 tuntia verrattuna 1,5-2,0 tuntiin. Kun d-amfetamiinia annettiin 150 mg:n suuruisena annoksena, se lisäsi merkittävästi DQRS-mittarin "Drug liking" -pistemäärää samassa määrin kuin IR-d-amfetamiini (40 mg suun kautta). Suuremman d-amfetamiiniannoksen huippuvaikutus oli kuitenkin vieläkin myöhäisempi, 4,0 tuntia. Kun tutkittiin laskimonsisäistä annostelureittiä, IR-d-amfetamiinin (20 mg laskimonsisäisesti) huippupistemäärä "Drug liking" -pisteytyksessä saavutettiin 20 minuutin kuluttua annostelusta, mikä osui yksiin plasman Cmax-arvon kanssa. Sitä vastoin vastaava d-amfetamiiniannos (50 mg laskimonsisäisesti) ei lisännyt merkittävästi "Dug likeing" -arvoa suhteessa lumelääkkeeseen, ja plasman d-amfetamiinin Cmax-arvo saavutettiin huomattavasti myöhemmin, 2,0 h:ssa. Molemmat yhdisteet tuottivat vastaavat AUC0-24h-arvot, mutta verrattuna IR-d-amfetamiinin vastaavaan annokseen plasman d-amfetamiinin Cmax-arvo oli lisdeksamfetamiinin osalta kolme kertaa pienempi ja tmax-arvo oli kolme kertaa suurempi.
Ensiapu yliannostustapauksessa.
Toksisuuden mekanismi liittyy ensisijaisesti liialliseen solunulkoiseen dopamiiniin, noradrenaliiniin ja serotoniiniin. Ensisijaiseen kliiniseen oireyhtymään kuuluvat näkyvät neurologiset ja kardiovaskulaariset vaikutukset, mutta sekundaarisiin komplikaatioihin voi liittyä munuais-, lihas-, keuhko- ja GI-vaikutuksia. Hyperaktiivisuus, hypertermia, takykardia, takypnea, mydriaasi, vapina, kouristukset ja muuttunut psyykkinen tila ovat joitakin amfetamiinimyrkytyksen yleisimpiä oireita. Diagnoosi voidaan vahvistaa havaitsemalla amfetamiinia vatsan sisällöstä tai oksennuksesta tai positiivisella virtsan toksikologisella tutkimuksella laittomien huumausaineiden varalta. Väärän positiivinen amfetamiiniseula voi esiintyä trazodonin yliannostuksen tai bupropionin yliannostuksen jälkeen. Amfetamiinimyrkytykselle ei ole vastalääkettä, mutta aktiivihiili on hätähoito. Potilaille, jotka pystyvät juomaan turvallisesti, suositellaan annettavaksi aktiivihiiltä 1-2 g/kg, enintään 100 g suun kautta, jos nauttiminen on tapahtunut edellisen tunnin aikana. Amfetamiiniin liittyvä myrkytys vaatii hoitoa valvomalla henkeä uhkaavia keskushermosto- ja sydän- ja verisuonitauteja rauhallisessa ympäristössä.
Indikaatiot sairaalaan menolle tai ambulanssin kutsumiselle: tajunnan heikkeneminen tai puuttuminen, heikentynyt puhe, heikentynyt motoriikka, orientaation puute tilassa ja ajassa, yli puoli tuntia kestävä voimakas kipu rintalastan takana, yli 38,0 C:n ruumiinlämmön nousu tai yli puoli tuntia kestävä hypertermia, yli 180/110 mmHg:n verenpaineen nousu ilman, että verenpainetta alentavalla hoidolla on vaikutusta.
1. Potilaiden, joiden verenpaine on yli 140/95 mmHg, hoitoon kuuluu yksi tabletti beetasalpaajaa, jolla ei ole sisäistä sympatomimeettistä vaikutusta, yksi tabletti ACE:n estäjää, 30 minuutin kuluttua - yksi tabletti rauhoittavaa lääkettä (0,25 mg alpratsolaamia).
2. Potilailla, joilla on voimakas ahdistus, paniikkikohtaus, psykoosi: yksi tabletti rauhoittavaa lääkettä ja yksi tabletti rauhoittavaa neuroleptiä, psykologista apua, kiireellistä psykoterapiaa.
3. Potilailla, joilla on rintalastan kipu, epämukavuus rinnassa: yksi tabletti kolmannen sukupolven hitaita kalsiumkanavan salpaajia, jotka vähentävät refleksinomaisesti sykettä, yksi tabletti 3. sukupolven ACE-estäjää TAI yksi tabletti imidatsoliinivaikutteista agonistia TAI yksi tabletti ; jos kipuoireyhtymä ei lievene 20 minuutissa, on suositeltavaa mennä sairaalaan.
4. Kun ruumiinlämpö nousee enintään 37,5 C, määrätään dynaaminen tarkkailu puolen tunnin ajaksi. Farmakologista hoitoa ei tarvita. Jos hypertermia jatkuu yli puoli tuntia (ulkoisten syiden puuttuessa), on suositeltavaa mennä sairaalaan.
5. Potilailla, joilla on voimakasta päänsärkyä, on suositeltavaa käyttää kouristuslääkkeitä yhdessä rauhoittavien kasviperäisten lääkkeiden tai rauhoittavien lääkkeiden kanssa pieninä annoksina. Jos päänsärkyyn liittyy oksentelua, suositellaan metoklopramidin 2,0 ml:n lihaksensisäistä injektiota. Yksittäinen pahoinvointi ja toiminnallinen dyspepsia eivät vaadi farmakologista hoitoa.
6. Vapinaan, kohtalaisiin kouristuksiin tai lievään psykomotoriseen levottomuuteen suositellaan rauhoittavia lääkkeitä. Neuroleptien käyttöä näissä tapauksissa ei suositella.
Beetasalpaaja, kuten propranololi, voi auttaa hallitsemaan sydämen takyarytmioita. Harkitse laskimonsisäistä nitroprussidia (aloita 0,5-1 mcg/kg minuutissa ja titraa tarpeen mukaan) vaikean hypertension hoitoon. Suonensisäistä nestettä on annettava, koska se ehkäisee hypertermiaa, auttaa ylläpitämään munuaisten toimintaa ja edistää amfetamiinin ja sen analogien poistumista. Vakavissa levottomuustapauksissa lääkäreiden on harkittava aggressiivista hoitoa pahanlaatuisen hypertension, rabdomyolyysin, hypertermian ja kouristusten välttämiseksi. Näyttö tukee suurten bentsodiatsepiiniannosten käyttöä amfetamiinin yliannostukseen liittyvän psykoosin ja levottomuuden hoidossa. Jos levottomuus, delirium ja liikehäiriöt eivät reagoi bentsodiatsepiineihin, voidaan käyttää toisen linjan hoitomuotoja, kuten antipsykootteja, kuten ziprasidonia tai haloperidolia, keskushermostoon vaikuttavia alfa-adrenoreseptoriagonisteja, kuten deksmedetomidiinia, tai propofolia. Neuromuskulaarinen halvaus, intubaatio ja aktiiviset jäähdytystoimenpiteet voivat olla tarpeen vakavissa tapauksissa. Potilaille, joilla on takykardia, on hankittava EKG ja harkittava telemetriaa. Käytä suonensisäistä nestettä ja rauhoittavia lääkkeitä sydänoireiden hallitsemiseksi. Jos potilaalla on vaikea hypertensio, harkitse suonensisäistä nitroprussidia. 0,9-prosenttisen normaalin keittosuolaliuoksen antaminen ja kreatiinikinaasin (CK), elektrolyyttien ja kreatiniinin seuranta on paras tapa hoitaa rabdomyolyysiä.
On tapausselostuksia Takotsubo-kardiomyopatiasta (TTC), joka tunnetaan myös stressin aiheuttamana kardiomyopatiana ja jonka laukaisee amfetamiinin yliannostus. Eräässä tapauksessa potilas saapui päivystyspoliklinikalle nautittuaan 30 amfetamiinisuolaista tablettia, ja oireina oli rintakipu ja hengenahdistus. Esittelyhetkellä sydämen entsyymit olivat koholla, elektrokardiogrammi oli merkityksetön, ja ejektiofraktio (EF) oli 25-30 prosenttia ja siinä oli vaikea hypokinesia. Vuorokautta myöhemmin oireet kuitenkin hävisivät, ja kolme päivää myöhemmin tehdyssä toistetussa kaikukardiografiassa EF oli 60 %, eikä alueellisia seinämäliikkeen poikkeavuuksia ollut.
Havainto- ja tallennussäännöt.
Pääsääntöisesti amfetamiinirasemaatin sekä d-enantiomeerin varastointi on suoritettava valolta ja kosteudelta suojatussa paikassa, mieluiten huoneenlämmössä tai vähintään 5 C:n ja enintään 40 C:n lämpötilassa. Sitä voidaan säilyttää elintarvikepaperissa tai polyeteenitereftalaattipakkauksissa, joissa ei ole metallisisältöä.
Dekstroamfetamiinin kerta-annoksen intranasaalisen käytön jälkeen havaitsemisjakso virtsassa on pikatutkimusmenetelmiä käytettäessä noin 46-72 tuntia, suun kautta käytettäessä jopa 120-220 tuntia. Dekstroamfetamiinin pitkäaikaista systemaattista käyttöä ei ole tutkittu metaboliittien tunnistamisen yhteydessä, vaikka teoreettisesti tiedetään, että on suuri mahdollisuus havaita tärkeimmät metaboliitit PFIA:lla tai kromatografia-massaspektrometrialla 1,5-2 kuukauden aikana viimeisen amfetamiinin käytön jälkeen (mikä on vähemmän kuin amfetamiinirasemaatilla). Dekstroamfetamiinimetaboliittien havaitsemisjakso hiuksissa on enintään 2,5-3 kuukautta.
Last edited:
