Reaktiot Grignard-reagensseilla.
Grignard-reagenssin kaava on RMgX, jossa X on halogeeni ja R on alkyyli- tai aryyliryhmä (bentseenirenkaaseen perustuva). Tässä aiheessa R:n katsotaan olevan alkyyliryhmä (esim. BuMgBr). Grignard-reagensseja valmistetaan lisäämällä halogeenialkaania pieniin magnesiumpaloihin kolvissa, joka sisältää dietyylieetteriä. Pullo varustetaan takaisinvirtauskondensaattorilla, ja seosta lämmitetään vesihauteessa 20-30 minuuttia.
Kaiken on oltava täysin kuivaa, koska Grignard-reagenssit reagoivat veden kanssa (ks. jäljempänä). Kaikki reaktiot, joissa käytetään Grignard-reagenssia, tehdään tässä reaktiossa syntyneellä seoksella. Sitä ei voi erottaa millään tavalla.
Grignard-reagenssit ja vesi.
Grignard-reagenssit reagoivat veden kanssa tuottaen alkaaneja. Tästä syystä kaiken on oltava hyvin kuivaa edellä mainitun valmistuksen aikana. Esim:Epäorgaanista tuotetta, Mg(OH)Br, kutsutaan "emäksiseksi bromidiksi", ja se on eräänlainen magnesiumbromidin ja magnesiumhydroksidin välivaihe.
Grignardien ja karbonyylien välinen yleinen reaktio.
Erilaisten karbonyyliyhdisteiden ja Grignard-reagenssien väliset reaktiot voivat näyttää melko monimutkaisilta, mutta itse asiassa ne kaikki reagoivat samalla tavalla - ainoastaan hiili-happi-kaksoissidokseen kiinnittyneet ryhmät muuttuvat. On paljon helpompaa ymmärtää, mitä tapahtuu, kun tarkastellaan tarkasti yleistä tapausta (käyttämällä "R"-ryhmiä erityisten ryhmien sijasta) - ja sitten lisätään erilaisia todellisia ryhmiä tarpeen mukaan.
Reaktiot ovat periaatteessa samanlaisia kuin hiilidioksidin kanssa tapahtuva reaktio - ainoastaan orgaanisen tuotteen luonne eroaa. Ensimmäisessä vaiheessa Grignard-reagenssi lisää hiili-happi-kaksoissidoksen yli.
Reaktiot ovat periaatteessa samanlaisia kuin hiilidioksidin kanssa tapahtuva reaktio - ainoastaan orgaanisen tuotteen luonne eroaa. Ensimmäisessä vaiheessa Grignard-reagenssi lisää hiili-happi-kaksoissidoksen yli.
Tämän jälkeen siihen lisätään laimeaa happoa hydrolyysin aikaansaamiseksi. (Käytän tavallisesti hyväksyttyä yhtälöä, enkä ota huomioon sitä, että Mg(OH)Br reagoi edelleen hapon kanssa).
Syntyy alkoholia. Yksi Grignard-reagenssien tärkeimmistä käyttökohteista on kyky valmistaa monimutkaisia alkoholeja helposti. Se, minkälaista alkoholia saadaan, riippuu siitä, mistä karbonyyliyhdisteestä lähdettiin liikkeelle - toisin sanoen siitä, mitä R ja R' ovat.
Grignard-reagensseja käytetään laajalti erilaisten orgaanisten yhdisteiden synteesissä. Seuraavassa esitetään joitakin esimerkkejä.
:
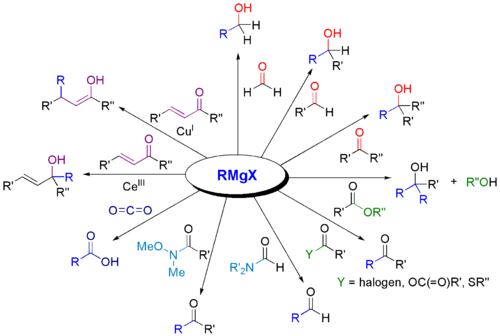
kanssa:
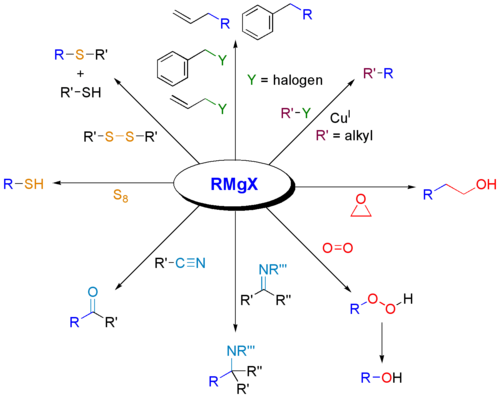
MiksiGrignard-reagenssit reagoivat karbonyylien kanssa?
Hiiliatomin ja magnesiumin välinen sidos on polaarinen. Hiili on elektronegatiivisempi kuin magnesium, joten sidoselektronipari vetäytyy hiiltä kohti. Näin hiiliatomiin jää hieman negatiivinen varaus.
Hiilen ja hapen kaksoissidos on myös erittäin polaarinen, ja hiiliatomilla on huomattava määrä positiivista varausta. Grignard-reagenssi voi näin ollen toimia nukleofiilinä, koska Grignard-reagenssin hiiliatomin lievästi negatiivinen varaus ja karbonyyliyhdisteen hiilen positiivinen varaus vetävät toisiaan puoleensa. Nukleofiili on negatiivinen (tai hieman negatiivinen) atomi, joka hyökkää muiden molekyylien tai ionien positiivisiin (tai hieman positiivisiin) keskuksiin.
Grignard-reagenssin, fenyylimagnesiumbromidin, valmistus.
Grignard-reagensseilla on hallitseva rooli orgaanisessa synteesissä. Näitä yhdisteitä voidaan mukauttaa monenlaisten funktionaalisten ryhmien valmistukseen, ja orgaanisten magnesiumjohdannaisten muodostaminen ja reagointi on yksi alkyylihalogenidien tärkeimmistä käyttökohteista orgaanisessa synteesissä. Halogenidin ja magnesiumin reaktio tapahtuu metallin pinnalla ja on muodollisesti metallin hapettumista. Reaktio suoritetaan yleensä kuivassa eetteriliuottimessa, jossa eetteri toimii Lewisin emäksinä liuottamalla Grignard-reagenssin ja sallimalla sen diffundoitua pois metallista. Metalliorgaanisen reagenssin muodostuminen edellyttää aktiivista pintaa metallissa, ja reaktion käynnistäminen voi olla hieman vaikeaa metallipinnalla olevien metallioksidien vuoksi. Magnesiumin jauhaminen laastissa muutaman minuutin ajan ennen käyttöä on usein tehokas keino saada puhdas pinta. Toinen hyödyllinen temppu reaktion käynnistämisessä on pienen jodikiteen lisääminen seokseen, joka reagoi magnesiumin kanssa muodostaen erittäin reaktiivisen magnesiumjodidin (MgI2) suolan.
Menettely.
Grignard-reagenssi valmistetaan varustamalla ensin kuiva 250 ml:n pyöreäpohjainen pullo CaCl2-kuivausputkella. Käyttökelpoinen magnesium (2 g = 0,082 moolia magnesiumkääntymiä) laitetaan kolviin, kalsiumkloridiputki kiinnitetään suoraan ja kolvi kuumennetaan perusteellisesti suurella kuumennusmanteli- ja reostaattikammiolla. Säädetään suuren kuumennusmantelin säädin asetukseen "6" ja kuumennetaan kolvia, kunnes se on liian kuuma sormella kosketettavaksi. Jäähdytettäessä kolvi kerää kuivaa ilmaa kalsiumkloridin läpi. Poista lämmitysmanteli ja jäähdytä pullo huoneenlämpöiseksi (pullon pitäisi tuntua kädessäsi vain hieman lämpimältä tai viileämmältä), ennen kuin jatkat. Poista kalsiumkloridin kuivausputki ja kaada 250 pyöreäpohjaiseen pulloon 15 ml absoluuttista eetteriä ja 9 ml (13,5 g = 0,086 moolia) bromibentseeniä. Aseta CaCl2-kuivausputki takaisin paikoilleen. Jos reaktio ei näy välittömästi, käynnistetään reaktio murskaamalla osa magnesiumkääntöpaloista. Tämä tehdään asettamalla kuiva sekoitussauva, jossa on litteä pää, ja murskaamalla varovasti magnesiumpala lujasti kolvin pohjaa vasten nesteen pinnan alle, jolloin sauva tekee kiertoliikkeen. Kun tämä tehdään oikein, neste muuttuu hieman sameaksi, ja puristetun metallin pinnalla alkaa nopea kuplinta. Tässä vaiheessa lisätään vielä 25 ml absoluuttista eetteriä ja kiinnitetään takaisinvirtauskondensaattori kolviin ja CaCl2-putki takaisinvirtauskondensaattorin yläosaan kuvan osoittamalla tavalla.
Älä aloita veden juoksuttamista lauhduttimen läpi ennen kuin eetterihöyryt ovat kostuttaneet lauhduttimen yläosassa olevan liitoksen. Jäähdytä tarvittaessa kolvi koskettamalla kolvin pohjaa jäähauteella reaktion hidastamiseksi, mutta älä käytä sitä, ellei se ole välttämätöntä. Se on tarpeen vain, jos eetterihöyryjä poistuu kuivausputken yläosasta. Jos reaktiota joudutaan jäähdyttämään, on varottava hidastamasta reaktiota liikaa, sillä se voi pysähtyä eikä käynnistyä uudelleen, kun jää poistetaan. Pyöritä kolvia voimakkaasti 60 sekunnin välein. Kun reaktio alkaa, laimennetun seoksen spontaani kiehuminen voi olla hidasta tai muuttua hitaaksi. Jos näin on, lisätään kolviin muutama ml lisää bromibentseeniä. Reaktio on valmis, kun eetteri lakkaa kuplimasta ja jäljelle jää vain muutamia pieniä metallijäämiä. Merkitään pullon eetteritaso. Tarkista reaktion aikana, että eetterin määrä ei ole vähentynyt. Jos on, lisätään lisää kuivaa eetteriä. KoskaGrignard-reagenssin liuos heikkenee seistessään, seuraava vaihe on aloitettava heti.
Grignard-reagenssin ja metyylibentsoaatin kondensaatio.
Grignard-reagenssin ja metyylibentsoaatin kondensaatio.
Sekoitetaan 5 g (0,037 moolia; 1,09 g/ml) metyylibentsoaattia ja 15 ml absoluuttista eetteriä erotussuppilossa, jäähdytetään Grignard-reagenssiliuosta sisältävää kolvia lyhyesti jäähauteessa. Poista kuivausputki ja aseta Claisenin sovitin ja erotussuppilo lauhduttimen yläosaan oikealla esitetyllä tavalla. Juoksutetaan metyylibentsoaattiliuosta pisaroittain kymmenen minuutin ajan ja jäähdytetään vain sen verran, mitä tarvitaan eksotermisen reaktion hallitsemiseksi. Tuotesuola erottuu valkoisena kiinteänä aineena tämän vaiheen aikana. Pyöritellään kolvia säännöllisin väliajoin, kunnes reaktio on laantunut ja kolvi on huoneenlämmössä. Siirry suoraan seuraavaan vaiheeseen.
Additiotuotteen hydrolyysi.
Additiotuotteen hydrolyysi.
Kaadetaan reaktioseos varovasti 250 ml:n Erlenmeyer-pulloon, jossa on 50 ml 10 %:n rikkihappoa ja noin 25 g jäätä. Huuhtele reaktiopullo muutamalla millilitralla tavallista (vedetöntä) eetteriä ja muutamalla millilitralla 10-prosenttista rikkihappoa. Lisää nämä huuhtelut Erlenmeyer-kolviin. Pyöritellään hyvin lisäyhdisteen hydrolyysin edistämiseksi; emäksiset magnesiumsuolat muuttuvat vesiliukoisiksi neutraaleiksi suoloiksi ja trifenyylikarbinoli jakautuu eetterikerrokseen. Saatetaan tarvita lisämäärä eetteriä (tavallista), jos alkuperäinen eetterikerros on haihtumisen vuoksi jäänyt liian pieneksi. Voit lopettaa tässä vaiheessa, jos aika ei riitä seuraavan osan suorittamiseen. Säilytä merkitty Erlenmeyer-astia hupussa, jossa on kevyesti asennettu korkki (ei kumitulppa). Tulpan on oltava riittävän löysä, jotta kehittyvän vetykaasun aiheuttama kaasunpaine vapautuu.
Kun kuluttamaton Mg-metalli joutuu kosketuksiin hapon kanssa, vetykaasua kehittyy voimakkaasti, ja reaktioseos voi vaahdota, jos lisäys tapahtuu liian nopeasti.
Tuotteen eristäminen.
Jos eetterikerroksessasi on kiinteitä valkoisia kiteitä, nämä tuotekiteet ovat muodostuneet siksi, että osa eetterikerroksesta on haihtunut. Nämä kiteet voidaan eristää kaatamalla seos erotussuppiloon lasisuppilon läpi, jonka varteen on asetettu pieni lasivillatulppa. Kiteet huuhdellaan pienellä määrällä eetteriliuotinta. Jäljelle jäävän tuotteen eristämiseksi huuhtele Erlenmeyer-pullo, josta kaadoit alkuperäisen liuoksen, muutamalla millilitralla tavallista eetteriä ja lisää se erotussuppiloon. Ravista suppiloa varovasti ja varmista, että suppiloon kertynyt kaasu poistetaan. Vedetään vesikerros pois. Ravistetaan eetterikerrosta 10-prosenttisella rikkihapolla magnesiumsuolojen poistamiseksi edelleen ja poistetaan rikkihappokerros. Pestään eetterikerros kyllästetyllä natriumkloridiliuoksella eetteriin liuenneen veden poistamiseksi. Poista natriumkloridiliuos. Näissä pesuissa käytettävät nestemäärät eivät ole kriittisiä. Yleensä pesunesteen määrä, joka vastaa yhtä kolmasosaa eetterin tilavuudesta, on riittävä. Eetteriliuoksen lopullista kuivausta varten kaadetaan eetterikerros erotussuppilon kaulasta Erlenmeyer-kolviin, lisätään noin 5 g rakeista vedetöntä natriumsulfaattia, sekoitetaan kolvia aika ajoin ja dekantoidaan eetteri kiinteästä kuiva-aineesta 5 minuutin kuluttua toiseen puhtaaseen, kuivaan Erlenmeyer-kolviin. Eetteriliuokseen lisätään 25 ml ligroiinia ja pullo suljetaan korkilla. Anna seoksen seistä yön yli tai seuraavaan laboratoriojaksoon asti. Seisonnan jälkeen trifenyylikarbinolin kiteiden pitäisi olla muodostuneet. Pääepäpuhtauden bifenyylin pitäisi jäädä liukenemaan uudelleenkiteytysliuottimeen. Kiteet suodatetaan imusuodatuksella, kunnes ne ovat kuivia. Merkitään ylös eristetyn tuotteen paino ja lasketaan saantoprosentti. Mitataan sulamispiste.
Kun kuluttamaton Mg-metalli joutuu kosketuksiin hapon kanssa, vetykaasua kehittyy voimakkaasti, ja reaktioseos voi vaahdota, jos lisäys tapahtuu liian nopeasti.
Tuotteen eristäminen.
Jos eetterikerroksessasi on kiinteitä valkoisia kiteitä, nämä tuotekiteet ovat muodostuneet siksi, että osa eetterikerroksesta on haihtunut. Nämä kiteet voidaan eristää kaatamalla seos erotussuppiloon lasisuppilon läpi, jonka varteen on asetettu pieni lasivillatulppa. Kiteet huuhdellaan pienellä määrällä eetteriliuotinta. Jäljelle jäävän tuotteen eristämiseksi huuhtele Erlenmeyer-pullo, josta kaadoit alkuperäisen liuoksen, muutamalla millilitralla tavallista eetteriä ja lisää se erotussuppiloon. Ravista suppiloa varovasti ja varmista, että suppiloon kertynyt kaasu poistetaan. Vedetään vesikerros pois. Ravistetaan eetterikerrosta 10-prosenttisella rikkihapolla magnesiumsuolojen poistamiseksi edelleen ja poistetaan rikkihappokerros. Pestään eetterikerros kyllästetyllä natriumkloridiliuoksella eetteriin liuenneen veden poistamiseksi. Poista natriumkloridiliuos. Näissä pesuissa käytettävät nestemäärät eivät ole kriittisiä. Yleensä pesunesteen määrä, joka vastaa yhtä kolmasosaa eetterin tilavuudesta, on riittävä. Eetteriliuoksen lopullista kuivausta varten kaadetaan eetterikerros erotussuppilon kaulasta Erlenmeyer-kolviin, lisätään noin 5 g rakeista vedetöntä natriumsulfaattia, sekoitetaan kolvia aika ajoin ja dekantoidaan eetteri kiinteästä kuiva-aineesta 5 minuutin kuluttua toiseen puhtaaseen, kuivaan Erlenmeyer-kolviin. Eetteriliuokseen lisätään 25 ml ligroiinia ja pullo suljetaan korkilla. Anna seoksen seistä yön yli tai seuraavaan laboratoriojaksoon asti. Seisonnan jälkeen trifenyylikarbinolin kiteiden pitäisi olla muodostuneet. Pääepäpuhtauden bifenyylin pitäisi jäädä liukenemaan uudelleenkiteytysliuottimeen. Kiteet suodatetaan imusuodatuksella, kunnes ne ovat kuivia. Merkitään ylös eristetyn tuotteen paino ja lasketaan saantoprosentti. Mitataan sulamispiste.
Psykoaktiivisten aineiden synteesit Grignard-reagenssin avulla.
Grignard-reagenssia käytetään useiden pinta-aktiivisten aineiden synteesissä. Esimerkiksi synteettisten kannabinoidien synteesissä alkyyliryhmän kiinnittämiseksi indolin typpiatomiin (ks. synteesiesimerkki JWH-018 ). Reaktio etenee melko nopeasti miedoissa olosuhteissa eikä vaadi kuumennusta.
Grignard-reagenssin nukleofiilinen lisäys mahdollistaa jonkin verran epäspesifistä ja stereospesifistä reaktiota amfetamiinin ja sen esiasteen, kuten fenyyli-2-propanonin (P2P),tuottamiseksi .
Toinen Grignard-reagenssin käyttötapa on käyttö mefedronin (4-MMC) synteesissä käyttämällä 4-metyylibentsaldehydiä lähtöaineena.
Indolymagnesiumjodidin reagointi substituoitujen alkyylihalogenidien, esim. nitriilien Cl(CH2)nCN ja klooriasetyylidietyyliamidin, kanssa vastaavien 3-substituoitujen indolien saamiseksi on hyvin tunnettu, vaikka hyvin reaktiiviset halogenidit, kuten metyylijodidi ja bentsyylikloridi, antavat joskus 1,3-disubstituoituja indoleja. Tämä DMT-reitti on mahdollinen Grignard-reagenssin avulla.
Edellisten erilaisten sovellusten lisäksi tätä suosittua lähestymistapaa hyödynnetään (o-kloorifenyyli)-syklopentyyliketonin valmistuksen ketamiinisynteesivaiheessa.
Johtopäätös.
Kuten näette, Grignard-reagenssia käytetään laajasti orgaanisissa synteeseissä ja lääkkeiden valmistuksessa osittain. Alkyylimagnesiumhalogenidit (joita kutsutaan myös Grignard-reagensseiksi) toimivat nukleofiileinä, jotka hyökkäävät elektrofiilisen hiiliatomin kimppuun muodostaen hiili-hiilisidoksen. Grignardin reaktio on tärkeä menetelmä hiili-hiilisidosten sekä hiili-heteroatomisidosten luomiseksi. Tämä luettelo salakemistien suosituimmista reaktioista osoittaa Grignard-reagenssien valtavan potentiaalin ja muodostaa laajan tutkimusalueen.
Last edited:
