- Joined
- Apr 29, 2023
- Messages
- 78
- Reaction score
- 44
- Points
- 18
PPA HYPOPHOSPHORE ET IODE =D AMPHÉTAMINE OU L'UTILISER POUR FABRIQUER DU 4 MÉTHYLAMINOREX
Informations debaseSécuritéPrixUtilisationPréparationProduits et matièrespremièresSpectreLié

ChemicalBook CAS DataBase List Phenylpropanolamine
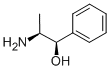
La phénylpropanolamine (PPA) est une amine sympathomimétique à action mixte similaire à l'éphédrine. Son principal mécanisme d'action est l'agonisme a-adrénergique direct, mais il existe également une stimulation indirecte de la libération de norépinéphrine. En novembre 2000, le comité consultatif sur les médicaments en vente libre de la Food and Drug Administration (FDA) des États-Unis a établi qu'il existait un lien significatif entre le PPA et les accidents vasculaires cérébraux hémorragiques et a recommandé que le PPA ne soit pas considéré comme sûr pour une utilisation en vente libre. Une lettre a alors été envoyée aux fabricants pour leur demander de retirer volontairement le PPA de leurs produits. Plus tard, en 2005, la FDA a publié une monographie finale provisoire pour les produits contenant du PPA, proposant le statut de catégorie II (généralement non reconnu comme sûr et efficace). À ce jour, aucune monographie finale n'a été publiée, mais tous les fabricants ont retiré le PPA de leurs produits.
Origine
Propadrine, MSD ,US ,1941
Utilisation
La noréphédrine, également appelée phénylpropanolamine (PPA), est une forme synthétique de l'alcaloïde éphédrine. Utilisée dans le traitement de l'incontinence urinaire chez les chiens et les chats ; décongestionnant nasal. Après des rapports faisant état d'hémorragies intracrâniennes et d'autres effets indésirables, dont plusieurs décès, le PPA n'est plus vendu aux États-Unis et au Canada.
Utilisations
Excitation nerveuse centrale
Utilisations
Le PPA était utilisé comme décongestionnant nasal et comme anorexigène. Des études ont montré un bénéfice chez l'homme pour l'incontinence urinaire, et le PPA est toujours utilisé en médecine vétérinaire à cette fin.
Définition
ChEBI : (-)-norephedrine est une amphétamine qui est un propylbenzène substitué par un groupe hydroxy en position 1 et par un groupe amino en position 2 (le stéréo-isomère 1R,2S). Il s'agit d'un alcaloïde végétal. Elle joue un rôle en tant que métabolite végétal. Elle fait partie des amphétamines et est un alcaloïde de la phénéthylamine.
Procédé de fabrication
Selon l'une des méthodes décrites dans le brevet américain 2,151,517, 10,7 kg de benzaldéhyde technique sont vigoureusement agités avec une solution de 11,0 kg de bisulfite de sodium dans 50,0 litres d'eau jusqu'à ce que la formation du produit d'addition soit complète. Simultanément, 8,25 kg de nitroéthane sont dissous dans une solution de 4,5 kg de soude caustique dans 20,0 litres d'eau et la solution chaude qui en résulte est ajoutée au magma de bisulfite de sodium benzaldéhyde sous forte agitation. Le mélange est agité pendant 30 minutes, puis laissé au repos pendant une nuit.
La partie aqueuse du mélange est alors retirée de la couche surnageante de phénylnitropropanol huileux et remplacée par une solution fraîche de 11,0 kg de bisulfite de sodium dans 50,0 litres d'eau. Le mélange de phénylnitropropanol et de solution de bisulfite est alors vigoureusement agité pendant 15 minutes afin d'éliminer et de récupérer de petites quantités de benzaldéhyde n'ayant pas réagi, puis on le laisse à nouveau se stratifier. Cette fois, le phénylnitropropanol est siphonné et filtré pour éliminer une petite quantité de matière résineuse. La solution aqueuse de bisulfite de sodium restante est mise à réagir avec le benzaldéhyde, comme décrit ci-dessus, ce qui rend le processus continu.
Le 1-phényl-2-nitropropanol ainsi obtenu est une huile incolore, d'une densité de 1,14 à 20°C, inodore à l'état pur, volatile à la vapeur et dont le point d'ébullition se situe entre 150° et 165°C sous une pression de 5 mm de mercure. Elle est soluble dans l'alcool, l'éther, l'acétone, le chloroforme, le tétrachlorure de carbone, le benzène et l'acide acétique glacial. Le rendement du 1-phényl-2-nitropropanol obtenu par cette procédure est de 17,1 à 17,7 kg.
Il est hydrogéné et converti en chlorhydrate dans les étapes suivantes. Le chlorure d'hydrogène a un point de fusion de 192°-194°C.
Selon une autre méthode décrite dans le brevet américain 3,028,429, le propiophénone peut réagir avec un nitrite d'alkyle pour donner de l'isonitrosopropiophénone qui est ensuite hydrogénée et finalement convertie en chlorhydrate.
nom de marque
Par exemplemultix ; Acutrim ; Adistop-f ; Amertuss ; Amplisiex ; Am-tuss liq ; Anorexin ; Antiadipositum ; Apoephedrin ; e Aridose ; Arm ; Bifed-20 ; Biphetane ; Biphetap ; Blu-hist ; Brocon cr ; Bromanate ; Bromepaph ;Brometapp;Bronco-quintoxil;Cenadex;Chlor-rest;Cinturex;Cletanol;Codimal;Cofpac;Cold cap;Coldecon;Col-decon;Conex-grippe;Contop;Coricidin f;Corsym;Coryztime;Cremacoat ;Dalca ; Decidex ; Decomine ; Demazine ; Deprecstop ; Dexatrim ; D-sinus ; Efed ii ; Eficol ; Endal ; Endecon ; Endex ; E-son ; Espornade spansule ; E-tapp 3 ; Exyphen ; Factus ; Fornagest ; Fugoa n ; Gardax ;Ginsopan;Headway;Histade;Histatapp;Hsp 540;Ipercron;Kol-tac;Kontexin;Koryza;Leder;Lipo-sinahist;Lunerin;Mardram;Minus-x;Monatuss;Mucolyt-expecto;Nd-hist;Nectatussin ;Neosoldana;Nexaam;Nobese;Norephedrine;Nornatane;Ornacol;Ornatos;Ornex;Pabron nose;Panacorn;Panadyl;Parhist;Partapp;Pholcolix spansule;Pneumidex;Polcimut;Profenade ;Propagest;Reduzin;Rhindecon;Rhinergal;Rhinervert;Rhinicept;Rhinidrin;Rhinocap;Rinexin;Rinomar;Rinotussal;Rinurel lictus;Rinurel comprimés;Rinutan;Rotabromophen;Rupton;Rynatapp ;Rynex;Ryza-gesic;Sacietyl;Scotuss;Secron;Sinacin;Sinudan;Sinu-lets;Sinutab cough l;Spandecon;Srda;Sto-caps;Sulfa-probocon;Symptrol;Taviset;Tinaroc;Totolin;Tricon;Tri-congestic ;Triogesic elixir;Triominic;Triotussic;Turbispan;Tussilene-dm;V cold;Veltane;Veltap;Vernate;Vistaminic;Voxin-pg;W 58;X 112 antiadipo;Zerinol;Partuss;Permatrim;Phenapap.
Fonction thérapeutique
Décongestionnant nasal, Anorexique
Organisation mondiale de la santé (OMS)
La phénylpropanolamine, une amine symopathomimétique, est largement disponible dans les préparations en vente libre depuis 1941. C'est l'un des décongestionnants nasaux les plus fréquemment utilisés et un ingrédient courant des préparations destinées à réduire le poids, bien que des doutes aient été émis quant à son utilité dans cette indication. Il est également utilisé pour traiter l'incontinence d'effort. Son utilisation a été associée à une élévation excessive occasionnelle de la pression artérielle, en particulier chez les personnes hypersensibles.
Description générale
La phénylpropanolamine est le N-desméthylanalogue de l'éphédrine et possède donc de nombreuses propriétés similaires. Sans le groupe N-méthyle, la phénylpropanolamine est légèrement plus polaire et ne pénètre donc pas dans le SNC aussi bien que l'éphédrine. Cette modification donne un agent qui a une action vasopressive légèrement plus élevée et une action stimulante centrale plus faible que l'éphédrine. Son action en tant que décongestionnant nasal est plus prolongée que celle de l'éphédrine. La phénylpropanolamine était un composant actif courant des coupe-faim et des médicaments contre la toux et le rhume jusqu'en 2001, date à laquelle la Food and Drug Administration (FDA) a recommandé son retrait de ces médicaments, car des études ont révélé un risque accru d'accident vasculaire cérébral hémorragique chez les jeunes femmes qui prenaient ce médicament.
Profil de sécurité
Modérément toxique par voie sous-cutanée. Lorsqu'il est chauffé jusqu'à décomposition, il émet des fumées très toxiques de NOx.
Évaluation de la toxicité
L'action principale du PPA est l'agonisme a-adrénergique direct, bien qu'il provoque également une libération indirecte de norépinéphrine au niveau des terminaisons nerveuses sympathiques postganglionnaires. Le PPA possède également de faibles propriétés agonistes β. L'hypertension résulte d'une vasoconstriction des vaisseaux sanguins périphériques à médiation α-adrénergique. La bradycardie réflexe est fréquente. Les effets sympathomimétiques peuvent produire de l'anxiété, de l'insomnie, de l'agitation, des tremblements, de la tachycardie et de la mydriase.
MSDS|CAS|CASDataBase|Nouveauxproduits
Contactez-nous|Versioninformatique
Livre de produits chimiques
Informations debaseSécuritéPrixUtilisationPréparationProduits et matièrespremièresSpectreLié

ChemicalBook CAS DataBase List Phenylpropanolamine

Phénylpropanolamine
- Nom du produitPhénylpropanolamine
- CAS14838-15-4
- Numéro CBNCB22131029
- MFC9H13NO
- MW151.21
- EINECS238-900-2
- Fichier MOL14838-15-4.mol
Propriétés chimiques
| Point de fusion | 101-101.5° |
| Point d'ébullition | 273,23°C (estimation approximative) |
| Densité | 1,0406 (estimation approximative) |
| Indice de réfraction | 1,5380 (estimation) |
| pka | pKa 9.19(H2O,t =25±0.5,I=0.01)(approximatif) |
| couleur | Plaques de H2O |
| FDA UNII | 33RU150WUN |
| Référence chimique NIST | Benzenemethanol, «alpha»-(1-aminoethyl)-, (r*,s*)-(.+/-.)-(14838-15-4) |
| Code ATC | R01BA01,R01BA51 |
| Système d'enregistrement des substances de l'EPA | Phenylpropanolamine (14838-15-4) |
Sécurité
| Données sur les substances dangereuses | 14838-15-4(Données sur les substances dangereuses) |
| Toxicité | LD50 scu-rat : 850 mg/kg JPETAB 85,199,45 |
Prix de la phénylpropanolamine
Propriétés chimiques de la phénylpropanolamine, utilisation, production
Description de la substanceLa phénylpropanolamine (PPA) est une amine sympathomimétique à action mixte similaire à l'éphédrine. Son principal mécanisme d'action est l'agonisme a-adrénergique direct, mais il existe également une stimulation indirecte de la libération de norépinéphrine. En novembre 2000, le comité consultatif sur les médicaments en vente libre de la Food and Drug Administration (FDA) des États-Unis a établi qu'il existait un lien significatif entre le PPA et les accidents vasculaires cérébraux hémorragiques et a recommandé que le PPA ne soit pas considéré comme sûr pour une utilisation en vente libre. Une lettre a alors été envoyée aux fabricants pour leur demander de retirer volontairement le PPA de leurs produits. Plus tard, en 2005, la FDA a publié une monographie finale provisoire pour les produits contenant du PPA, proposant le statut de catégorie II (généralement non reconnu comme sûr et efficace). À ce jour, aucune monographie finale n'a été publiée, mais tous les fabricants ont retiré le PPA de leurs produits.
Origine
Propadrine, MSD ,US ,1941
Utilisation
La noréphédrine, également appelée phénylpropanolamine (PPA), est une forme synthétique de l'alcaloïde éphédrine. Utilisée dans le traitement de l'incontinence urinaire chez les chiens et les chats ; décongestionnant nasal. Après des rapports faisant état d'hémorragies intracrâniennes et d'autres effets indésirables, dont plusieurs décès, le PPA n'est plus vendu aux États-Unis et au Canada.
Utilisations
Excitation nerveuse centrale
Utilisations
Le PPA était utilisé comme décongestionnant nasal et comme anorexigène. Des études ont montré un bénéfice chez l'homme pour l'incontinence urinaire, et le PPA est toujours utilisé en médecine vétérinaire à cette fin.
Définition
ChEBI : (-)-norephedrine est une amphétamine qui est un propylbenzène substitué par un groupe hydroxy en position 1 et par un groupe amino en position 2 (le stéréo-isomère 1R,2S). Il s'agit d'un alcaloïde végétal. Elle joue un rôle en tant que métabolite végétal. Elle fait partie des amphétamines et est un alcaloïde de la phénéthylamine.
Procédé de fabrication
Selon l'une des méthodes décrites dans le brevet américain 2,151,517, 10,7 kg de benzaldéhyde technique sont vigoureusement agités avec une solution de 11,0 kg de bisulfite de sodium dans 50,0 litres d'eau jusqu'à ce que la formation du produit d'addition soit complète. Simultanément, 8,25 kg de nitroéthane sont dissous dans une solution de 4,5 kg de soude caustique dans 20,0 litres d'eau et la solution chaude qui en résulte est ajoutée au magma de bisulfite de sodium benzaldéhyde sous forte agitation. Le mélange est agité pendant 30 minutes, puis laissé au repos pendant une nuit.
La partie aqueuse du mélange est alors retirée de la couche surnageante de phénylnitropropanol huileux et remplacée par une solution fraîche de 11,0 kg de bisulfite de sodium dans 50,0 litres d'eau. Le mélange de phénylnitropropanol et de solution de bisulfite est alors vigoureusement agité pendant 15 minutes afin d'éliminer et de récupérer de petites quantités de benzaldéhyde n'ayant pas réagi, puis on le laisse à nouveau se stratifier. Cette fois, le phénylnitropropanol est siphonné et filtré pour éliminer une petite quantité de matière résineuse. La solution aqueuse de bisulfite de sodium restante est mise à réagir avec le benzaldéhyde, comme décrit ci-dessus, ce qui rend le processus continu.
Le 1-phényl-2-nitropropanol ainsi obtenu est une huile incolore, d'une densité de 1,14 à 20°C, inodore à l'état pur, volatile à la vapeur et dont le point d'ébullition se situe entre 150° et 165°C sous une pression de 5 mm de mercure. Elle est soluble dans l'alcool, l'éther, l'acétone, le chloroforme, le tétrachlorure de carbone, le benzène et l'acide acétique glacial. Le rendement du 1-phényl-2-nitropropanol obtenu par cette procédure est de 17,1 à 17,7 kg.
Il est hydrogéné et converti en chlorhydrate dans les étapes suivantes. Le chlorure d'hydrogène a un point de fusion de 192°-194°C.
Selon une autre méthode décrite dans le brevet américain 3,028,429, le propiophénone peut réagir avec un nitrite d'alkyle pour donner de l'isonitrosopropiophénone qui est ensuite hydrogénée et finalement convertie en chlorhydrate.
nom de marque
Par exemplemultix ; Acutrim ; Adistop-f ; Amertuss ; Amplisiex ; Am-tuss liq ; Anorexin ; Antiadipositum ; Apoephedrin ; e Aridose ; Arm ; Bifed-20 ; Biphetane ; Biphetap ; Blu-hist ; Brocon cr ; Bromanate ; Bromepaph ;Brometapp;Bronco-quintoxil;Cenadex;Chlor-rest;Cinturex;Cletanol;Codimal;Cofpac;Cold cap;Coldecon;Col-decon;Conex-grippe;Contop;Coricidin f;Corsym;Coryztime;Cremacoat ;Dalca ; Decidex ; Decomine ; Demazine ; Deprecstop ; Dexatrim ; D-sinus ; Efed ii ; Eficol ; Endal ; Endecon ; Endex ; E-son ; Espornade spansule ; E-tapp 3 ; Exyphen ; Factus ; Fornagest ; Fugoa n ; Gardax ;Ginsopan;Headway;Histade;Histatapp;Hsp 540;Ipercron;Kol-tac;Kontexin;Koryza;Leder;Lipo-sinahist;Lunerin;Mardram;Minus-x;Monatuss;Mucolyt-expecto;Nd-hist;Nectatussin ;Neosoldana;Nexaam;Nobese;Norephedrine;Nornatane;Ornacol;Ornatos;Ornex;Pabron nose;Panacorn;Panadyl;Parhist;Partapp;Pholcolix spansule;Pneumidex;Polcimut;Profenade ;Propagest;Reduzin;Rhindecon;Rhinergal;Rhinervert;Rhinicept;Rhinidrin;Rhinocap;Rinexin;Rinomar;Rinotussal;Rinurel lictus;Rinurel comprimés;Rinutan;Rotabromophen;Rupton;Rynatapp ;Rynex;Ryza-gesic;Sacietyl;Scotuss;Secron;Sinacin;Sinudan;Sinu-lets;Sinutab cough l;Spandecon;Srda;Sto-caps;Sulfa-probocon;Symptrol;Taviset;Tinaroc;Totolin;Tricon;Tri-congestic ;Triogesic elixir;Triominic;Triotussic;Turbispan;Tussilene-dm;V cold;Veltane;Veltap;Vernate;Vistaminic;Voxin-pg;W 58;X 112 antiadipo;Zerinol;Partuss;Permatrim;Phenapap.
Fonction thérapeutique
Décongestionnant nasal, Anorexique
Organisation mondiale de la santé (OMS)
La phénylpropanolamine, une amine symopathomimétique, est largement disponible dans les préparations en vente libre depuis 1941. C'est l'un des décongestionnants nasaux les plus fréquemment utilisés et un ingrédient courant des préparations destinées à réduire le poids, bien que des doutes aient été émis quant à son utilité dans cette indication. Il est également utilisé pour traiter l'incontinence d'effort. Son utilisation a été associée à une élévation excessive occasionnelle de la pression artérielle, en particulier chez les personnes hypersensibles.
Description générale
La phénylpropanolamine est le N-desméthylanalogue de l'éphédrine et possède donc de nombreuses propriétés similaires. Sans le groupe N-méthyle, la phénylpropanolamine est légèrement plus polaire et ne pénètre donc pas dans le SNC aussi bien que l'éphédrine. Cette modification donne un agent qui a une action vasopressive légèrement plus élevée et une action stimulante centrale plus faible que l'éphédrine. Son action en tant que décongestionnant nasal est plus prolongée que celle de l'éphédrine. La phénylpropanolamine était un composant actif courant des coupe-faim et des médicaments contre la toux et le rhume jusqu'en 2001, date à laquelle la Food and Drug Administration (FDA) a recommandé son retrait de ces médicaments, car des études ont révélé un risque accru d'accident vasculaire cérébral hémorragique chez les jeunes femmes qui prenaient ce médicament.
Profil de sécurité
Modérément toxique par voie sous-cutanée. Lorsqu'il est chauffé jusqu'à décomposition, il émet des fumées très toxiques de NOx.
Évaluation de la toxicité
L'action principale du PPA est l'agonisme a-adrénergique direct, bien qu'il provoque également une libération indirecte de norépinéphrine au niveau des terminaisons nerveuses sympathiques postganglionnaires. Le PPA possède également de faibles propriétés agonistes β. L'hypertension résulte d'une vasoconstriction des vaisseaux sanguins périphériques à médiation α-adrénergique. La bradycardie réflexe est fréquente. Les effets sympathomimétiques peuvent produire de l'anxiété, de l'insomnie, de l'agitation, des tremblements, de la tachycardie et de la mydriase.
Produits de préparation et matières premières
Matières premièresSpectre de la phénylpropanolamine
14838-15-4, PhénylpropanolamineRecherche connexe
Envoyer une demandeMSDS|CAS|CASDataBase|Nouveauxproduits
Contactez-nous|Versioninformatique
Livre de produits chimiques
