- Joined
- Dec 27, 2022
- Messages
- 30
- Reaction score
- 81
- Points
- 18
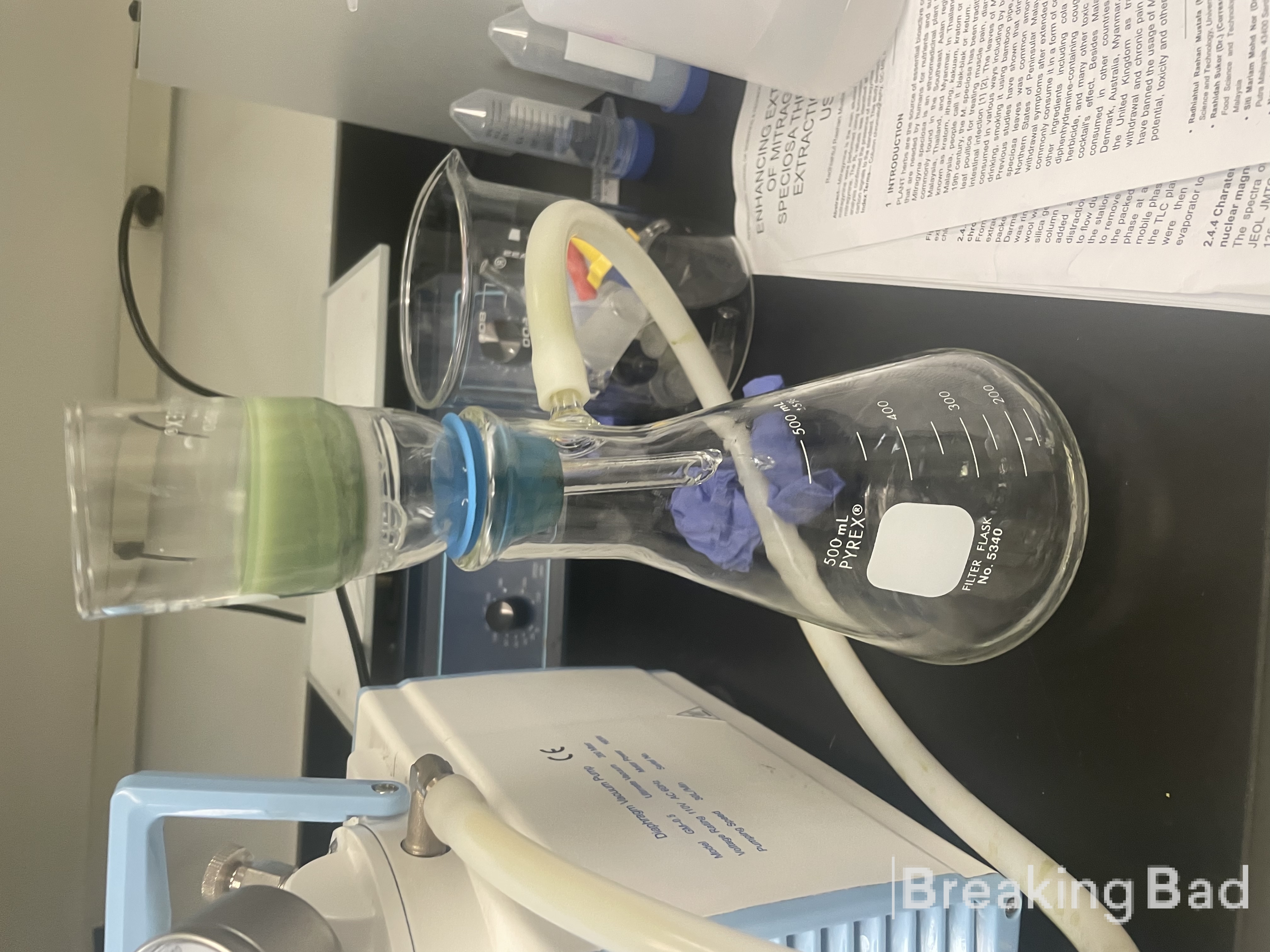
Oké jongens! Tijd om wat kennis met jullie te delen. Ik zal een synthese beschrijven die ik heb gedaan voor psilocine, compleet met foto's. Ik gebruikte de geproduceerde psilocine en ontwikkelde een eenvoudige zelfklevende patch. Om de permeatie van de psilocine in de patch te testen, gebruikten we een diffusieapparaat dat ik in elkaar heb gezet. Het bestaat uit verschillende membranen, met een patch van 1 cm ^ 2 bovenop een stuk verse menselijke huid van 1 cm ^ 2 met een dikte van 400 um (gedoneerd door een chirurgisch centrum voor buikwandcorrecties). Onder de huid is er een constante waterstroom met pH 7,4 en lichaamstemperatuur. Het diffusieapparaat kan een fractie van 1 ml per uur verzamelen, die vervolgens via LC-MS wordt geanalyseerd. De hoeveelheid psilocine in het flesje van 1 ml geeft de flux (mg/uur/cm^2). Dit geeft aan hoeveel psilocine er per uur passeert met een patch van cm^2.
De volgende publicatie, Structure Elucidation and Spectroscopic Analysis of Chromophores Produced by Oxidative Psilocin Dimerization, gaat dieper in op deze kwestie. Wanneer het dimeer gevormd wordt, is het niet op te sporen via HPLC-analyse en ATR-FTIR, wat vreemd is. Dit geeft onderzoeksgroepen valse positieven voor de zuiverheid van hun psilocine. Ik heb een manier gevonden om psilocine in de patch te stabiliseren.
Hoe dan ook, laten we beginnen! Ik heb elke stap zelf gedaan, met de hulp van mijn partner die chemisch ingenieur is. Dit was in de tijd dat ik een schema 1 en 3 DEA licentie had, niet alleen voor onderzoek, maar ook voor productie.
Deel I (Psilocine Synthese)
stap 1: synthese van 3-[2-(Dimethylamino)-2-oxoacetyl]-1H-indol-4-yl acetaat
1a. Een rondbodemkolf van 2000 ml met vier hals werd uitgerust met een bovenroerder, een J-Kem temperatuurregelaar, een druppeltrechter van 250 ml en een rubberen tussenschot waardoor een positieve druk van droogN2 werd ingebracht. Het tussenschot werd verwijderd en de kolf werd gelijkelijk gevuld met 1H-indol-4-yl acetaat (5; 50,1 g, 285 mmol, 1 equiv)
en anhyd Et2O (700 ml). De kolf werd opnieuw afgesloten met het septum en gespoeld met N2. De suspensie werd 10 minuten geroerd en vervolgens
gekoeld tot 0 °C in een ijsbad gedurende 30 minuten.

1b. De druppeltrechter werd gevuld met een oplossing van oxalylchloride (37,1 mL, 428 mmol, 1,5 equiv) in Et2O (60 mL). De oxalylchlorideoplossing werd druppelsgewijs toegevoegd met een snelheid die voldoende was om de temperatuur op of onder 5 °C te houden, om de vorming van dimeer en andere mogelijke bijproducten te minimaliseren. Naarmate de toevoeging vorderde, werd een gele slurry van 10 gevormd en toen de toevoeging voltooid was, werd het mengsel 4 uur geroerd.

1c. Na deze tijd werd heptaan (400 ml) toegevoegd en werd het mengsel gedurende 30 minuten bij 0 °C geroerd. De verkregen gele vaste stof werd snel gefiltreerd en achtereenvolgens gespoeld met heptaan (2 × 300 mL), dat snel werd gebruikt in de volgende stap. . Een 2,0 M oplossing van dimethylamine in THF (175 ml) werd druppelsgewijs toegevoegd met een snelheid die voldoende was om de temperatuur onder 5 °C te houden om nevenreacties te minimaliseren. Nadat de
toevoeging voltooid was, werd pyridine (46 mL) in THF (100 mL) druppelsgewijs toegevoegd en werd het mengsel 60 minuten lang goed geroerd. Heptaan (600 mL) werd toegevoegd en de inhoud van de kolf werd afgezogen gefiltreerd via een Büchnertrechter. Het gefilterde residu werd overgebracht in een rondbodemkolf en gedeïoniseerd H2O (1000 ml) werd toegevoegd, gedurende 30 minuten geroerd en gefilterd via een Büchnertrechter. De gebroken witte vaste stof werd achtereenvolgens gedurende 40 minuten getritueerd in EtOAc (600 ml) en heptaan (400 ml). De slurry werd gefiltreerd via de Büchner trechter en de vaste stof werd gedroogd in een oven bij 40 °C gedurende een nacht om 6 te verkrijgen als een lichtgele vaste stof; opbrengst: 66,1 g (81%); mp 205-207 °C.



ATR-FTIR bevestigde de synthese van 3-[2-(Dimethylamino)-2-oxoacetyl]-1H-indol-4-yl acetaat. Deze verbinding kan enkele maanden bij 4C worden bewaard!
Stap 2: Psilocine synthese
Stap 2A: Een 2000 mL, vierhals, rondbodemkolf werd uitgerust met een bovenroerder, J-Kem temperatuurregelaar, een
250 mL druppeltrechter en een rubberen tussenschot waardoor een positieve druk van droge N2 werd ingebracht. Het tussenschot werd verwijderd en de
kolf gevuld met achtereenvolgens 3-[2-(dimethylamino)-2-oxoacetyl]-1H-indol-4-yl acetaat (6; 31,5 g, 115 mmol) en 2-CH3-THF (1000
mL). De kolf werd ondergedompeld in een ijsbad bij 0 °C en een oplossing van 2,3 M LiAlH4 in 2-CH3-THF (140 mL, 322 mmol) werd toegevoegd via de druppeltrechter van 250 mL.
de druppeltrechter van 250 ml. De druppeltrechter werd gespoeld met extra 2-CH3-THF (20 mL). De LiAlH4-oplossing werd druppelsgewijs toegevoegd
met een snelheid die de temperatuur onder 20 °C hield. Na de toevoeging werd het ijswaterbad verwijderd en werd het mengsel 30 min. geroerd.
De lichtgele oplossing werd verwarmd tot reflux (80 °C) met een verwarmingsmantel en werd ivoorkleurig na 3 uur.
gele vaste stoffen werd waargenomen aan de zijkanten van de rondbodemkolf



Stap 2C. De verwarmingsmantel werd verwijderd en men liet de erlenmeyer afkoelen tot 50 °C. De erlenmeyer werd opnieuw
gekoeld tot 20 °C. De reactie werd geblust door achtereenvolgens 3 druppels 1 M NaOH en 3 druppels gedeïoniseerd H2O toe te voegen. Het mengsel
werd verdund met THF (500 ml) en 20 minuten geroerd. Het mengsel werd gefiltreerd via een Büchnertrechter en het filtraat werd bewaard onder N2.
De filterkoek werd snel opnieuw gemengd met 200 mL [10% oplossing van (7% ammoniak in MeOH) in CH2Cl2] en THF (500 mL). De filtraten
werden vervolgens gecombineerd en geconcentreerd tot een groene vaste stof. De vaste stof werd getritueerd met 1:1 EtOAc/heptaan (50 mL) en vervolgens gefiltreerd via een Büchnertrechter.
Büchner trechter. De donkergroene vaste stof werd gedroogd in een oven bij 40 °C gedurende een nacht om droge psilocine (7) te verkrijgen als een donkergroene vaste stof; opbrengst: 20,7
g (91%); mp 167-169 °C.


Psilocine is gesynthetiseerd.
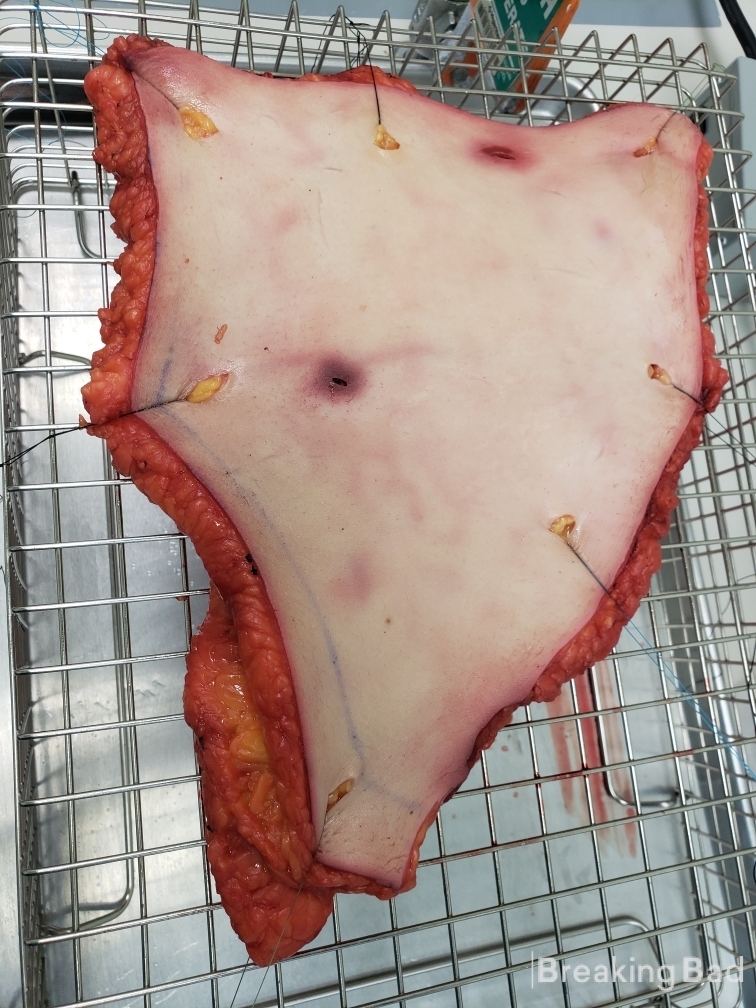
Deel II: Ontwikkeling van de transdermale Psilocinepatch en In-Vitro studie (LET OP: JE ZULT VERVUILD MENSELIJK VLEES ZIEN, HET IS SLECHT).
Vervolgens los ik de psilocine op in een eigen mengsel van acrylaatpolymeer (in heptaan), giet ik de oplossing in een afgietsel en gebruik ik een gietmes om de kleeflaag op 100 um te krijgen. Eenmaal gedroogd breng ik de steunlaag aan en pons ik een patch van 1 cm ^ 2 uit. Deze patch wordt gebruikt voor het in vitro onderzoek.
De volgende foto is een momentopname van het diffusieapparaat (patch bovenop de huid met water dat eronder stroomt)

Ik hoop dat jullie genoten hebben!
De volgende publicatie, Structure Elucidation and Spectroscopic Analysis of Chromophores Produced by Oxidative Psilocin Dimerization, gaat dieper in op deze kwestie. Wanneer het dimeer gevormd wordt, is het niet op te sporen via HPLC-analyse en ATR-FTIR, wat vreemd is. Dit geeft onderzoeksgroepen valse positieven voor de zuiverheid van hun psilocine. Ik heb een manier gevonden om psilocine in de patch te stabiliseren.
Hoe dan ook, laten we beginnen! Ik heb elke stap zelf gedaan, met de hulp van mijn partner die chemisch ingenieur is. Dit was in de tijd dat ik een schema 1 en 3 DEA licentie had, niet alleen voor onderzoek, maar ook voor productie.
Deel I (Psilocine Synthese)
stap 1: synthese van 3-[2-(Dimethylamino)-2-oxoacetyl]-1H-indol-4-yl acetaat
1a. Een rondbodemkolf van 2000 ml met vier hals werd uitgerust met een bovenroerder, een J-Kem temperatuurregelaar, een druppeltrechter van 250 ml en een rubberen tussenschot waardoor een positieve druk van droogN2 werd ingebracht. Het tussenschot werd verwijderd en de kolf werd gelijkelijk gevuld met 1H-indol-4-yl acetaat (5; 50,1 g, 285 mmol, 1 equiv)
en anhyd Et2O (700 ml). De kolf werd opnieuw afgesloten met het septum en gespoeld met N2. De suspensie werd 10 minuten geroerd en vervolgens
gekoeld tot 0 °C in een ijsbad gedurende 30 minuten.
1b. De druppeltrechter werd gevuld met een oplossing van oxalylchloride (37,1 mL, 428 mmol, 1,5 equiv) in Et2O (60 mL). De oxalylchlorideoplossing werd druppelsgewijs toegevoegd met een snelheid die voldoende was om de temperatuur op of onder 5 °C te houden, om de vorming van dimeer en andere mogelijke bijproducten te minimaliseren. Naarmate de toevoeging vorderde, werd een gele slurry van 10 gevormd en toen de toevoeging voltooid was, werd het mengsel 4 uur geroerd.
1c. Na deze tijd werd heptaan (400 ml) toegevoegd en werd het mengsel gedurende 30 minuten bij 0 °C geroerd. De verkregen gele vaste stof werd snel gefiltreerd en achtereenvolgens gespoeld met heptaan (2 × 300 mL), dat snel werd gebruikt in de volgende stap. . Een 2,0 M oplossing van dimethylamine in THF (175 ml) werd druppelsgewijs toegevoegd met een snelheid die voldoende was om de temperatuur onder 5 °C te houden om nevenreacties te minimaliseren. Nadat de
toevoeging voltooid was, werd pyridine (46 mL) in THF (100 mL) druppelsgewijs toegevoegd en werd het mengsel 60 minuten lang goed geroerd. Heptaan (600 mL) werd toegevoegd en de inhoud van de kolf werd afgezogen gefiltreerd via een Büchnertrechter. Het gefilterde residu werd overgebracht in een rondbodemkolf en gedeïoniseerd H2O (1000 ml) werd toegevoegd, gedurende 30 minuten geroerd en gefilterd via een Büchnertrechter. De gebroken witte vaste stof werd achtereenvolgens gedurende 40 minuten getritueerd in EtOAc (600 ml) en heptaan (400 ml). De slurry werd gefiltreerd via de Büchner trechter en de vaste stof werd gedroogd in een oven bij 40 °C gedurende een nacht om 6 te verkrijgen als een lichtgele vaste stof; opbrengst: 66,1 g (81%); mp 205-207 °C.
ATR-FTIR bevestigde de synthese van 3-[2-(Dimethylamino)-2-oxoacetyl]-1H-indol-4-yl acetaat. Deze verbinding kan enkele maanden bij 4C worden bewaard!
Stap 2: Psilocine synthese
Stap 2A: Een 2000 mL, vierhals, rondbodemkolf werd uitgerust met een bovenroerder, J-Kem temperatuurregelaar, een
250 mL druppeltrechter en een rubberen tussenschot waardoor een positieve druk van droge N2 werd ingebracht. Het tussenschot werd verwijderd en de
kolf gevuld met achtereenvolgens 3-[2-(dimethylamino)-2-oxoacetyl]-1H-indol-4-yl acetaat (6; 31,5 g, 115 mmol) en 2-CH3-THF (1000
mL). De kolf werd ondergedompeld in een ijsbad bij 0 °C en een oplossing van 2,3 M LiAlH4 in 2-CH3-THF (140 mL, 322 mmol) werd toegevoegd via de druppeltrechter van 250 mL.
de druppeltrechter van 250 ml. De druppeltrechter werd gespoeld met extra 2-CH3-THF (20 mL). De LiAlH4-oplossing werd druppelsgewijs toegevoegd
met een snelheid die de temperatuur onder 20 °C hield. Na de toevoeging werd het ijswaterbad verwijderd en werd het mengsel 30 min. geroerd.
De lichtgele oplossing werd verwarmd tot reflux (80 °C) met een verwarmingsmantel en werd ivoorkleurig na 3 uur.
gele vaste stoffen werd waargenomen aan de zijkanten van de rondbodemkolf
Stap 2C. De verwarmingsmantel werd verwijderd en men liet de erlenmeyer afkoelen tot 50 °C. De erlenmeyer werd opnieuw
gekoeld tot 20 °C. De reactie werd geblust door achtereenvolgens 3 druppels 1 M NaOH en 3 druppels gedeïoniseerd H2O toe te voegen. Het mengsel
werd verdund met THF (500 ml) en 20 minuten geroerd. Het mengsel werd gefiltreerd via een Büchnertrechter en het filtraat werd bewaard onder N2.
De filterkoek werd snel opnieuw gemengd met 200 mL [10% oplossing van (7% ammoniak in MeOH) in CH2Cl2] en THF (500 mL). De filtraten
werden vervolgens gecombineerd en geconcentreerd tot een groene vaste stof. De vaste stof werd getritueerd met 1:1 EtOAc/heptaan (50 mL) en vervolgens gefiltreerd via een Büchnertrechter.
Büchner trechter. De donkergroene vaste stof werd gedroogd in een oven bij 40 °C gedurende een nacht om droge psilocine (7) te verkrijgen als een donkergroene vaste stof; opbrengst: 20,7
g (91%); mp 167-169 °C.
Psilocine is gesynthetiseerd.
Deel II: Ontwikkeling van de transdermale Psilocinepatch en In-Vitro studie (LET OP: JE ZULT VERVUILD MENSELIJK VLEES ZIEN, HET IS SLECHT).
Vervolgens los ik de psilocine op in een eigen mengsel van acrylaatpolymeer (in heptaan), giet ik de oplossing in een afgietsel en gebruik ik een gietmes om de kleeflaag op 100 um te krijgen. Eenmaal gedroogd breng ik de steunlaag aan en pons ik een patch van 1 cm ^ 2 uit. Deze patch wordt gebruikt voor het in vitro onderzoek.
De volgende foto is een momentopname van het diffusieapparaat (patch bovenop de huid met water dat eronder stroomt)
Ik hoop dat jullie genoten hebben!


