G.Patton
Expert
- Joined
- Jul 5, 2021
- Messages
- 2,772
- Solutions
- 3
- Reaction score
- 2,999
- Points
- 113
- Deals
- 1
Uvod
Dietil eter ali CH3CH2-O-CH2CH3 (Et2O) je odlično topilo za številne reakcije, vendar je izredno vnetljiv. Profesionalni kemiki so dobro obveščeni o nevarnostih, ki jih predstavlja uporaba etra, vendar se laiki teh nevarnosti manj verjetno zavedajo. Hlapi dietil etra v suhem zraku lahko tvorijo eksplozivne perokside. Z drugimi besedami, tudi v okolju brez iskrenja/plamena lahko pride do eksplozije, ko se srečamo s hlapi etra. Zaradi tega je treba imeti način za odstranjevanje hlapov iz okolice (odličen primer je digestor) in ne smemo uporabljati etra v dneh z zelo nizko vlažnostjo. Ker je dietil eter vnetljiv in nagnjen k vžigu, je treba ta postopek izvesti z vročo kuhalnico/mešalnikom, namenjenim za uporabo v vnetljivih okoljih. Takšen grelnik/mešalnik ne ustvarja kontaktne iskre, ko se vklopi grelna plošča, za mešalnik pa se običajno uporablja izmenični motor brez ščetk, saj motorji na enosmerni tok s ščetkami običajno proizvajajo majhne iskre, ki bi lahko vžgale morebitne blodeče hlape.
Dietil eter se pripravi iz etanola (znanega tudi kot žitni alkohol, etilni alkohol, pitni alkohol) s segrevanjem s koncentrirano žveplovo kislino. Reakcija poteka prek vmesnega člena, "etil žveplove kisline", tako kot večina tovrstnih reakcij. To sintezo lahko enostavno razširite, tako da sorazmerno povečate reakcijsko bučko in število snovi.
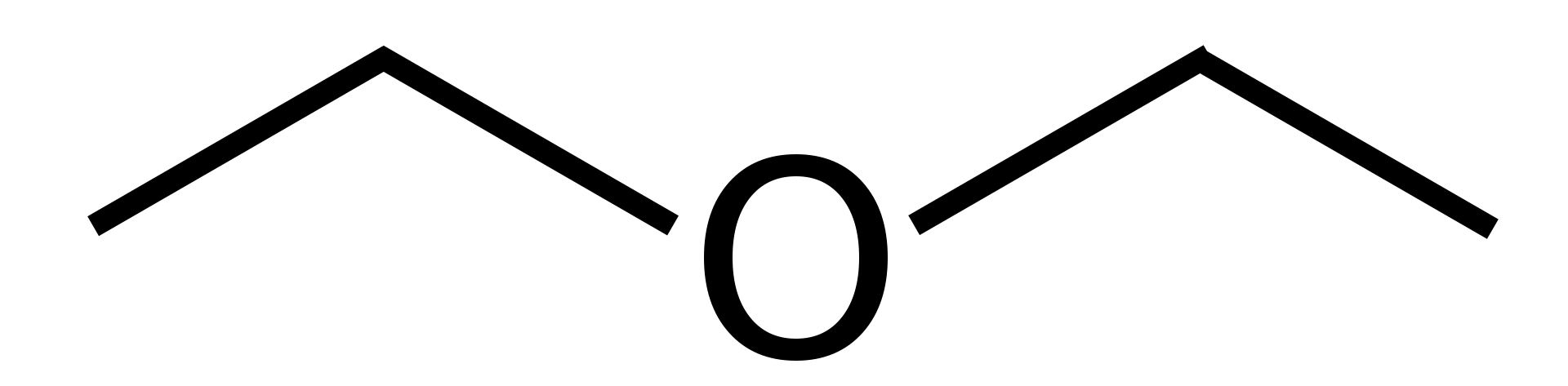
Videz: brezbarvna tekočina s suhim, rumovim, sladkastim vonjem;Dietil eter se pripravi iz etanola (znanega tudi kot žitni alkohol, etilni alkohol, pitni alkohol) s segrevanjem s koncentrirano žveplovo kislino. Reakcija poteka prek vmesnega člena, "etil žveplove kisline", tako kot večina tovrstnih reakcij. To sintezo lahko enostavno razširite, tako da sorazmerno povečate reakcijsko bučko in število snovi.
vrelišče: 34,65 °C/760 mm Hg;
tališče: -116,3 °C;
molekulska masa: 74,123 g/mol;
gostota: 0,7134 g/ml (20 °C).
Oprema in steklovina.
Priprava za frakcionirano destilacijo;0,5 l bučka s kroglastim dnom in tremi vrati
Magnetno mešalo;
Kopeli za olje in ledeno vodo;
0.5 L x2 lijak za kapljanje;
laboratorijski termometer (od 0 °C do 200 °C) z nastavkom za bučko;
trakovi z indikatorjem pH;
stojalo za retorto in objemka za pritrditev aparatur;
laboratorijska tehtnica (primerna za 1-200 g);
100 ml x2 in 200 ml x2 Erlenmeyerjeve bučke s pokrovčki;
200 ml x2; 100 ml x2 čaše;
500 ml ali 100 ml merilni valj;
vrelišča.
Reagenti.
123,9 ml (97 g, 2 mol) etanola 95 %;109 ml (200,16 g, 2 mol) žveplove kisline (98 %);
50 g natrijevega hidroksida (NaOH);
50 g natrijevega klorida (NaCl);
15 g kalcijevega klorida (CaCl2);
~1,5 L destilirane vode;
~20 g kovinskega natrija (Na)
Manipulacije
1. Čeprav to ni najbolj prijeten postopek, lahko dietil eter dobimo s kondenzacijo etanola. V ta namen sestavite tipično napravo za frakcionirano destilacijo s kolono vigreux in bučko s tremi vrati. Preden vse skupaj zaprete, ne pozabite v bučko spustiti magnetnega mešalnika, ki ga boste segrevali na oljni kopeli (v etru ni dovoljeno uporabljati plamena, saj veste). Stolpec vigreuxa je v srednjem vratu, dodajalni lij v enem stranskem vratu, termometer pa v drugem stranskem vratu.
2. V erlenmajerico dodajte 2x mol (kjer je x mnogokratnik, 1 = 2 mola, 1,5 = 3 mola itd.) azeotropa etanola (tj. 95 % etanola). Etanolu počasi dodajte 2x mol koncentrirane (98 %) žveplove kisline (zaradi vode se bo segrela) prek kapalnega lijaka. Vključite mešalnik, vklopite ogrevanje in erlenmajerico segrejte na 130 °C. Prepričajte se, da je kondenzator dobro oskrbljen s hladno vodo, in nadaljujte s segrevanjem, dokler vsebina reakcijske bučke ne doseže približno 135 °C.
3. Ko se začne destilacija, skozi dodajalni lijak počasi dodajajte še do 2x mola etanola s hitrostjo, ki je enaka kapljicam, ki prihajajo iz kondenzatorja. Za 2 mola alkohola (123,9 g) naj bi z ustrezno vigreuxovo kolono potrebovali 1 uro. Pri krajši koloni (ali, če je sploh ni) bo potrebna počasnejša destilacija (in če ne boste uporabili kolone, boste morali izdelek precej izpirati s slano vodo).
4 . Vsebino sprejemne bučke prelijte v veliko čašo ali skledo in jo prelijte z 10-odstotno raztopino natrijevega hidroksida (NaOH aq), dokler pH ni nevtralen. To zmes prelijte v ločilni lijak, da ločite eter od vodnega hidroksida, in jo še dvakrat sperite z enakim volumnom napol nasičene raztopine natrijevega klorida (NaCl) (~18 g/100 ml vode pri tekočem stanju). Zadnjo raztopino za izpiranje + eter pustimo v erlenmajerici, dokler se vse ne umiri, nato pa previdno odcedimo izpiranje in z vrha v erlenmajerico z okroglim dnom prelijemo eter. Dodajte 15 g kalcijevega klorida (CaCl2) (vlažen rid) na vsak mol etra, spustite magnet za mešanje in mešajte 2 uri.
5 . Destilirajte eter iz kalcijevega klorida s segrevanjem na kopeli (oljni ali vodni) pri temperaturi, ki ne presega 45 °C. Zberite destilat s temperaturo 31-36 °C.
Brezvodni etil eter. To je za tiste formule, ki zahtevajo suhi, čisti ali brezvodni eter. Zgornji etrski produkt sušimo nad tankimi rezinami kovinskega natrija (dobro se obnese tudi kovinska natrijeva žica) 24 ur. Nato se eter destilira na vodni kopeli nad svežim kovinskim natrijem (svež pomeni drugo serijo, kot ste jo sušili).
Opomba: eter pri daljšem zadrževanju, tudi če ste ga kupili v trgovini, razvije eksplozivne perokside. Zato pred ravnanjem s skladiščenim etrom pretresite z železovim sulfatom ali svinčevim peroksidom. Da bi preprečili nastanek peroksidov v svežem etru, v temno posodo dodajte več delov bakrene ali železne žice in jo shranite na hladnem mestu.
Čiščenje
4 . Vsebino sprejemne bučke prelijte v veliko čašo ali skledo in jo prelijte z 10-odstotno raztopino natrijevega hidroksida (NaOH aq), dokler pH ni nevtralen. To zmes prelijte v ločilni lijak, da ločite eter od vodnega hidroksida, in jo še dvakrat sperite z enakim volumnom napol nasičene raztopine natrijevega klorida (NaCl) (~18 g/100 ml vode pri tekočem stanju). Zadnjo raztopino za izpiranje + eter pustimo v erlenmajerici, dokler se vse ne umiri, nato pa previdno odcedimo izpiranje in z vrha v erlenmajerico z okroglim dnom prelijemo eter. Dodajte 15 g kalcijevega klorida (CaCl2) (vlažen rid) na vsak mol etra, spustite magnet za mešanje in mešajte 2 uri.
5 . Destilirajte eter iz kalcijevega klorida s segrevanjem na kopeli (oljni ali vodni) pri temperaturi, ki ne presega 45 °C. Zberite destilat s temperaturo 31-36 °C.
Brezvodni etil eter. To je za tiste formule, ki zahtevajo suhi, čisti ali brezvodni eter. Zgornji etrski produkt sušimo nad tankimi rezinami kovinskega natrija (dobro se obnese tudi kovinska natrijeva žica) 24 ur. Nato se eter destilira na vodni kopeli nad svežim kovinskim natrijem (svež pomeni drugo serijo, kot ste jo sušili).
Opomba: eter pri daljšem zadrževanju, tudi če ste ga kupili v trgovini, razvije eksplozivne perokside. Zato pred ravnanjem s skladiščenim etrom pretresite z železovim sulfatom ali svinčevim peroksidom. Da bi preprečili nastanek peroksidov v svežem etru, v temno posodo dodajte več delov bakrene ali železne žice in jo shranite na hladnem mestu.
Čiščenje
Čiščenje in sušenje dietil etra za Grignardove reakcije z uporabo kalijevega hidroksida in natrija
- G.Patton
- 1
Čiščenje in sušenje dietil etra za Grignardove reakcije z uporabo kalijevega hidroksida in natrija
Ekstrakcija dietiletra in heptana iz zagonske tekočine
- G.Patton
- 5
Ekstrakcija dietiletra in heptana iz zagonske tekočine
Last edited:
