SoldadoDeDrogas
🥷 RESIDENT 🥷
Kan någon hjälpa mig att förstå om det är möjligt att använda generiska nasala inhalatorer som innehåller "levmetamfetamin 50 mg" för att komma till d-meth.
https://bbgate.com/threads/methamphetamine-synthesis-vicks-inhaler.4974/#post-46343 Kommer dessa instruktioner att fungera i teorin?
Eller måste jag använda ovanstående racemisering och upplösning som tillhandahålls av Amphibian? Eller 41Dxflatline, etc?
https://bbgate.com/threads/methamphetamine-synthesis-vicks-inhaler.4974/#post-46343 Kommer dessa instruktioner att fungera i teorin?
Eller måste jag använda ovanstående racemisering och upplösning som tillhandahålls av Amphibian? Eller 41Dxflatline, etc?
Även om det skulle fungera ... vissa av dessa kemikalier är svåra att få tag på eller kan vara farliga som mitt användarnamn, istället bör du använda naproxen och använda pope-peachy med NASID Naproxen. Jag har lagt upp hela guiden nedan
↑View previous replies…
- By azides
Utarbetandet har publicerats tidigare men igen
Det är ....
Studie av mekanismen för den optiska upplösningen av N-metylamfetamin via diastereoisomerisk saltbildning med Pope-Peachey-upplösningsmetoden som diskuterades av retorten senare
https://sci-hub.wf/10.1016/s0957-4166(00)86170-4
https://www.sciencedirect.com/science/article/abs/pii/S0957416600861704
refenenser och anmärkningar
I.) Newman,P. Optical Resolution Procedures for Chemical Compounds, vol.l-3, optical Resolution Informztion
Catre, Manhattan College, New York, 1978-84;
2.) Jacques,J.; Collet,A.; Wilen,SH. Enantiomers, Racemates and Resolutions, Wiley and Sons, New York,
1981,378.p.
3.) Fogassy,E.; hs,M.; Faigl,F ; Rohonczy,J, Ecsery,Z. J.Chem.Soc.Perkin Trans.2, 1986, 1881
4.) Pope,W.J.; Peachey,S.J. J.Chem.Soc.,1899,75,1066
5.) 7,84 g (0,0525 mol) racemisk N-metylamfetamin och 9,73 g (0,0525 mol) racemisk N-
metylamfetaminhydroklorid löstes i 70 ml abs. etanol och 7,91 g (0,0525 mol) R,R-
tartaxinsyra i 56 ml abs. etanol. Båda stamlösningarna delades upp i femton volymportioner med en
burett och reagerade vid 22+1"C Blandningarna fick stå ostörda i 15, 90 minuter och 5, 24, 1 IS
timmar, varefter utfällningarna filtrerades och torkades. Från 0,4 g av varje salt frigjordes basen med ccNaOH
och extraherades från vattenfasen med dikblorometbane.
6.) Alla experiment utfördes på samma arbetsbänk vid 2Ul'C rumstemperatur. Stamlösningar av
racematet och lösningsmedlet användes för att undvika fel i viktmätningar. Alla kolvar som användes
hade identisk storlek och form.
7.)Salternas innehåll av tartrat och hydroklorid bestämdes genom potenciometri med en RADIOMETER-
85 TTT automatisk titrator med 0,1 N NaOH och 0,1 N AgNO,.
8.) Den specifika rotationen mättes med en Perkin Elmer 241 polarhneter. Den specifika rotationen för
optiskt ren R-N-metylamfetamin är [a]: - -18,90 (c 0,1, IN HCI).
9.) Salterna tvättades inte vid filtreringen. Den lilla mängden hydroklorid som finns i salterna kommer förmodligen
från moderluten som fastnat och torkat på ytan av saltet.
10.) Detta är i enlighet med resultaten3, att R-l II är det mer stabila saltet än S-1.11
Om du vill ha mer kan du också läsa retorten nedan allt ska vara i https://sci-hub.wf i stort sett dock
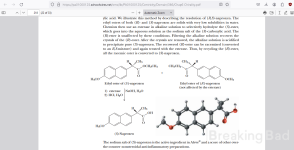
Istället används i denna twist endast en halv ekvivalent kiral amin. En halv ekvivalent av en billigare, optiskt inaktiv aminbas används i stället. Detta gör inte bara processen billigare, utan resulterar i en mer dramatisk skillnad i lösligheter. Den konjugerade basen av den önskade (d)-(+)-enantiomeren kristalliseras ut med den konjugerade syran av den kirala aminen, med hög selektivitet. Detta lämnar den mer lösliga saltprodukten av (l)-(-)-naproxen och den achirala aminen kvar i lösningen.
Det är ....
Studie av mekanismen för den optiska upplösningen av N-metylamfetamin via diastereoisomerisk saltbildning med Pope-Peachey-upplösningsmetoden som diskuterades av retorten senare
https://sci-hub.wf/10.1016/s0957-4166(00)86170-4
https://www.sciencedirect.com/science/article/abs/pii/S0957416600861704
refenenser och anmärkningar
I.) Newman,P. Optical Resolution Procedures for Chemical Compounds, vol.l-3, optical Resolution Informztion
Catre, Manhattan College, New York, 1978-84;
2.) Jacques,J.; Collet,A.; Wilen,SH. Enantiomers, Racemates and Resolutions, Wiley and Sons, New York,
1981,378.p.
3.) Fogassy,E.; hs,M.; Faigl,F ; Rohonczy,J, Ecsery,Z. J.Chem.Soc.Perkin Trans.2, 1986, 1881
4.) Pope,W.J.; Peachey,S.J. J.Chem.Soc.,1899,75,1066
5.) 7,84 g (0,0525 mol) racemisk N-metylamfetamin och 9,73 g (0,0525 mol) racemisk N-
metylamfetaminhydroklorid löstes i 70 ml abs. etanol och 7,91 g (0,0525 mol) R,R-
tartaxinsyra i 56 ml abs. etanol. Båda stamlösningarna delades upp i femton volymportioner med en
burett och reagerade vid 22+1"C Blandningarna fick stå ostörda i 15, 90 minuter och 5, 24, 1 IS
timmar, varefter utfällningarna filtrerades och torkades. Från 0,4 g av varje salt frigjordes basen med ccNaOH
och extraherades från vattenfasen med dikblorometbane.
6.) Alla experiment utfördes på samma arbetsbänk vid 2Ul'C rumstemperatur. Stamlösningar av
racematet och lösningsmedlet användes för att undvika fel i viktmätningar. Alla kolvar som användes
hade identisk storlek och form.
7.)Salternas innehåll av tartrat och hydroklorid bestämdes genom potenciometri med en RADIOMETER-
85 TTT automatisk titrator med 0,1 N NaOH och 0,1 N AgNO,.
8.) Den specifika rotationen mättes med en Perkin Elmer 241 polarhneter. Den specifika rotationen för
optiskt ren R-N-metylamfetamin är [a]: - -18,90 (c 0,1, IN HCI).
9.) Salterna tvättades inte vid filtreringen. Den lilla mängden hydroklorid som finns i salterna kommer förmodligen
från moderluten som fastnat och torkat på ytan av saltet.
10.) Detta är i enlighet med resultaten3, att R-l II är det mer stabila saltet än S-1.11
Om du vill ha mer kan du också läsa retorten nedan allt ska vara i https://sci-hub.wf i stort sett dock
Istället används i denna twist endast en halv ekvivalent kiral amin. En halv ekvivalent av en billigare, optiskt inaktiv aminbas används i stället. Detta gör inte bara processen billigare, utan resulterar i en mer dramatisk skillnad i lösligheter. Den konjugerade basen av den önskade (d)-(+)-enantiomeren kristalliseras ut med den konjugerade syran av den kirala aminen, med hög selektivitet. Detta lämnar den mer lösliga saltprodukten av (l)-(-)-naproxen och den achirala aminen kvar i lösningen.
Last edited: