@G.Patton Domnívám se, že jeden z nakreslených meziproduktů na této syntéze (a z původního článku o rhodiu) je nesprávný.
(3), vyobrazení meziproduktu amfetamin-formaldehyd-imin má stejnou strukturu jako fenylaceton-methylamin-imin, který lze vidět na jiném místě
to se mi nezdá správné ze dvou důvodů: za prvé, nakreslením standardního mechanismu vzniku iminu na substrátu vzniká imin, kde dvojná vazba je mezi N a rádoby methylovou skupinou na metamfetaminu, a NE mezi N a alfa-uhlíkem jako v uvedené struktuře. a zamyslete se: dvojná vazba vzniká, když osamělý pár aminu odkopne vodu vzniklou na formaldehydovém kyslíku jako odcházející skupinu, což se musí stát na straně formaldehydu (rádoby methylové skupiny)
za druhé, syntéza je uváděna jako stereospecifická na základě výchozího substrátu. to znamená, že redukcí d-amph vznikne d-meth a totéž platí pro l-isomer. struktura, jak je uvedena (3), nemá žádná chirální centra a její redukce je ekvivalentní standardní reduktivní aminyzaci fenylacetonu, která dává racemický produkt. navrhovaná struktura, kterou jsem uvedl pro meziprodukt, má chirální centrum, které by bylo stejné jako u výchozího materiálu, a proto odpovídá pozorované stereospecifičnosti reakce.
pokud mám pravdu, vyjasnilo by to otázky týkající se stereospecifičnosti reakce dříve ve vlákně. pokud jsem někde udělal chybu, omlouvám se, ale zajímalo mě, proč redukce nechirálního (3) vede k nerecemické směsi produktů, když se použije nerecemický výchozí materiál amfetamin.
(3), vyobrazení meziproduktu amfetamin-formaldehyd-imin má stejnou strukturu jako fenylaceton-methylamin-imin, který lze vidět na jiném místě
to se mi nezdá správné ze dvou důvodů: za prvé, nakreslením standardního mechanismu vzniku iminu na substrátu vzniká imin, kde dvojná vazba je mezi N a rádoby methylovou skupinou na metamfetaminu, a NE mezi N a alfa-uhlíkem jako v uvedené struktuře. a zamyslete se: dvojná vazba vzniká, když osamělý pár aminu odkopne vodu vzniklou na formaldehydovém kyslíku jako odcházející skupinu, což se musí stát na straně formaldehydu (rádoby methylové skupiny)
za druhé, syntéza je uváděna jako stereospecifická na základě výchozího substrátu. to znamená, že redukcí d-amph vznikne d-meth a totéž platí pro l-isomer. struktura, jak je uvedena (3), nemá žádná chirální centra a její redukce je ekvivalentní standardní reduktivní aminyzaci fenylacetonu, která dává racemický produkt. navrhovaná struktura, kterou jsem uvedl pro meziprodukt, má chirální centrum, které by bylo stejné jako u výchozího materiálu, a proto odpovídá pozorované stereospecifičnosti reakce.
pokud mám pravdu, vyjasnilo by to otázky týkající se stereospecifičnosti reakce dříve ve vlákně. pokud jsem někde udělal chybu, omlouvám se, ale zajímalo mě, proč redukce nechirálního (3) vede k nerecemické směsi produktů, když se použije nerecemický výchozí materiál amfetamin.
Dobrý den, za prvé, uhlík a má větší elektronovou hustotu než methyl uhlík. Typický mechanismus vede k takovému meziproduktu (skrytý pod vodoznakem Breaking Bad, sry):
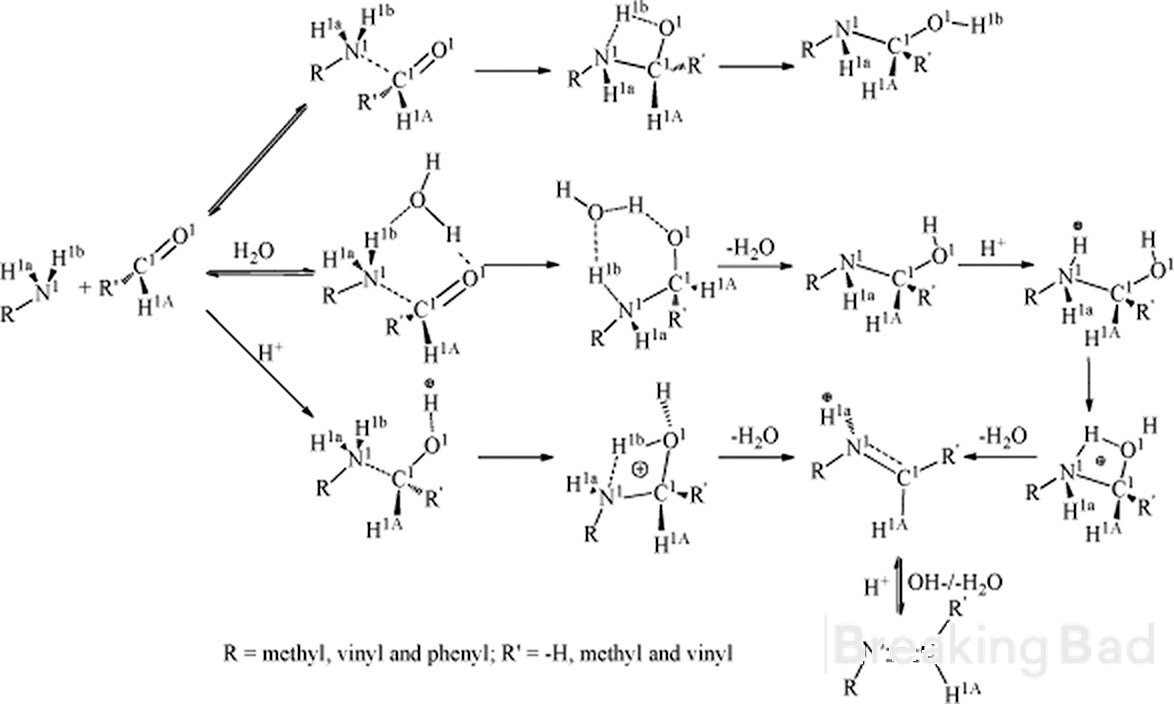
Za druhé, máte nějaké spolehlivé údaje o stereo specifickém výsledku této syntézy?
Za druhé, máte nějaké spolehlivé údaje o stereo specifickém výsledku této syntézy?
