@G.Patton Manau, kad vienas iš šioje sintezėje (ir iš originalaus straipsnio apie rodį) piešiamų tarpinių produktų yra neteisingas.
(3) pavaizduotas amfetamino-formaldehido imino tarpinis produktas turi tokią pačią struktūrą kaip ir fenilacetono-metilamino iminas, kurį galima pamatyti kitur
man tai neatrodo teisinga dėl dviejų priežasčių: pirma, nubrėžus standartinį imino susidarymo mechanizmą ant substrato, gaunamas iminas, kuriame dviguba jungtis yra tarp N ir būsimos metilo grupės metamfetamine, o NE tarp N ir alfa anglies, kaip nurodyta pateiktoje struktūroje. ir pagalvokite: dviguba jungtis susidaro, kai amino vienguba pora išmuša vandenį, susidariusį ant formaldehido deguonies, kaip išeinančią grupę, o tai turi būti padaryta formaldehido (būsimos metilo grupės) pusėje
antra, sintezė yra stereospecifinė pagal pradinį substratą. tai yra, redukuojant d-amf gausime d-meth ir tą patį l-izomerą. struktūra, kaip parodyta (3), neturi chiralinių centrų, o jos redukavimas yra lygiavertis standartiniam redukciniam fenilacetono aminavimui, kurio metu gaunamas raceminis produktas. siūloma tarpinio junginio struktūra, kurią pateikiau, turi chiralinį centrą, kuris būtų toks pat kaip pradinės medžiagos ir todėl atitiktų stebimą reakcijos stereospecifiškumą.
jei esu teisus, tai leistų išsiaiškinti anksčiau šioje temoje iškeltus klausimus dėl reakcijos stereospecifiškumo. jei kur nors suklydau, atsiprašau, bet man buvo įdomu, kodėl redukuojant nechiralinį (3) gaunamas nerachirinis produktų mišinys, kai naudojama nerachirinė pradinė medžiaga amfetaminas.
(3) pavaizduotas amfetamino-formaldehido imino tarpinis produktas turi tokią pačią struktūrą kaip ir fenilacetono-metilamino iminas, kurį galima pamatyti kitur
man tai neatrodo teisinga dėl dviejų priežasčių: pirma, nubrėžus standartinį imino susidarymo mechanizmą ant substrato, gaunamas iminas, kuriame dviguba jungtis yra tarp N ir būsimos metilo grupės metamfetamine, o NE tarp N ir alfa anglies, kaip nurodyta pateiktoje struktūroje. ir pagalvokite: dviguba jungtis susidaro, kai amino vienguba pora išmuša vandenį, susidariusį ant formaldehido deguonies, kaip išeinančią grupę, o tai turi būti padaryta formaldehido (būsimos metilo grupės) pusėje
antra, sintezė yra stereospecifinė pagal pradinį substratą. tai yra, redukuojant d-amf gausime d-meth ir tą patį l-izomerą. struktūra, kaip parodyta (3), neturi chiralinių centrų, o jos redukavimas yra lygiavertis standartiniam redukciniam fenilacetono aminavimui, kurio metu gaunamas raceminis produktas. siūloma tarpinio junginio struktūra, kurią pateikiau, turi chiralinį centrą, kuris būtų toks pat kaip pradinės medžiagos ir todėl atitiktų stebimą reakcijos stereospecifiškumą.
jei esu teisus, tai leistų išsiaiškinti anksčiau šioje temoje iškeltus klausimus dėl reakcijos stereospecifiškumo. jei kur nors suklydau, atsiprašau, bet man buvo įdomu, kodėl redukuojant nechiralinį (3) gaunamas nerachirinis produktų mišinys, kai naudojama nerachirinė pradinė medžiaga amfetaminas.
G.Patton
Expert
- Joined
- Jul 5, 2021
- Messages
- 3,045
- Solutions
- 3
- Reaction score
- 3,479
- Points
- 113
- Deals
- 1
Sveiki. pirma, a anglis turi didesnį elektronų tankį nei metilo anglis. Tipiškas mechanizmas lemia tokį tarpinį junginį (paslėpta po Breaking Bad vandens ženklu, sry):
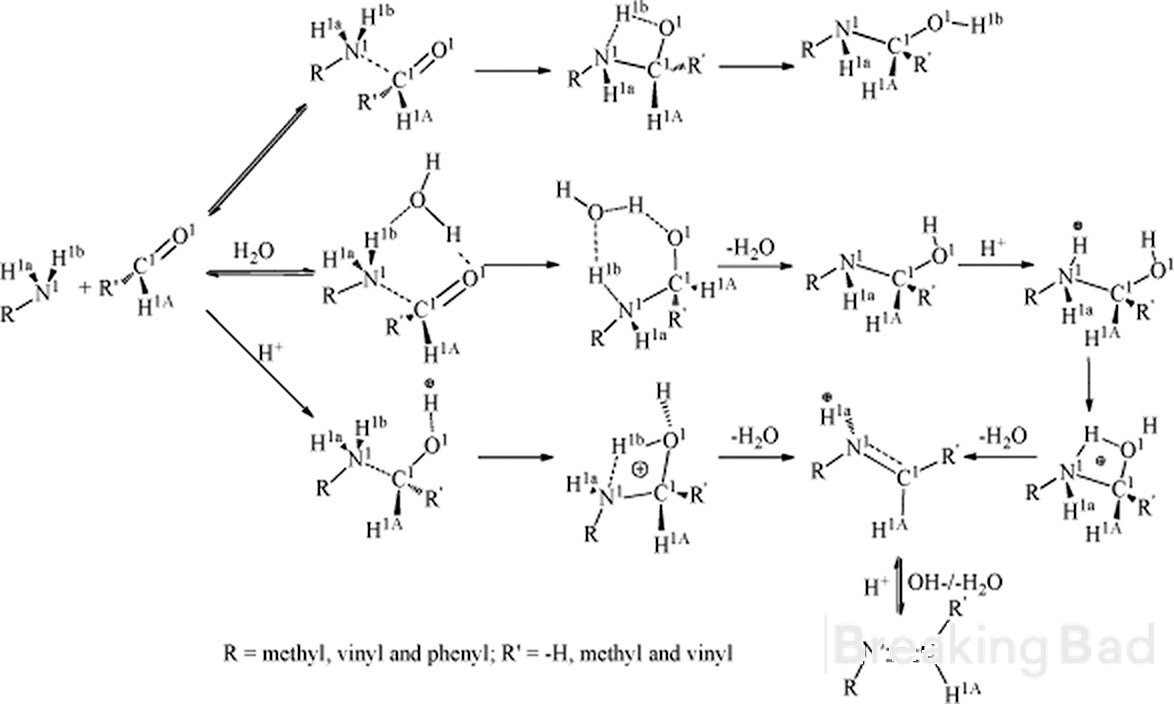
Antra, ar turite kokių nors patikimų duomenų apie stereospecifinį šios sintezės rezultatą?
Antra, ar turite kokių nors patikimų duomenų apie stereospecifinį šios sintezės rezultatą?
↑View previous replies…
- Language
- 🇷🇺
- Joined
- Apr 2, 2024
- Messages
- 3
- Reaction score
- 0
- Points
- 1
- By NexusPrime
Rodiklis yra klaida, dvigubos jungties nėra, žr. toliau pateiktą pavyzdį su benzaldehidu
