Brain
Expert Pharmacologist
- Joined
- Jul 6, 2021
- Messages
- 328
- Reaction score
- 332
- Points
- 63
Dekstroamfetamina (D-AMP) należy do klasy stymulantów ośrodkowego układu nerwowego. Żywności i Leków w USA klasyfikuje ją jako substancję z harmonogramu II o wysokim potencjale nadużywania. Leki o natychmiastowym i opóźnionym uwalnianiu amfetaminy są zatwierdzone przez FDA do leczenia ADHD i narkolepsji zarówno u dorosłych, jak i dzieci. Dekstroamfetamina różni się od swojego odbicia - lewamfetaminy - ponieważ ma bardziej wyraźną stymulację układu nerwowego z powodu dopaminy, a mniej - z powodu noradrenaliny.
Synteza dekstroamfetaminy z P2P
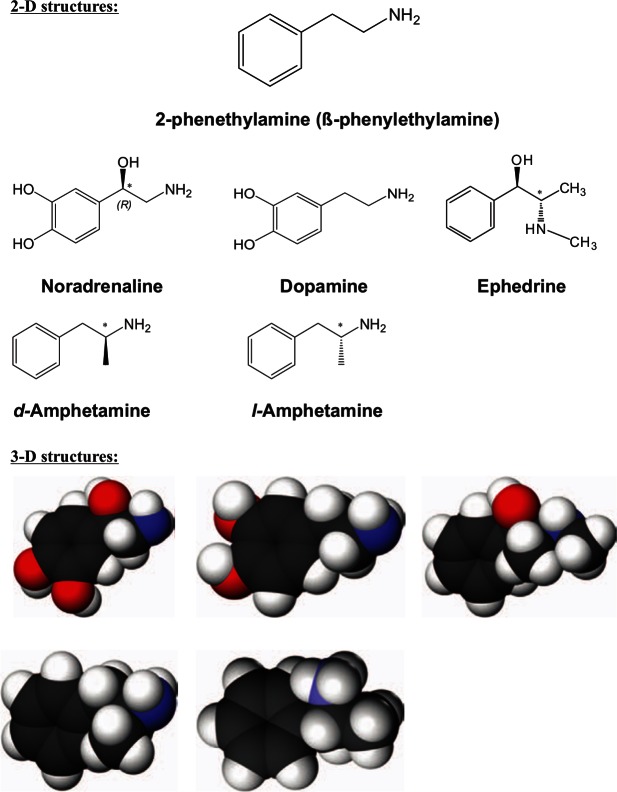
Właściwości fizykochemiczne i formy substancji.
Zasadniczo dekstroamfetamina, a także racemat amfetaminy, ma wygląd bezbarwnej lotnej oleistej cieczy o charakterystycznym "rybim" zapachu i jest dobrze rozpuszczalna w rozpuszczalnikach organicznych. Jego temperatura wrzenia wynosi 200-203 °C. Enancjomer może mieć wygląd proszku z tworzeniem małych "kamieni" w kolorze białym lub jasnożółtym/kremowym, o słabym zapachu, słabo higroskopijny, częściowo rozpuszczalny w wodzie, gdy jest w postaci tabletki. Najczęściej występuje w postaci siarczanu, chlorowodorku, sacharynianu i bardzo rzadko w postaci fosforanu. Z reguły dekstroamfetamina jest częścią różnych leków, takich jak "Aderral" i "Dexedrine", gdzie występuje w postaci sacharynianu i siarczanu w stężeniach 25% całkowitej objętości. Jest również częścią "Vyvanse", "Elvanse", "Tyvense", gdzie występuje w stanie proaktywnym dimesylanu lizdeksamfetaminy; fermentacja z l-lizyną metabolizuje ją do aktywnej postaci d-amfetaminy; "Dexedrine". Inne nazwy handlowe leków obejmują: Siarczan deksedryny, Afatin, d-Amfetasul, Domafate Obesedrin, Dexten, Maxiton, Sympamin, Simpamina-D, Albemap, Dadex, Ardex, Dexalone, Amsustain, Betafedrina, d-Betafedryna, Diocurb, Dextrostat.
Farmakokinetyka.
Po podaniu amfetamina jest metabolizowana przez hydroksylację, gdzie głównym cytochromem jest CYP2D6, beta-hydroksylację (DBH) i oksydacyjną deaminację (FMO3); istnieją inne enzymy, które są mniej zaangażowane w metabolizm amfetaminy, takie jak ligaza maślanu-CoA i glicyna-N-acylotransferaza. Biodostępność (przy niezmienionym pH przewodu pokarmowego) osiąga 70-75% dla racematu i do 80-83% dla dekstroamfetaminy. Wiązanie z białkami osocza osiąga 15-30% według różnych źródeł u zdrowych osób, objętość dystrybucji jest umiarkowana, substancja aktywnie przechodzi przez barierę krew-mózg ze zmiennym współczynnikiem 17p. T1/2 wynosi około 7-15 godzin, w zależności od wielu czynników, w tym pH moczu (z przyspieszeniem okresu półtrwania przy niższych wartościach). Imax - 15-70 minut. Dawka śmiertelna d-izomeru amfetaminy nie została zbadana, jednak istnieją teoretyczne wnioski dotyczące dużych wartości LD 50 wynoszących 5-10% na podstawie dostępnych ekstrapolowanych danych standardowego racematu siarczanu amfetaminy (98-130 mg/kg). Amfetamina jest eliminowana w prawie takich samych wskaźnikach jakościowych znanych metabolitów, jednak objętość kwasu hipurowego, benzoiloglikuronidu i norefedryny jest znacznie mniejsza (60% wszystkich danych), co wynika ze specyfiki tego racematu w kontekście metabolizmu na poziomie deaminacji. W badaniach na gryzoniach wykazano wyraźny spadek genotoksyczności w przeciwieństwie do standardowego racematu amfetaminy w dawce 4600 mg/ml.
Mechanizm działania.
Farmakodynamiczny mechanizm działania prawie nie różni się od podstawowej formy amfetaminy. Poprzez hamowanie i odwracanie transporterów serotoniny, noradrenaliny i dopaminy, interakcję z TAAR1, co ostatecznie prowadzi do wzrostu stężenia monoamin i katecholamin jednocześnie w szczelinie synaptycznej (szczelina ma szerokość 10-50 nm między błonami, krawędzie są wzmocnione przez kontakty międzykomórkowe). Ważną cechą konkretnie dekstroamfetaminy jest fakt, że powinowactwo prawoskrętnego enancjomeru do TAAR1 jest znacznie większe (według różnych źródeł o 15-30%), a VMAT2 wychwytuje mniejszą ilość tego enancjomeru i minimalne powinowactwo do transportera serotoniny, w przeciwieństwie do lewoskrętnego, a obciążenie takich układów jak CDK5R1, DLG1 i CAMKIIAA jest znacznie mniejsze przy równoważnych efektach klinicznych.
Nie mniej ważny jest fakt naukowy zidentyfikowany przez Novascreen BioSciences Corporation, że ze względu na niższe powinowactwo do szeregu receptorów (a1, a2, b-adrenoreceptorów, mu-opioidowych, histaminowych, CCK, NK, GABA, ETeA i innych), nasilenie zarówno niepożądanych ubocznych efektów klinicznych, jak i innych negatywnych konsekwencji na poziomie molekularnym jest znacznie niższe, co decyduje o pierwszeństwie tej konkretnej formy substancji z zachowaniem odpowiednich pożądanych efektów klinicznych. Efektem netto tych wielu właściwości działania jest to, że d-amfetamina zwiększa "dostępność" lub zdolność koncentracji katecholamin w przestrzeni pozakomórkowej poprzez odwrócenie transportu katecholamin z końcowego końca neuronu, co jest również jedną z cech prawoskrętnego enancjomeru. Wskaźniki hamowania wychwytu [3 H] przez synaptosomy mózgu szczura przez d-enancjomer różnią się i różnią się znacznie od racematu amfetaminy. Dla noradrenaliny Ki = nM przy wartości 45-50, dla dopaminy 82-200, dla 5-HT wskaźniki wahają się od 1840 do 3830 w szczurzych modelach mózgu. Bardziej "miękki" efekt cyklu uzależnienia od tej formy amfetaminy jest konsekwencją stosunkowo niższej nadekspresji FosB w jądrze półleżącym, obecności pozytywnych efektów i braku hamowania CREB przez fosfotazy białkowe i serynowe właśnie ze względu na niższe powinowactwo i wpływ na układy glutaminianergiczne i serotoninowo-ergiczne. Efekty neurochemiczne w porównaniu mają również charakterystyczną zdolność; w badaniach Heala i Wickensa wykryto zmiany w aktywności ruchowej, gdzie jej maksymalna wartość była 3-4 razy mniejsza niż przy przyjmowaniu chlorowodorku amfetaminy lub siarczanu, co jest bezpośrednio związane z szybkością i korektą molekularną odpływu dopaminy w prążkowiu mózgu.

Chociaż eksperymenty in vitro zapewniają dobry wgląd w poszczególne mechanizmy, skuteczność amfetaminy w stosunku do innych pośrednich agonistów monoamin, na przykład klasycznych inhibitorów wychwytu zwrotnego, można oszacować jedynie na podstawie eksperymentów in vivo. Wykorzystaliśmy mikrodializę domózgową z podwójną sondą do zbadania efektów in vivo d- i l-amfetaminy u szczura z samoistnym nadciśnieniem (SHR), który został zaproponowany jako gryzoni model ADHD. Oba izomery amfetaminy w sposób zależny od dawki zwiększały pozakomórkowe stężenie noradrenaliny w korze przedczołowej (PFC) i dopaminy w prążkowiu. Farmakodynamika ich działania jest typowa dla środków uwalniających monoaminy, tj. szybki początek działania ze szczytowym wzrostem wypływu noradrenaliny i dopaminy występującym po 30-45 minutach, duże efekty (400-450% wartości wyjściowej dla noradrenaliny i 700-1500% wartości wyjściowej dla dopaminy), ze stosunkowo szybkim spadkiem po maksimum. Chociaż w niniejszym przeglądzie nie uwzględniono wyników porównawczych, wielkość wzrostów wywołanych przez izomery amfetaminy jest większa niż te zgłaszane dla klasycznych inhibitorów wychwytu zwrotnego, takich jak atomoksetyna lub bupropion, i nie ma pułapu dawka-efekt dla działań amfetaminy.
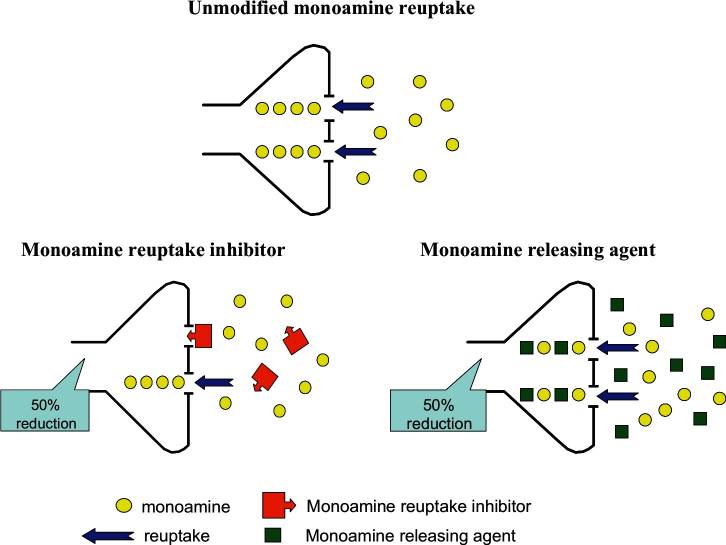
Porównując wpływ leków na wypływ katecholamin w PFC, ważne jest, aby wziąć pod uwagę bardzo nietypową neuroanatomię tego regionu mózgu. Gęstość miejsc DAT na neuronach dopaminergicznych PFC jest bardzo niska, a w konsekwencji większość uwalnianej dopaminy jest sekwestrowana przez NET do neuronów noradrenergicznych. Mimo że na neuronach dopaminergicznych PFC znajduje się niewiele miejsc DAT, ich zdolność wychwytu zwrotnego jest wystarczająca, aby amfetamina wywołała znaczne uwalnianie dopaminy, chociaż sugeruje się, że większość uwalniania dopaminy w PFC pochodzi z neuronów noradrenergicznych. W badaniach Shire Development na modelach in vivo wykazano statystycznie istotną różnicę. D-AMP w różny sposób wpływał na poznawcze komponenty kontroli impulsywnej: odsetek impulsywnych wyborów zmniejszał się przy tym samym poziomie nagrody, co również potwierdza skuteczność tego enancjomeru.
Metody stosowania i dawki.
Rekreacyjna dawka d-enancjomeru amfetaminy zaczyna się od 40-60 mg przy stosowaniu doustnym, w przypadku obecnej tolerancji dawkę początkową można zwiększyć do 120-160 mg przy jednorazowym stosowaniu doustnym. Przy podawaniu donosowym zaleca się stosowanie dawki początkowej 30-50 mg. Podawanie pozajelitowe tej postaci jest dozwolone tylko w przypadku uzyskania czystego roztworu. Wszelkie tabletki lub proszki są zalecane do stosowania wyłącznie po podaniu doustnym i donosowym. Przy podawaniu pozajelitowym dawka początkowa wynosi 0,15-0,24 mg/kg.
Obraz kliniczny zatrucia amfetaminą.
Powyższe objawy są "łagodne", ich nasilenie jest do 40% mniejsze niż w przypadku postaci złożonej. Dlatego takie negatywne działania niepożądane, jak trudności w oddawaniu moczu, zaburzenia rytmu serca, zwiększona częstość akcji serca, podwyższone ciśnienie krwi, zwiększona potliwość, wysoka temperatura ciała, nudności, rozszerzenie źrenic występują wyłącznie przy wysokich dawkach i są proporcjonalnie różne w porównaniu z racematem.
1. Euforia i uczucie zwiększonej energii;
2. Przedłużone czuwanie;
3. Wspaniałe pomysły lub działania;
4. Gwałtowne lub agresywne zachowanie;
5. Uprzedzenia potwierdzające;
6. Labilność nastroju;
7. Zachowanie charakteryzujące się powtarzającymi się stereotypami;
8. Złudzenia słuchowe, wzrokowe lub dotykowe;
9. Zniekształcenie osobowości;
10. Tłumienie apetytu.
Ponadto osoby używające D-AMP muszą mieć co najmniej dwa z następujących objawów, aby mogły zostać zdiagnozowane:
1. Tachykardia;
2. Nadciśnienie tętnicze;
3. Pocenie się i dreszcze gorączkowe;
4. Nudności lub wymioty;
5. Osłabienie mięśni;
6. Ból lub dyskomfort za mostkiem;
7. Pobudzenie psychoruchowe;
8. Rozszerzenie źrenic.
Objawy zatrucia D-AMP obejmują głównie objawy powikłań ze strony układu sercowo-naczyniowego i nerwowego. Zaburzenia oddechowe rozwijają się rzadziej.
Zaburzenia serca: nadciśnienie i tachykardia są najczęstsze przy przyjmowaniu małych dawek. Początkowa bradykardia jest również możliwa ze względu na wzrost napięcia przywspółczulnego. Arytmie (nadkomorowe są częste) mogą być spowodowane kryzysem współczulnym lub blokadą szybkich kanałów sodowych. Niedokrwienie i zawał mięśnia sercowego są spowodowane skurczem naczyń wieńcowych, który osiąga maksimum 30 minut po podaniu donosowym D-AMP i zbiega się z maksymalnym stężeniem leku we krwi. Dalszy skurcz naczyń wieńcowych może rozwinąć się po 90 minutach, co jest związane z akumulacją metabolitów D-AMP. Wzrost agregacji płytek krwi prowadzi do tworzenia się skrzepów krwi w naczyniach wieńcowych. Ponadto wzrasta zapotrzebowanie mięśnia sercowego na tlen. Rzadkim powikłaniem jest pęknięcie aorty.
Specjalne instrukcje, interakcje z innymi substancjami.
Bezwzględnymi przeciwwskazaniami do stosowania jakiejkolwiek formy amfetaminy są: ciężka miażdżyca naczyń krwionośnych, wszelkie objawowe choroby sercowo-naczyniowe, przyjmowanie MAO (i 14 dni po ostatnim użyciu leku z tej grupy), jaskra, nadczynność tarczycy.
Zasada "non-ADIOS":
Bezalkoholowe - nie zaleca się stosowania z alkoholem.
Non-Dissociatives - nie zaleca się stosowania z lekami dysocjacyjnymi.
Non-iMAO - nie zaleca się stosowania z inhibitorami monoaminooksydazy.
Non-Opiates - nie zaleca się stosowania z agonistami receptorów opioidowych.
Non-Stimulators - nie zaleca się stosowania z lekami pobudzającymi.
1. Podczas stosowania D-AMP razem z lekami z grupy inhibitorów PDE-5 zwiększa się ryzyko wystąpienia działań niepożądanych obu substancji. Najczęstsze działania niepożądane: silny ból głowy o charakterze spastycznym, nudności. Częstość występowania ciężkich stanów krytycznych jest niska.
2. Podczas stosowania D-AMP razem z marihuaną istnieje ryzyko wystąpienia podwyższonego ciśnienia krwi, bólu głowy, drobnego drżenia, suchości w jamie ustnej. Prawdopodobieństwo wystąpienia ciężkich stanów krytycznych jest niskie.
3. W przypadku stosowania D-AMP z neuroleptykami/lekami uspokajającymi istnieje wysokie ryzyko zniwelowania głównych efektów działania D-AMP. Prawdopodobieństwo wystąpienia ciężkich stanów krytycznych jest niskie (w przypadkach, gdy nie ma przeciwwskazań do przyjmowania neuroleptyków).
4. Nie zaleca się stosowania D-AMP podczas leczenia lekami przeciwbakteryjnymi, przeciwwirusowymi i przeciwgrzybiczymi, hormonami, antykoagulantami.
5. Nie zaleca się stosowania D-AMP podczas jakichkolwiek manipulacji chirurgicznych oraz w czasie przed i po nich przez określony czas (okres jest określany indywidualnie).
6. Nie zaleca się stosowania D-AMP w przypadku zdiagnozowania jakichkolwiek zaburzeń układu sercowo-naczyniowego, nerek, wątroby, płuc, ośrodkowego układu nerwowego.
7. Nie zaleca się stosowania D-AMP w okresie ciąży i laktacji.
W dwóch wcześniej opublikowanych badaniach Jasinski i Krishnan porównali subiektywne skutki IR d-amfetaminy u doświadczonych ochotników, gdy związki te były podawane dożylnie i doustnie. W badaniu, w którym porównywano te związki po podaniu doustnym, d-amfetamina IR (40 mg (29,6 mg bazy d-amfetaminy)) wywołała statystycznie istotny wzrost w stosunku do placebo w zakresie "Lubienia narkotyków" w skali Kwestionariusza Oceny Narkotyków - Podmiot (DQRS), podczas gdy równoważna dawka d-amf (100 mg, doustnie) nie wywołała takiego efektu. Co więcej, czas wystąpienia szczytowego efektu farmakologicznego d-amfetaminy był znacznie opóźniony w porównaniu z d-amfetaminą IR, wynosząc 3,0 h w porównaniu z 1,5-2,0 h. Gdy d-amfetamina była podawana w zwiększonej dawce 150 mg, znacząco zwiększała wynik DQRS "Drug liking" w stopniu równoważnym do d-amfetaminy IR (40 mg doustnie). Jednak szczytowy efekt wyższej dawki d-amfetaminy był jeszcze bardziej opóźniony i wynosił 4,0 godz. Po zbadaniu drogi dożylnej, d-amfetamina IR (20 mg dożylnie) osiągnęła szczytowy wynik "Lubienia narkotyków" 20 minut po podaniu, co zbiegło się z Cmax w osoczu. W przeciwieństwie do tego, równoważna dawka d-amfetaminy (50 mg dożylnie) nie zwiększyła znacząco "lubienia leku" w porównaniu z placebo, a Cmax d-amfetaminy w osoczu wystąpiło znacznie później, po 2,0 h. Oba związki dały równoważne wartości AUC0-24h, ale w porównaniu z równoważną dawką d-amfetaminy IR, Cmax dla d-amfetaminy w osoczu było trzykrotnie mniejsze dla lisdexamfetaminy, a tmax było trzykrotnie większe.
Pierwsza pomoc w przypadku przedawkowania.
Mechanizm toksyczności jest przede wszystkim związany z nadmiernym zewnątrzkomórkowym stężeniem dopaminy, noradrenaliny i serotoniny. Podstawowy zespół kliniczny obejmuje wyraźne skutki neurologiczne i sercowo-naczyniowe, ale wtórne powikłania mogą obejmować skutki nerkowe, mięśniowe, płucne i żołądkowo-jelitowe. Nadpobudliwość, hipertermia, tachykardia, tachypnea, rozszerzenie źrenic, drżenie, drgawki i zmieniony stan psychiczny to niektóre z najczęstszych oznak i objawów zatrucia amfetaminą. Diagnozę można potwierdzić poprzez wykrycie amfetaminy w treści żołądkowej lub wymiocinach lub poprzez pozytywny wynik badania toksykologicznego moczu na obecność nielegalnych narkotyków. Fałszywie dodatni wynik testu na obecność amfetaminy może wystąpić po przedawkowaniu trazodonu lub bupropionu. Nie ma antidotum na toksyczne działanie amfetaminy, jednak węgiel aktywowany może być stosowany w nagłych wypadkach. U pacjentów, którzy mogą bezpiecznie pić, zaleca się podawanie węgla aktywowanego, od 1 do 2 g/kg do 100 g doustnie, jeśli spożycie nastąpiło w ciągu ostatniej godziny. Zatrucie amfetaminą wymaga postępowania polegającego na opanowaniu zagrażających życiu objawów ze strony ośrodkowego układu nerwowego i układu krążenia w spokojnym otoczeniu.
Wskazania do udania się do szpitala lub wezwania pogotowia ratunkowego: zaburzenia lub brak świadomości, zaburzenia mowy, aktywności ruchowej, brak orientacji w czasie i przestrzeni, silny ból za mostkiem trwający ponad pół godziny, wzrost temperatury ciała o ponad 38,0 C lub hipertermia trwająca ponad pół godziny, wzrost ciśnienia krwi o ponad 180/110 mmHg bez efektu leczenia hipotensyjnego.
1. Leczenie pacjentów z ciśnieniem krwi powyżej 140/95 mm Hg obejmuje jedną tabletkę beta-blokera bez wewnętrznej aktywności sympatykomimetycznej, jedną tabletkę inhibitora ACE, po 30 minutach - jedną tabletkę leku uspokajającego (0,25 mg alprazolamu).
2. U pacjentów z silnym lękiem, atakiem paniki, psychozą: jedna tabletka leku uspokajającego i jedna tabletka neuroleptyku o działaniu uspokajającym, pomoc psychologiczna, psychoterapia w nagłych wypadkach.
3. U pacjentów z bólem mostka, dyskomfortem w klatce piersiowej: jedna tabletka powolnych blokerów kanału wapniowego trzeciej generacji, odruchowo zmniejszająca częstość akcji serca, jedna tabletka inhibitora ACE trzeciej generacji LUB jedna tabletka agonisty działania imidazoliny LUB jedna tabletka ; jeśli zespół bólowy nie stanie się mniej intensywny w ciągu 20 minut, zaleca się udanie się do szpitala.
4. W przypadku wzrostu temperatury ciała o nie więcej niż 37,5 C zaleca się dynamiczną obserwację przez pół godziny. Leczenie farmakologiczne nie jest wymagane. Jeśli hipertermia utrzymuje się przez ponad pół godziny (przy braku przyczyn zewnętrznych), zaleca się udanie się do szpitala.
5. U pacjentów z intensywnymi bólami głowy zaleca się stosowanie leków przeciwskurczowych w połączeniu z uspokajającymi lekami ziołowymi lub uspokajającymi w małych dawkach. Jeśli bólowi głowy towarzyszą wymioty, zaleca się domięśniowe wstrzyknięcie metoklopramidu w dawce 2,0 ml. Izolowane nudności i dyspepsja czynnościowa nie wymagają leczenia farmakologicznego.
6. W przypadku drżenia, umiarkowanych drgawek lub łagodnego pobudzenia psychoruchowego zaleca się stosowanie leków uspokajających. Zdecydowanie odradza się stosowanie neuroleptyków w takich przypadkach.
Lek beta-adrenolityczny, taki jak propranolol, może pomóc w opanowaniu tachyarytmii serca. W przypadku ciężkiego nadciśnienia tętniczego należy rozważyć dożylne podanie nitroprusydku (rozpoczynając od 0,5 do 1 mcg/kg na minutę i miareczkując w razie potrzeby). Należy podawać dożylnie płyny, ponieważ przeciwdziałają one hipertermii, pomagają w utrzymaniu czynności nerek i wspomagają eliminację amfetaminy i jej analogów. W przypadkach silnego pobudzenia klinicyści powinni rozważyć agresywne leczenie w celu uniknięcia nadciśnienia złośliwego, rabdomiolizy, hipertermii i drgawek. Dowody przemawiają za stosowaniem dużych dawek benzodiazepin w leczeniu psychozy i pobudzenia związanych z przedawkowaniem amfetaminy. W przypadkach, w których pobudzenie, delirium i zaburzenia ruchowe nie reagują na benzodiazepiny, terapie drugiego rzutu obejmują leki przeciwpsychotyczne, takie jak ziprasidon lub haloperidol, centralne agoniści receptorów alfa-adrenergicznych, takie jak deksmedetomidyna lub propofol. W ciężkich przypadkach może być konieczne zastosowanie paraliżu nerwowo-mięśniowego, intubacji i aktywnego chłodzenia. U pacjentów z tachykardią należy wykonać EKG i rozważyć telemetrię. Podać dożylnie płyny i zastosować sedację w celu opanowania objawów kardiologicznych. W przypadku ciężkiego nadciśnienia tętniczego należy rozważyć dożylne podanie nitroprusydku. Najlepszym sposobem leczenia rabdomiolizy jest rozpoczęcie podawania 0,9% soli fizjologicznej i monitorowanie kinazy kreatynowej (CK), elektrolitów i kreatyniny.
Istnieją opisy przypadków kardiomiopatii Takotsubo (TTC), znanej również jako kardiomiopatia wywołana stresem, która jest wywoływana przedawkowaniem amfetaminy. W jednym przypadku pacjent zgłosił się na oddział ratunkowy po spożyciu 30 tabletek soli amfetaminy z objawami bólu w klatce piersiowej i duszności. W momencie zgłoszenia enzymy sercowe były podwyższone, elektrokardiogram nie wyróżniał się, a frakcja wyrzutowa (EF) wynosiła od 25% do 30% z ciężką hipokinezą. Jednak 24 godziny później objawy ustąpiły, a powtórne badanie echokardiograficzne wykonane trzy dni później wykazało EF na poziomie 60% bez regionalnych nieprawidłowości ruchu ściany.
Warunki wykrywania i zasady przechowywania.
Zasadniczo przechowywanie racematu amfetaminy, jak również d-enancjomeru, powinno odbywać się w miejscu chronionym przed światłem i wilgocią, najlepiej w temperaturze pokojowej lub w temperaturze co najmniej 5 C i nie wyższej niż 40 C. Można go przechowywać w papierze spożywczym lub w opakowaniach z politereftalanu etylenu bez zawartości metalu.
Po jednorazowym donosowym zażyciu dekstroamfetaminy okres wykrywalności w moczu przy zastosowaniu ekspresowych metod badawczych wynosi około 46-72 godzin, przy zażyciu doustnym do 120-220 godzin. Długotrwałe, systematyczne stosowanie dekstroamfetaminy nie było badane w kontekście identyfikacji metabolitów, choć teoretycznie wiadomo, że istnieje duża szansa na wykrycie głównych metabolitów metodą PFIA lub chromatografii-spektrometrii mas w ciągu 1,5-2 miesięcy od ostatniego użycia amfetaminy (czyli krócej niż w przypadku racematu amfetaminy). Okres wykrywania metabolitów dekstroamfetaminy we włosach wynosi do 2,5-3 miesięcy.
Synteza dekstroamfetaminy z P2P
Właściwości fizykochemiczne i formy substancji.
Zasadniczo dekstroamfetamina, a także racemat amfetaminy, ma wygląd bezbarwnej lotnej oleistej cieczy o charakterystycznym "rybim" zapachu i jest dobrze rozpuszczalna w rozpuszczalnikach organicznych. Jego temperatura wrzenia wynosi 200-203 °C. Enancjomer może mieć wygląd proszku z tworzeniem małych "kamieni" w kolorze białym lub jasnożółtym/kremowym, o słabym zapachu, słabo higroskopijny, częściowo rozpuszczalny w wodzie, gdy jest w postaci tabletki. Najczęściej występuje w postaci siarczanu, chlorowodorku, sacharynianu i bardzo rzadko w postaci fosforanu. Z reguły dekstroamfetamina jest częścią różnych leków, takich jak "Aderral" i "Dexedrine", gdzie występuje w postaci sacharynianu i siarczanu w stężeniach 25% całkowitej objętości. Jest również częścią "Vyvanse", "Elvanse", "Tyvense", gdzie występuje w stanie proaktywnym dimesylanu lizdeksamfetaminy; fermentacja z l-lizyną metabolizuje ją do aktywnej postaci d-amfetaminy; "Dexedrine". Inne nazwy handlowe leków obejmują: Siarczan deksedryny, Afatin, d-Amfetasul, Domafate Obesedrin, Dexten, Maxiton, Sympamin, Simpamina-D, Albemap, Dadex, Ardex, Dexalone, Amsustain, Betafedrina, d-Betafedryna, Diocurb, Dextrostat.
Farmakokinetyka.
Po podaniu amfetamina jest metabolizowana przez hydroksylację, gdzie głównym cytochromem jest CYP2D6, beta-hydroksylację (DBH) i oksydacyjną deaminację (FMO3); istnieją inne enzymy, które są mniej zaangażowane w metabolizm amfetaminy, takie jak ligaza maślanu-CoA i glicyna-N-acylotransferaza. Biodostępność (przy niezmienionym pH przewodu pokarmowego) osiąga 70-75% dla racematu i do 80-83% dla dekstroamfetaminy. Wiązanie z białkami osocza osiąga 15-30% według różnych źródeł u zdrowych osób, objętość dystrybucji jest umiarkowana, substancja aktywnie przechodzi przez barierę krew-mózg ze zmiennym współczynnikiem 17p. T1/2 wynosi około 7-15 godzin, w zależności od wielu czynników, w tym pH moczu (z przyspieszeniem okresu półtrwania przy niższych wartościach). Imax - 15-70 minut. Dawka śmiertelna d-izomeru amfetaminy nie została zbadana, jednak istnieją teoretyczne wnioski dotyczące dużych wartości LD 50 wynoszących 5-10% na podstawie dostępnych ekstrapolowanych danych standardowego racematu siarczanu amfetaminy (98-130 mg/kg). Amfetamina jest eliminowana w prawie takich samych wskaźnikach jakościowych znanych metabolitów, jednak objętość kwasu hipurowego, benzoiloglikuronidu i norefedryny jest znacznie mniejsza (60% wszystkich danych), co wynika ze specyfiki tego racematu w kontekście metabolizmu na poziomie deaminacji. W badaniach na gryzoniach wykazano wyraźny spadek genotoksyczności w przeciwieństwie do standardowego racematu amfetaminy w dawce 4600 mg/ml.
Mechanizm działania.
Farmakodynamiczny mechanizm działania prawie nie różni się od podstawowej formy amfetaminy. Poprzez hamowanie i odwracanie transporterów serotoniny, noradrenaliny i dopaminy, interakcję z TAAR1, co ostatecznie prowadzi do wzrostu stężenia monoamin i katecholamin jednocześnie w szczelinie synaptycznej (szczelina ma szerokość 10-50 nm między błonami, krawędzie są wzmocnione przez kontakty międzykomórkowe). Ważną cechą konkretnie dekstroamfetaminy jest fakt, że powinowactwo prawoskrętnego enancjomeru do TAAR1 jest znacznie większe (według różnych źródeł o 15-30%), a VMAT2 wychwytuje mniejszą ilość tego enancjomeru i minimalne powinowactwo do transportera serotoniny, w przeciwieństwie do lewoskrętnego, a obciążenie takich układów jak CDK5R1, DLG1 i CAMKIIAA jest znacznie mniejsze przy równoważnych efektach klinicznych.
Nie mniej ważny jest fakt naukowy zidentyfikowany przez Novascreen BioSciences Corporation, że ze względu na niższe powinowactwo do szeregu receptorów (a1, a2, b-adrenoreceptorów, mu-opioidowych, histaminowych, CCK, NK, GABA, ETeA i innych), nasilenie zarówno niepożądanych ubocznych efektów klinicznych, jak i innych negatywnych konsekwencji na poziomie molekularnym jest znacznie niższe, co decyduje o pierwszeństwie tej konkretnej formy substancji z zachowaniem odpowiednich pożądanych efektów klinicznych. Efektem netto tych wielu właściwości działania jest to, że d-amfetamina zwiększa "dostępność" lub zdolność koncentracji katecholamin w przestrzeni pozakomórkowej poprzez odwrócenie transportu katecholamin z końcowego końca neuronu, co jest również jedną z cech prawoskrętnego enancjomeru. Wskaźniki hamowania wychwytu [3 H] przez synaptosomy mózgu szczura przez d-enancjomer różnią się i różnią się znacznie od racematu amfetaminy. Dla noradrenaliny Ki = nM przy wartości 45-50, dla dopaminy 82-200, dla 5-HT wskaźniki wahają się od 1840 do 3830 w szczurzych modelach mózgu. Bardziej "miękki" efekt cyklu uzależnienia od tej formy amfetaminy jest konsekwencją stosunkowo niższej nadekspresji FosB w jądrze półleżącym, obecności pozytywnych efektów i braku hamowania CREB przez fosfotazy białkowe i serynowe właśnie ze względu na niższe powinowactwo i wpływ na układy glutaminianergiczne i serotoninowo-ergiczne. Efekty neurochemiczne w porównaniu mają również charakterystyczną zdolność; w badaniach Heala i Wickensa wykryto zmiany w aktywności ruchowej, gdzie jej maksymalna wartość była 3-4 razy mniejsza niż przy przyjmowaniu chlorowodorku amfetaminy lub siarczanu, co jest bezpośrednio związane z szybkością i korektą molekularną odpływu dopaminy w prążkowiu mózgu.
Chociaż eksperymenty in vitro zapewniają dobry wgląd w poszczególne mechanizmy, skuteczność amfetaminy w stosunku do innych pośrednich agonistów monoamin, na przykład klasycznych inhibitorów wychwytu zwrotnego, można oszacować jedynie na podstawie eksperymentów in vivo. Wykorzystaliśmy mikrodializę domózgową z podwójną sondą do zbadania efektów in vivo d- i l-amfetaminy u szczura z samoistnym nadciśnieniem (SHR), który został zaproponowany jako gryzoni model ADHD. Oba izomery amfetaminy w sposób zależny od dawki zwiększały pozakomórkowe stężenie noradrenaliny w korze przedczołowej (PFC) i dopaminy w prążkowiu. Farmakodynamika ich działania jest typowa dla środków uwalniających monoaminy, tj. szybki początek działania ze szczytowym wzrostem wypływu noradrenaliny i dopaminy występującym po 30-45 minutach, duże efekty (400-450% wartości wyjściowej dla noradrenaliny i 700-1500% wartości wyjściowej dla dopaminy), ze stosunkowo szybkim spadkiem po maksimum. Chociaż w niniejszym przeglądzie nie uwzględniono wyników porównawczych, wielkość wzrostów wywołanych przez izomery amfetaminy jest większa niż te zgłaszane dla klasycznych inhibitorów wychwytu zwrotnego, takich jak atomoksetyna lub bupropion, i nie ma pułapu dawka-efekt dla działań amfetaminy.
Porównując wpływ leków na wypływ katecholamin w PFC, ważne jest, aby wziąć pod uwagę bardzo nietypową neuroanatomię tego regionu mózgu. Gęstość miejsc DAT na neuronach dopaminergicznych PFC jest bardzo niska, a w konsekwencji większość uwalnianej dopaminy jest sekwestrowana przez NET do neuronów noradrenergicznych. Mimo że na neuronach dopaminergicznych PFC znajduje się niewiele miejsc DAT, ich zdolność wychwytu zwrotnego jest wystarczająca, aby amfetamina wywołała znaczne uwalnianie dopaminy, chociaż sugeruje się, że większość uwalniania dopaminy w PFC pochodzi z neuronów noradrenergicznych. W badaniach Shire Development na modelach in vivo wykazano statystycznie istotną różnicę. D-AMP w różny sposób wpływał na poznawcze komponenty kontroli impulsywnej: odsetek impulsywnych wyborów zmniejszał się przy tym samym poziomie nagrody, co również potwierdza skuteczność tego enancjomeru.
Metody stosowania i dawki.
Rekreacyjna dawka d-enancjomeru amfetaminy zaczyna się od 40-60 mg przy stosowaniu doustnym, w przypadku obecnej tolerancji dawkę początkową można zwiększyć do 120-160 mg przy jednorazowym stosowaniu doustnym. Przy podawaniu donosowym zaleca się stosowanie dawki początkowej 30-50 mg. Podawanie pozajelitowe tej postaci jest dozwolone tylko w przypadku uzyskania czystego roztworu. Wszelkie tabletki lub proszki są zalecane do stosowania wyłącznie po podaniu doustnym i donosowym. Przy podawaniu pozajelitowym dawka początkowa wynosi 0,15-0,24 mg/kg.
Obraz kliniczny zatrucia amfetaminą.
Powyższe objawy są "łagodne", ich nasilenie jest do 40% mniejsze niż w przypadku postaci złożonej. Dlatego takie negatywne działania niepożądane, jak trudności w oddawaniu moczu, zaburzenia rytmu serca, zwiększona częstość akcji serca, podwyższone ciśnienie krwi, zwiększona potliwość, wysoka temperatura ciała, nudności, rozszerzenie źrenic występują wyłącznie przy wysokich dawkach i są proporcjonalnie różne w porównaniu z racematem.
1. Euforia i uczucie zwiększonej energii;
2. Przedłużone czuwanie;
3. Wspaniałe pomysły lub działania;
4. Gwałtowne lub agresywne zachowanie;
5. Uprzedzenia potwierdzające;
6. Labilność nastroju;
7. Zachowanie charakteryzujące się powtarzającymi się stereotypami;
8. Złudzenia słuchowe, wzrokowe lub dotykowe;
9. Zniekształcenie osobowości;
10. Tłumienie apetytu.
Ponadto osoby używające D-AMP muszą mieć co najmniej dwa z następujących objawów, aby mogły zostać zdiagnozowane:
1. Tachykardia;
2. Nadciśnienie tętnicze;
3. Pocenie się i dreszcze gorączkowe;
4. Nudności lub wymioty;
5. Osłabienie mięśni;
6. Ból lub dyskomfort za mostkiem;
7. Pobudzenie psychoruchowe;
8. Rozszerzenie źrenic.
Objawy zatrucia D-AMP obejmują głównie objawy powikłań ze strony układu sercowo-naczyniowego i nerwowego. Zaburzenia oddechowe rozwijają się rzadziej.
Zaburzenia serca: nadciśnienie i tachykardia są najczęstsze przy przyjmowaniu małych dawek. Początkowa bradykardia jest również możliwa ze względu na wzrost napięcia przywspółczulnego. Arytmie (nadkomorowe są częste) mogą być spowodowane kryzysem współczulnym lub blokadą szybkich kanałów sodowych. Niedokrwienie i zawał mięśnia sercowego są spowodowane skurczem naczyń wieńcowych, który osiąga maksimum 30 minut po podaniu donosowym D-AMP i zbiega się z maksymalnym stężeniem leku we krwi. Dalszy skurcz naczyń wieńcowych może rozwinąć się po 90 minutach, co jest związane z akumulacją metabolitów D-AMP. Wzrost agregacji płytek krwi prowadzi do tworzenia się skrzepów krwi w naczyniach wieńcowych. Ponadto wzrasta zapotrzebowanie mięśnia sercowego na tlen. Rzadkim powikłaniem jest pęknięcie aorty.
Specjalne instrukcje, interakcje z innymi substancjami.
Bezwzględnymi przeciwwskazaniami do stosowania jakiejkolwiek formy amfetaminy są: ciężka miażdżyca naczyń krwionośnych, wszelkie objawowe choroby sercowo-naczyniowe, przyjmowanie MAO (i 14 dni po ostatnim użyciu leku z tej grupy), jaskra, nadczynność tarczycy.
Zasada "non-ADIOS":
Bezalkoholowe - nie zaleca się stosowania z alkoholem.
Non-Dissociatives - nie zaleca się stosowania z lekami dysocjacyjnymi.
Non-iMAO - nie zaleca się stosowania z inhibitorami monoaminooksydazy.
Non-Opiates - nie zaleca się stosowania z agonistami receptorów opioidowych.
Non-Stimulators - nie zaleca się stosowania z lekami pobudzającymi.
1. Podczas stosowania D-AMP razem z lekami z grupy inhibitorów PDE-5 zwiększa się ryzyko wystąpienia działań niepożądanych obu substancji. Najczęstsze działania niepożądane: silny ból głowy o charakterze spastycznym, nudności. Częstość występowania ciężkich stanów krytycznych jest niska.
2. Podczas stosowania D-AMP razem z marihuaną istnieje ryzyko wystąpienia podwyższonego ciśnienia krwi, bólu głowy, drobnego drżenia, suchości w jamie ustnej. Prawdopodobieństwo wystąpienia ciężkich stanów krytycznych jest niskie.
3. W przypadku stosowania D-AMP z neuroleptykami/lekami uspokajającymi istnieje wysokie ryzyko zniwelowania głównych efektów działania D-AMP. Prawdopodobieństwo wystąpienia ciężkich stanów krytycznych jest niskie (w przypadkach, gdy nie ma przeciwwskazań do przyjmowania neuroleptyków).
4. Nie zaleca się stosowania D-AMP podczas leczenia lekami przeciwbakteryjnymi, przeciwwirusowymi i przeciwgrzybiczymi, hormonami, antykoagulantami.
5. Nie zaleca się stosowania D-AMP podczas jakichkolwiek manipulacji chirurgicznych oraz w czasie przed i po nich przez określony czas (okres jest określany indywidualnie).
6. Nie zaleca się stosowania D-AMP w przypadku zdiagnozowania jakichkolwiek zaburzeń układu sercowo-naczyniowego, nerek, wątroby, płuc, ośrodkowego układu nerwowego.
7. Nie zaleca się stosowania D-AMP w okresie ciąży i laktacji.
W dwóch wcześniej opublikowanych badaniach Jasinski i Krishnan porównali subiektywne skutki IR d-amfetaminy u doświadczonych ochotników, gdy związki te były podawane dożylnie i doustnie. W badaniu, w którym porównywano te związki po podaniu doustnym, d-amfetamina IR (40 mg (29,6 mg bazy d-amfetaminy)) wywołała statystycznie istotny wzrost w stosunku do placebo w zakresie "Lubienia narkotyków" w skali Kwestionariusza Oceny Narkotyków - Podmiot (DQRS), podczas gdy równoważna dawka d-amf (100 mg, doustnie) nie wywołała takiego efektu. Co więcej, czas wystąpienia szczytowego efektu farmakologicznego d-amfetaminy był znacznie opóźniony w porównaniu z d-amfetaminą IR, wynosząc 3,0 h w porównaniu z 1,5-2,0 h. Gdy d-amfetamina była podawana w zwiększonej dawce 150 mg, znacząco zwiększała wynik DQRS "Drug liking" w stopniu równoważnym do d-amfetaminy IR (40 mg doustnie). Jednak szczytowy efekt wyższej dawki d-amfetaminy był jeszcze bardziej opóźniony i wynosił 4,0 godz. Po zbadaniu drogi dożylnej, d-amfetamina IR (20 mg dożylnie) osiągnęła szczytowy wynik "Lubienia narkotyków" 20 minut po podaniu, co zbiegło się z Cmax w osoczu. W przeciwieństwie do tego, równoważna dawka d-amfetaminy (50 mg dożylnie) nie zwiększyła znacząco "lubienia leku" w porównaniu z placebo, a Cmax d-amfetaminy w osoczu wystąpiło znacznie później, po 2,0 h. Oba związki dały równoważne wartości AUC0-24h, ale w porównaniu z równoważną dawką d-amfetaminy IR, Cmax dla d-amfetaminy w osoczu było trzykrotnie mniejsze dla lisdexamfetaminy, a tmax było trzykrotnie większe.
Pierwsza pomoc w przypadku przedawkowania.
Mechanizm toksyczności jest przede wszystkim związany z nadmiernym zewnątrzkomórkowym stężeniem dopaminy, noradrenaliny i serotoniny. Podstawowy zespół kliniczny obejmuje wyraźne skutki neurologiczne i sercowo-naczyniowe, ale wtórne powikłania mogą obejmować skutki nerkowe, mięśniowe, płucne i żołądkowo-jelitowe. Nadpobudliwość, hipertermia, tachykardia, tachypnea, rozszerzenie źrenic, drżenie, drgawki i zmieniony stan psychiczny to niektóre z najczęstszych oznak i objawów zatrucia amfetaminą. Diagnozę można potwierdzić poprzez wykrycie amfetaminy w treści żołądkowej lub wymiocinach lub poprzez pozytywny wynik badania toksykologicznego moczu na obecność nielegalnych narkotyków. Fałszywie dodatni wynik testu na obecność amfetaminy może wystąpić po przedawkowaniu trazodonu lub bupropionu. Nie ma antidotum na toksyczne działanie amfetaminy, jednak węgiel aktywowany może być stosowany w nagłych wypadkach. U pacjentów, którzy mogą bezpiecznie pić, zaleca się podawanie węgla aktywowanego, od 1 do 2 g/kg do 100 g doustnie, jeśli spożycie nastąpiło w ciągu ostatniej godziny. Zatrucie amfetaminą wymaga postępowania polegającego na opanowaniu zagrażających życiu objawów ze strony ośrodkowego układu nerwowego i układu krążenia w spokojnym otoczeniu.
Wskazania do udania się do szpitala lub wezwania pogotowia ratunkowego: zaburzenia lub brak świadomości, zaburzenia mowy, aktywności ruchowej, brak orientacji w czasie i przestrzeni, silny ból za mostkiem trwający ponad pół godziny, wzrost temperatury ciała o ponad 38,0 C lub hipertermia trwająca ponad pół godziny, wzrost ciśnienia krwi o ponad 180/110 mmHg bez efektu leczenia hipotensyjnego.
1. Leczenie pacjentów z ciśnieniem krwi powyżej 140/95 mm Hg obejmuje jedną tabletkę beta-blokera bez wewnętrznej aktywności sympatykomimetycznej, jedną tabletkę inhibitora ACE, po 30 minutach - jedną tabletkę leku uspokajającego (0,25 mg alprazolamu).
2. U pacjentów z silnym lękiem, atakiem paniki, psychozą: jedna tabletka leku uspokajającego i jedna tabletka neuroleptyku o działaniu uspokajającym, pomoc psychologiczna, psychoterapia w nagłych wypadkach.
3. U pacjentów z bólem mostka, dyskomfortem w klatce piersiowej: jedna tabletka powolnych blokerów kanału wapniowego trzeciej generacji, odruchowo zmniejszająca częstość akcji serca, jedna tabletka inhibitora ACE trzeciej generacji LUB jedna tabletka agonisty działania imidazoliny LUB jedna tabletka ; jeśli zespół bólowy nie stanie się mniej intensywny w ciągu 20 minut, zaleca się udanie się do szpitala.
4. W przypadku wzrostu temperatury ciała o nie więcej niż 37,5 C zaleca się dynamiczną obserwację przez pół godziny. Leczenie farmakologiczne nie jest wymagane. Jeśli hipertermia utrzymuje się przez ponad pół godziny (przy braku przyczyn zewnętrznych), zaleca się udanie się do szpitala.
5. U pacjentów z intensywnymi bólami głowy zaleca się stosowanie leków przeciwskurczowych w połączeniu z uspokajającymi lekami ziołowymi lub uspokajającymi w małych dawkach. Jeśli bólowi głowy towarzyszą wymioty, zaleca się domięśniowe wstrzyknięcie metoklopramidu w dawce 2,0 ml. Izolowane nudności i dyspepsja czynnościowa nie wymagają leczenia farmakologicznego.
6. W przypadku drżenia, umiarkowanych drgawek lub łagodnego pobudzenia psychoruchowego zaleca się stosowanie leków uspokajających. Zdecydowanie odradza się stosowanie neuroleptyków w takich przypadkach.
Lek beta-adrenolityczny, taki jak propranolol, może pomóc w opanowaniu tachyarytmii serca. W przypadku ciężkiego nadciśnienia tętniczego należy rozważyć dożylne podanie nitroprusydku (rozpoczynając od 0,5 do 1 mcg/kg na minutę i miareczkując w razie potrzeby). Należy podawać dożylnie płyny, ponieważ przeciwdziałają one hipertermii, pomagają w utrzymaniu czynności nerek i wspomagają eliminację amfetaminy i jej analogów. W przypadkach silnego pobudzenia klinicyści powinni rozważyć agresywne leczenie w celu uniknięcia nadciśnienia złośliwego, rabdomiolizy, hipertermii i drgawek. Dowody przemawiają za stosowaniem dużych dawek benzodiazepin w leczeniu psychozy i pobudzenia związanych z przedawkowaniem amfetaminy. W przypadkach, w których pobudzenie, delirium i zaburzenia ruchowe nie reagują na benzodiazepiny, terapie drugiego rzutu obejmują leki przeciwpsychotyczne, takie jak ziprasidon lub haloperidol, centralne agoniści receptorów alfa-adrenergicznych, takie jak deksmedetomidyna lub propofol. W ciężkich przypadkach może być konieczne zastosowanie paraliżu nerwowo-mięśniowego, intubacji i aktywnego chłodzenia. U pacjentów z tachykardią należy wykonać EKG i rozważyć telemetrię. Podać dożylnie płyny i zastosować sedację w celu opanowania objawów kardiologicznych. W przypadku ciężkiego nadciśnienia tętniczego należy rozważyć dożylne podanie nitroprusydku. Najlepszym sposobem leczenia rabdomiolizy jest rozpoczęcie podawania 0,9% soli fizjologicznej i monitorowanie kinazy kreatynowej (CK), elektrolitów i kreatyniny.
Istnieją opisy przypadków kardiomiopatii Takotsubo (TTC), znanej również jako kardiomiopatia wywołana stresem, która jest wywoływana przedawkowaniem amfetaminy. W jednym przypadku pacjent zgłosił się na oddział ratunkowy po spożyciu 30 tabletek soli amfetaminy z objawami bólu w klatce piersiowej i duszności. W momencie zgłoszenia enzymy sercowe były podwyższone, elektrokardiogram nie wyróżniał się, a frakcja wyrzutowa (EF) wynosiła od 25% do 30% z ciężką hipokinezą. Jednak 24 godziny później objawy ustąpiły, a powtórne badanie echokardiograficzne wykonane trzy dni później wykazało EF na poziomie 60% bez regionalnych nieprawidłowości ruchu ściany.
Warunki wykrywania i zasady przechowywania.
Zasadniczo przechowywanie racematu amfetaminy, jak również d-enancjomeru, powinno odbywać się w miejscu chronionym przed światłem i wilgocią, najlepiej w temperaturze pokojowej lub w temperaturze co najmniej 5 C i nie wyższej niż 40 C. Można go przechowywać w papierze spożywczym lub w opakowaniach z politereftalanu etylenu bez zawartości metalu.
Po jednorazowym donosowym zażyciu dekstroamfetaminy okres wykrywalności w moczu przy zastosowaniu ekspresowych metod badawczych wynosi około 46-72 godzin, przy zażyciu doustnym do 120-220 godzin. Długotrwałe, systematyczne stosowanie dekstroamfetaminy nie było badane w kontekście identyfikacji metabolitów, choć teoretycznie wiadomo, że istnieje duża szansa na wykrycie głównych metabolitów metodą PFIA lub chromatografii-spektrometrii mas w ciągu 1,5-2 miesięcy od ostatniego użycia amfetaminy (czyli krócej niż w przypadku racematu amfetaminy). Okres wykrywania metabolitów dekstroamfetaminy we włosach wynosi do 2,5-3 miesięcy.
Last edited:
