G.Patton
Expert
- Joined
- Jul 5, 2021
- Messages
- 2,659
- Solutions
- 3
- Reaction score
- 2,734
- Points
- 113
- Deals
- 1
Introdução.
Este ficheiro trata da síntese do GHB e de compostos relacionados. É altamente perigoso tentar uma síntese de GHB sem o conhecimento adequado de química orgânica prática. A forma mais simples de produzir GHB é através da hidrólise da lactona correspondente (um éster intramolecular cíclico) para o hidroxiácido desejado. A hidrólise do éster pode ser efectuada de duas formas: Uma reação catalisada por ácido ou uma reação catalisada por base. A reação catalisada por uma base é a nossa escolha aqui porque a reação não é reversível como a reação catalisada por um ácido e, portanto, obteremos rendimentos mais elevados e obteremos o sal de sódio do GHB, uma vez que o ácido livre não é estável e ciclizará imediatamente em gama-butirolactona novamente.
Transformação da gama-butirolactona em gama-hidroxibutirato de sódio (Na-GHB).
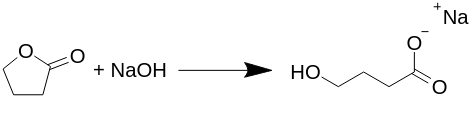
A reação ocorre de forma equimolar (reage o mesmo número de moléculas) e não há subprodutos produzidos nesta reação, como gás hidrogénio, água ou qualquer outra coisa, como proposto em vários outros textos. Todas as preparações publicadas de GHB, ou mais corretamente de Na-GHB, refluxam butirolactona com hidróxido de sódio em vários solventes, geralmente em álcool aquoso, mas isso não é necessário.
Propriedades físico-químicas.
gama-butirolactona.
Mol wt 86.09; mp -43.53 °C; bp 204°C; d 1.12 g/ml
CAS No: [96-48-0]
Miscível com água, solúvel em metanol, etanol, acetona, éter, benzeno
LD50: 1720 mg/kg (oral, rato) 1540 mg/kg (oral, rato)
Utilizações: Solvente, removedor de tinta, eletrólito de condensador, em química orgânica
Sinónimos: GBL, BLO, butirolactona, lactona do ácido gama-hidroxibutírico, 1,2-butanolida, 1,4-butanolida, 4-butanolida, 2-oxanolona, tetra-hidro-2-furanona, di-hidro-2(3H)-furanona.
GHB de sódio.
Mol wt 126.09; mp 145-146 °C
N.o CAS: [502-85-2]
LD50:2700 mg/kg (oral, rato)
Sinónimos: Gamma-OH, oxibato de sódio, gama-oxibutirato de sódio, Somatomax PM, Wy-3478, NSC-84223, Somsanit, Anetamina.
GHB de potássio.
Mol wt: 142.20
GHB de cálcio.
Mol wt246,16; mp 164-166 °C, 166-168 °C.
GHB de magnésio.
Mol wt 230,39; mp (anidro) 172-174 °C; tetra-hidrato 118-120 °C; penta-hidrato 76-78 °C.
Mol wt 86.09; mp -43.53 °C; bp 204°C; d 1.12 g/ml
CAS No: [96-48-0]
Miscível com água, solúvel em metanol, etanol, acetona, éter, benzeno
LD50: 1720 mg/kg (oral, rato) 1540 mg/kg (oral, rato)
Utilizações: Solvente, removedor de tinta, eletrólito de condensador, em química orgânica
Sinónimos: GBL, BLO, butirolactona, lactona do ácido gama-hidroxibutírico, 1,2-butanolida, 1,4-butanolida, 4-butanolida, 2-oxanolona, tetra-hidro-2-furanona, di-hidro-2(3H)-furanona.
GHB de sódio.
Mol wt 126.09; mp 145-146 °C
N.o CAS: [502-85-2]
LD50:2700 mg/kg (oral, rato)
Sinónimos: Gamma-OH, oxibato de sódio, gama-oxibutirato de sódio, Somatomax PM, Wy-3478, NSC-84223, Somsanit, Anetamina.
GHB de potássio.
Mol wt: 142.20
GHB de cálcio.
Mol wt246,16; mp 164-166 °C, 166-168 °C.
GHB de magnésio.
Mol wt 230,39; mp (anidro) 172-174 °C; tetra-hidrato 118-120 °C; penta-hidrato 76-78 °C.
Procedimentos laboratoriais para a síntese de sais de GHB.
Seguir os procedimentos comuns de segurança no laboratório. Usar uma bata de laboratório e óculos de proteção. Vai trabalhar com soluções cáusticas e solventes quentes! Esteja consciente dos riscos associados ao fabrico de GHB! Nunca trabalhe sozinho!
GHB de sódio.
Procedimento:
Dissolver 130 gramas (3,25 moles) de hidróxido de sódio puro em 400 ml de água destilada num balão de fundo redondo de três gargalos de 1000 ml, agitando. A dissolução é exotérmica e a solução aquece. Pode utilizar-se um banho de água fria para regular a temperatura. Depois de tudo se ter dissolvido até formar uma solução límpida, adicionar lentamente 250 ml (280 g, 3,25 moles) de gama-butirolactona em porções de 50 ml, com boa agitação. Recomenda-se a utilização de um funil de decantação. A adição de gama-butirolactona à solução de hidróxido de sódio é também exotérmica e, se for adicionada demasiado depressa, a solução começará a ferver, o que não é desejável. Mantenha o controlo da temperatura com um termómetro imerso. A adição da gama-butirolactona demorará entre 20 a 30 minutos. Quando tudo tiver sido adicionado, deixe a mistura reagir durante mais 10 minutos, mexendo ocasionalmente.
Agora é altura de verificar se a reação está completa, verificando o pH com papel de pH universal. O nosso objetivo é obter um pH de 7-8. Se o pH for demasiado elevado (pH > 8), adicionar 10 ml de gama-butirolactona e deixar reagir durante mais alguns minutos. Se o pH for demasiado baixo (pH < 7), adicionar alguns ml de solução aq. de NaOH concentrada. Continuar assim até que o pH esteja dentro dos limites desejados.
A solução é perfeitamente límpida e tem um sabor ligeiramente salgado. Pode ser ligeiramente amarelada, mas não muito, se se tiver utilizado butirolactona suficientemente pura (a destilação da lactona antes da utilização resolve este problema, b.p. 204 °C). Se se utilizar um ácido para neutralizar uma solução demasiado básica (em vez de adicionar mais lactona), os cristais do sal de sódio do ácido podem precipitar na solução e o sabor fica seriamente afetado. A solução final será de cerca de 750 ml, 50% NaGHB. A solução pode ser concentrada (por ebulição do excesso de água) até ~600 ml sem cristalizar à temperatura ambiente, mas se for concentrada até ~500 ml, solidificará invariavelmente.
Agora é altura de verificar se a reação está completa, verificando o pH com papel de pH universal. O nosso objetivo é obter um pH de 7-8. Se o pH for demasiado elevado (pH > 8), adicionar 10 ml de gama-butirolactona e deixar reagir durante mais alguns minutos. Se o pH for demasiado baixo (pH < 7), adicionar alguns ml de solução aq. de NaOH concentrada. Continuar assim até que o pH esteja dentro dos limites desejados.
A solução é perfeitamente límpida e tem um sabor ligeiramente salgado. Pode ser ligeiramente amarelada, mas não muito, se se tiver utilizado butirolactona suficientemente pura (a destilação da lactona antes da utilização resolve este problema, b.p. 204 °C). Se se utilizar um ácido para neutralizar uma solução demasiado básica (em vez de adicionar mais lactona), os cristais do sal de sódio do ácido podem precipitar na solução e o sabor fica seriamente afetado. A solução final será de cerca de 750 ml, 50% NaGHB. A solução pode ser concentrada (por ebulição do excesso de água) até ~600 ml sem cristalizar à temperatura ambiente, mas se for concentrada até ~500 ml, solidificará invariavelmente.
Preparação de GHB de sódio utilizando bicarbonato de sódio (bicarbonato de sódio, NaHCO3).
Adicionar 273 g de NaHCO3 (3,25 moles) a 1125 mL de água destilada num balão de fundo redondo de três gargalos. Levar lentamente a solução a ferver enquanto se agita com uma vareta de vidro ou similar. Todo o bicarbonato de sódio se dissolverá. O dióxido de carbono será visto a sair da solução à medida que esta começa a ferver. Isto é o bicarbonato de sódio a decompor-se numa base ligeiramente forte, o carbonato de sódio.
Reduzir o calor para uma fervura ligeira e adicionar lentamente 250 ml de gama-butirolactona (280 g, 3,25 moles). A adição não é imediatamente exotérmica, como na síntese do hidróxido de sódio. Manter esta solução em ebulição ligeira durante 30 minutos. Verificar o pH com papel de pH universal. O nosso objetivo é obter um pH de cerca de 7, mas qualquer valor entre 6 e 8 é perfeitamente seguro. Se o pH for demasiado elevado, adicionar uma pequena quantidade de GBL e continuar a refluxar.
A solução será perfeitamente límpida e deverá ser absolutamente incolor. Se não for perfeitamente incolor, ou seja, se tiver sido utilizada butirolactona ligeiramente impura e a solução tiver adquirido uma cor amarela clara, adicionar cerca de 100 mL de carvão ativado. Deixar ferver durante 10 minutos. Arrefecer a solução e filtrar, lavando o carvão ativado duas ou três vezes com porções de 50 ml de água fria. Nesta síntese, serão produzidos 410 g de NaGHB. Esta solução pode ser concentrada a cerca de 50% de NaGHB antes de começar a cristalizar. Se desejar obter um pó, aqueça até que a temperatura da solução atinja 150 °C, depois verta-a para um prato de pirex arrefecido e deixe-a arrefecer e solidificar. Esta síntese é perfeita para ser usada quando não há hidróxido de sódio de grau ACS, alimentar ou eletrónico disponível.
A solução será perfeitamente límpida e deverá ser absolutamente incolor. Se não for perfeitamente incolor, ou seja, se tiver sido utilizada butirolactona ligeiramente impura e a solução tiver adquirido uma cor amarela clara, adicionar cerca de 100 mL de carvão ativado. Deixar ferver durante 10 minutos. Arrefecer a solução e filtrar, lavando o carvão ativado duas ou três vezes com porções de 50 ml de água fria. Nesta síntese, serão produzidos 410 g de NaGHB. Esta solução pode ser concentrada a cerca de 50% de NaGHB antes de começar a cristalizar. Se desejar obter um pó, aqueça até que a temperatura da solução atinja 150 °C, depois verta-a para um prato de pirex arrefecido e deixe-a arrefecer e solidificar. Esta síntese é perfeita para ser usada quando não há hidróxido de sódio de grau ACS, alimentar ou eletrónico disponível.
GHB de potássio.
Use a síntese de etanol descrita acima para o GHB de sódio, mas substitua os 130 gramas de NaOH por 182 gramas de KOH (este cálculo é baseado no átomo de K mais pesado e no maior teor de água do KOH em relação ao NaOH). A utilização de KOH dá aos utilizadores de K-GHB o suplemento de potássio que alguns dizem ser necessário em relação à administração de GHB. Não esquecer que o K-GHB (em pó) é ligeiramente menos ativo (em peso) do que o Na-GHB, uma vez que o ião K é mais pesado do que o Na. As diferenças entre o K-GHB e o Na-GHB residem no facto de o sal de K ser mais solúvel em água do que o sal de Na e de o sabor ser mais parecido com sal/alcaçuz do que com o sabor a sal/sabão do Na-GHB.
GHB de cálcio.
74 g de hidróxido de cálcio analiticamente puro são suspensos em 200 ml de água destilada. São adicionados 160 ml de 4-butirolactona em porções (cada porção cerca de 5 a 10 ml) e sob agitação a esta suspensão à temperatura ambiente. Após a adição de 20 ml, a mistura reacional aquece até cerca de 50 °C a 60 °C. A adição de 4-butirolactona é controlada de modo a que a temperatura se mantenha entre cerca de 50 °C e 60 °C, o que demora cerca de 1 hora. Durante este tempo, o hidróxido de cálcio dissolveu-se praticamente por completo. O material de reação está contaminado com um ligeiro precipitado amarelo-ferrugem. Dilui-se com 300 ml de metanol, deixa-se repousar durante 4 horas e filtra-se através de um filtro de pregas. O filtrado límpido é cuidadosamente tratado com 200 ml de acetona, de modo a que, após cada porção de acetona que provoca um precipitado, se dê tempo para que este se redissolva. Obtém-se uma solução límpida e aquosa, que é colocada para cristalização. Após duas horas de repouso, começam a depositar-se cristais incolores. Neste estado, a cristalização é acelerada pela adição contínua de acetona (num total de 100 ml). O tempo de cristalização é de 24 horas. Os cristais são aspirados e lavados inicialmente com 50 ml de metanol e depois adicionalmente com 60 ml de acetona. Os cristais são secos a temperaturas de cerca de 60 °C a 80 °C numa estufa. Rendimento: 230 g. Ponto de fusão 166-168 °C. (imediatamente). O produto é o sal de cálcio não higroscópico e isento de água do ácido 4-hidroxibutírico. A solução aquosa tem um valor de pH de 7 a 7,5. O sal pode ser armazenado durante o tempo desejado e não se altera com o ar. Mesmo após armazenamento, não é atraída água do ar.
O resíduo cristaliza numa massa de cristais incolores, que é depois seca a temperaturas de cerca de 60 °C a 80 °C. Rendimento: cerca de 105 g. Ponto de fusão 164-166 °C. O produto é o cálcio di-(4-hidroxibutírico). A recristalização faz-se dissolvendo o produto num pouco de metanol, adicionando-lhe acetona até à turvação e cristalizando-o a frio.
Em vez de metanol, podem utilizar-se etanol e isopropanol para a recristalização, com o mesmo êxito. Sem empregar álcoois contendo água como meio de recristalização ou como aditivo da recristalização e purificação, não se obtêm sais de cálcio estáveis e, em particular, não higroscópicos. O teor de água dos álcoois deve ser de cerca de 3-10% em volume. O produto final assim obtido dissolve-se facilmente em água, não é hidroscópico e tem um odor aromático agradável.
O resíduo cristaliza numa massa de cristais incolores, que é depois seca a temperaturas de cerca de 60 °C a 80 °C. Rendimento: cerca de 105 g. Ponto de fusão 164-166 °C. O produto é o cálcio di-(4-hidroxibutírico). A recristalização faz-se dissolvendo o produto num pouco de metanol, adicionando-lhe acetona até à turvação e cristalizando-o a frio.
Em vez de metanol, podem utilizar-se etanol e isopropanol para a recristalização, com o mesmo êxito. Sem empregar álcoois contendo água como meio de recristalização ou como aditivo da recristalização e purificação, não se obtêm sais de cálcio estáveis e, em particular, não higroscópicos. O teor de água dos álcoois deve ser de cerca de 3-10% em volume. O produto final assim obtido dissolve-se facilmente em água, não é hidroscópico e tem um odor aromático agradável.
GHB de magnésio .
60 g de hidróxido de magnésio (grau analítico) são suspensos em 200 ml de água da torneira, sob agitação. Numa corrente e sob agitação, misturam-se 160 ml de butirolactona nesta suspensão. Em seguida, a mistura é aquecida num banho de água durante 6 horas, sob agitação, num balão de 2 litros. O hidróxido de magnésio dissolve-se praticamente por completo. O balão é deixado em repouso durante a noite, enquanto os contaminantes se depositam e a solução é decantada sem esforço do depósito de contaminantes. O decantado aquoso é inicialmente agitado com 100 ml de acetona durante 10 minutos. O líquido xaroposo incolor, que agora se tornou mais viscoso, é misturado novamente com 100 ml de acetona, como descrito acima, a acetona é novamente removida por decantação e o xarope incolor e bastante viscoso é deixado à temperatura ambiente durante cerca de 2 a 4 horas. Solidifica-se numa massa cristalina incolor, que é triturada num almofariz e seca ao ar durante várias horas. Ponto de fusão 76 °C a 78 °C. Rendimento: 314 g na forma analiticamente pura.
Este sal de magnésio contém cerca de 5 moles de água de hidratação. Não é hidroscópico, é estável e pode ser armazenado durante longos períodos de tempo arbitrários. Ao secar durante várias horas entre 40 °C e 50 °C, perde parte da sua água de cristalização (1 mol) e funde-se a 118 °C a 120 °C. O 4-hidroxibutirato de magnésio isento de água pode ser produzido por remoção de água por sublimação e/ou evaporação de água sob pressão parcial reduzida de água e a temperatura elevada, ou por cristalização a partir de uma solução contendo um solvente orgânico. O sal isento de água funde a 172-174 °C. A análise química mostra 10,50 por cento em peso de magnésio (calculado 10,55% em peso de magnésio). Todas as modificações são não higroscópicas e estáveis durante o armazenamento. 1 g do sal de magnésio dissolve-se em 2 ml de água à temperatura ambiente, o pH da solução aquosa é 7. Dissolve-se facilmente em água, metanol e etanol, não se dissolve em éter e hidrocarbonetos, não é higroscópico, é armazenável e tem um odor aromático agradável.
Este sal de magnésio contém cerca de 5 moles de água de hidratação. Não é hidroscópico, é estável e pode ser armazenado durante longos períodos de tempo arbitrários. Ao secar durante várias horas entre 40 °C e 50 °C, perde parte da sua água de cristalização (1 mol) e funde-se a 118 °C a 120 °C. O 4-hidroxibutirato de magnésio isento de água pode ser produzido por remoção de água por sublimação e/ou evaporação de água sob pressão parcial reduzida de água e a temperatura elevada, ou por cristalização a partir de uma solução contendo um solvente orgânico. O sal isento de água funde a 172-174 °C. A análise química mostra 10,50 por cento em peso de magnésio (calculado 10,55% em peso de magnésio). Todas as modificações são não higroscópicas e estáveis durante o armazenamento. 1 g do sal de magnésio dissolve-se em 2 ml de água à temperatura ambiente, o pH da solução aquosa é 7. Dissolve-se facilmente em água, metanol e etanol, não se dissolve em éter e hidrocarbonetos, não é higroscópico, é armazenável e tem um odor aromático agradável.
Outros sais.
Os sais de lítio e de amónio do GHB seriam perigosos de ingerir. O ião de lítio é tóxico e, juntamente com a lactona NH3, transforma-se em pirrolidona.
Síntese Perguntas e Respostas.
P: Posso usar lixívia em vez de hidróxido de sódio puro?
R: Não, isso pode ter resultados imprevisíveis para a sua saúde. A lixívia das lojas de ferragens não tem nem de perto nem de longe os critérios de pureza rigorosos de, por exemplo, grau alimentar, grau ACS ou grau eletrónico. Algumas pessoas contam histórias de sucesso utilizando lixívia, o que é realmente possível, mas, como já foi dito, os resultados são imprevisíveis.
P: Não tenho os objectos de vidro que dizem ser necessários, posso ferver a solução numa panela no fogão?
R: Não, não pode. O hidróxido de sódio corroerá o metal e diversos iões metálicos entrarão no seu produto. Pode, claro, utilizar material de vidro mais simples do que nas minhas sugestões e fazer os ajustes necessários ao procedimento.
P: Não consigo recristalizar o Na-GHB a partir do etanol. Forma-se uma confusão pegajosa.
R: O seu Na-GHB não está seco ou o seu etanol não é anidro. A água torna a recristalização quase impossível. O facto de o GHB sódico ser deliquescente (higroscópico) não melhora a situação. É necessário secar bem o GHB, de preferência num exsicador a vácuo, antes de tentar a recristalização ou qualquer outra alternativa improvisada. O etanol que tenciona utilizar (geralmente fornecido com uma pureza de 95%, sendo o restante água) deve ser seco por secagem sobre sulfato de cálcio anidro, seguida de destilação a partir de óxido de cálcio, tomando as medidas adequadas para excluir a humidade da reação.
P: Onde posso comprar butirolactona/É seguro comprar butirolactona?
R: Não faço ideia de como está a situação no seu país. As respostas a estas perguntas dependem muito de quem és e de onde vives. No entanto, podes contactar qualquer um dos muitos vendedores de kits de GHB que podem ser encontrados online.
R: Não, isso pode ter resultados imprevisíveis para a sua saúde. A lixívia das lojas de ferragens não tem nem de perto nem de longe os critérios de pureza rigorosos de, por exemplo, grau alimentar, grau ACS ou grau eletrónico. Algumas pessoas contam histórias de sucesso utilizando lixívia, o que é realmente possível, mas, como já foi dito, os resultados são imprevisíveis.
P: Não tenho os objectos de vidro que dizem ser necessários, posso ferver a solução numa panela no fogão?
R: Não, não pode. O hidróxido de sódio corroerá o metal e diversos iões metálicos entrarão no seu produto. Pode, claro, utilizar material de vidro mais simples do que nas minhas sugestões e fazer os ajustes necessários ao procedimento.
P: Não consigo recristalizar o Na-GHB a partir do etanol. Forma-se uma confusão pegajosa.
R: O seu Na-GHB não está seco ou o seu etanol não é anidro. A água torna a recristalização quase impossível. O facto de o GHB sódico ser deliquescente (higroscópico) não melhora a situação. É necessário secar bem o GHB, de preferência num exsicador a vácuo, antes de tentar a recristalização ou qualquer outra alternativa improvisada. O etanol que tenciona utilizar (geralmente fornecido com uma pureza de 95%, sendo o restante água) deve ser seco por secagem sobre sulfato de cálcio anidro, seguida de destilação a partir de óxido de cálcio, tomando as medidas adequadas para excluir a humidade da reação.
P: Onde posso comprar butirolactona/É seguro comprar butirolactona?
R: Não faço ideia de como está a situação no seu país. As respostas a estas perguntas dependem muito de quem és e de onde vives. No entanto, podes contactar qualquer um dos muitos vendedores de kits de GHB que podem ser encontrados online.
Precursores.
O precursor óbvio para a síntese de GHB é a gama-butirolactona. Esta pode ser produzida a partir de precursores como o tetra-hidrofurano (THF) com oxidantes como o tetróxido de ruténio, o hipoclorito de cálcio e o ácido nítrico. Podem também ser utilizados derivados do ácido 4-halo-butírico (cloro, bromo, iodo). Como na síntese seguinte, podem ser convertidos em gama-butirolactona por destilação com metóxido de sódio.
Gama-butirolactona a partir do ácido 4-bromobutírico
A uma solução de 7,8 g de sódio em 500 ml de álcool absoluto foram adicionados 60,5 g de ácido 4-bromobutírico. A mistura reacional foi fervida sob um condensador de refluxo durante cerca de cinco horas. Durante este tempo, o brometo de sódio separou-se. O álcool foi destilado num banho de vapor e a lactona foi separada do brometo de sódio por extração com éter. Evaporou-se o éter e destilou-se a lactona sob pressão normal. O rendimento foi de 21,2 g (67%) de produto em ebulição a 202-206 °C. Uma alternativa pode ser a cloração radicalar livre do ácido butírico com cloreto de enxofre na presença de peróxidos, separar os isómeros por destilação, produzir o sal de sódio do ácido 4-clorobutírico e ciclizar a lactona como no caso do derivado 4-bromo acima referido. A gama-butirolactona também pode ser obtida a partir do ácido 4-metoxibutírico, da 3-fenoxipropilcianida, do ácido gama-dietilaminobutírico e do éter beta-cloroetilvinílico, bem como de muitos outros produtos químicos demasiado exóticos. Industrialmente, é normalmente produzido pela reação do acetileno com formaldeído a altas temperaturas e pressões.
Desidrogenação do 1,4-butanodiol (BDO) em gama-butirolactona (GBL).
Uma mistura de 90,1 g (1 mole) de 1,4-butanodiol, 4 g de catalisador de cromite de cobre e 0,15 g de hidróxido de sódio em pó de grau de reagente (ou melhor KOH) foi agitada vigorosamente e aquecida sob refluxo. A cerca de 200 °C, ocorreu uma evolução viva do hidrogénio, a temperatura desceu cerca de 10 °C e a desidrogenação prosseguiu sem problemas. A evolução do gás (39 L/2 mol por mole de 1,4-butanodiol reagido) cessou em cerca de 3 h. A mistura reacional foi arrefecida à temperatura ambiente, filtrada do catalisador e destilada sob pressão reduzida para dar gama-butirolactona em cerca de 80% de rendimento e 1,4-butanodiol não reagido em cerca de 10% de rendimento.
Preparação do catalisador de desidrogenação de cromite cúprica de elevada atividade.
Adicionou-se, sob agitação, uma solução de 260 g de nitrato de cobre (II) tri-hidratado em 900 ml de água da torneira a 80 °C a uma solução de 178 g de dicromato de sódio di-hidratado e 225 ml de NH4OH a 28%, completada até 900 ml a 25 °C. O precipitado foi recolhido por filtração por sucção e lavado com água três vezes. O cromato de cobre e amónio foi seco a 75-80 °C durante a noite. Este foi pulverizado e adicionado em pequenas porções a um balão de 1 litro de 3 gargalos equipado com um agitador de aço inoxidável do tipo Hershberg que raspava junto ao fundo do balão. O balão foi parcialmente imerso num banho de óleo a 350 °C (com 300-320 °C, podem obter-se bons resultados). O tempo de adição foi de 15 minutos (libertaram-se muitos fumos) e a mistura foi agitada a 350 °C durante mais 15 minutos, depois de tudo estar concluído. O pó arrefecido e preto empoeirado foi utilizado tal e qual para a desidrogenação.
Adicionou-se, sob agitação, uma solução de 260 g de nitrato de cobre (II) tri-hidratado em 900 ml de água da torneira a 80 °C a uma solução de 178 g de dicromato de sódio di-hidratado e 225 ml de NH4OH a 28%, completada até 900 ml a 25 °C. O precipitado foi recolhido por filtração por sucção e lavado com água três vezes. O cromato de cobre e amónio foi seco a 75-80 °C durante a noite. Este foi pulverizado e adicionado em pequenas porções a um balão de 1 litro de 3 gargalos equipado com um agitador de aço inoxidável do tipo Hershberg que raspava junto ao fundo do balão. O balão foi parcialmente imerso num banho de óleo a 350 °C (com 300-320 °C, podem obter-se bons resultados). O tempo de adição foi de 15 minutos (libertaram-se muitos fumos) e a mistura foi agitada a 350 °C durante mais 15 minutos, depois de tudo estar concluído. O pó arrefecido e preto empoeirado foi utilizado tal e qual para a desidrogenação.
Síntese de gama-butirolactona a partir de tetra-hidrofurano (THF)
A uma mistura agitada de 7,2 g (0,1 mol) de tetra-hidrofurano em 100 ml de água foram adicionados 15,1 g de bromato de sódio e 13,6 g (0,1 mol) de hidrogenossulfato de potássio. Foi necessário um arrefecimento externo para manter a temperatura da solução entre 25-30 °C. A agitação foi mantida durante 16 horas à temperatura ambiente, após o que todo o THF foi consumido. Para extinguir o excesso de bromo formado, utilizou-se uma solução ácida de sulfito de sódio [o bissulfito deve funcionar igualmente bem]. Assim, foram adicionados 140-150 ml de uma solução a 10% e 13,6 g (0,1 mol) de hidrogenossulfato de potássio. A reação foi arrefecida e extraída com 5x30 ml de diclorometano. As camadas orgânicas combinadas foram secas sobre MgSO4 e o solvente foi removido sob vácuo. O resíduo foi destilado para dar gama-butirolactona em 73% de rendimento (bp 204-205 °C).
Reação de Sandmeyer de GABA a GBL/GHB.
É espetacular para um químico que pretenda preparar GHB em pequenas quantidades e com rendimentos elevados e fazê-lo sem obter diretamente quaisquer produtos químicos regulamentados, como a gama-butirolactona (GBL) ou o 1,4-butanodiol (BDO). Também evita os rendimentos tipicamente baixos observados na oxidação do tetrahidrofurano (THF). Utiliza um aminoácido fácil de obter, o ácido gama-aminobutírico (GABA), e nitrito de sódio (NaNO2). A escala é muito boa e funciona sem grandes problemas. Não é utilizado nenhum produto químico suspeito.
A reação de Sandmeyer utiliza ácido nitroso para transformar aminas em sais de diazónio. Esta reação, tal como se aplica à transformação do GABA em GHB, é apresentada na primeira reação abaixo. Os sais de diazónio alifáticos sofrem rapidamente hidrólise na presença de água, libertando azoto gasoso e deixando um grupo hidroxilo. Este fenómeno é ilustrado na segunda fase. Como resultado destas reacções, o GABA pode ser transformado em GHB numa reação de um só frasco, fácil de realizar.
Executar a reação.
Preparar um balão de 2 L, colocado em água gelada em cima de um agitador magnético. Agora.
Executar a reação.
Preparar um balão de 2 L, colocado em água gelada em cima de um agitador magnético. Agora.
- Adicione 3mol de GABA (309,4 g).
- Adicione3mol de NaNO2 (207,0 g).
- Adicionar700 ml de água (o volume total passa a ser cerca de 1100 ml).
- Colocar uma barra de agitação de 1" e começar a agitar.
- Carregarum funil de adição de 500 ml com pressão igualada com 3,3 mol de HCl(aq) (385,0 g 31,25%, 334,8 ml 31,25%).
- Instalar o funil de adição com um adaptador de saída de gás e ventilar para o exterior.
Começar a deitar lentamente o ácido clorídrico na mistura. Goteje-o a um ritmo constante de cerca de 1 gota a cada 2-5 segundos. Acelere o processo à medida que o tempo passa e substitua o gelo conforme necessário, mas não permita que a evolução do gás venenoso castanho se torne vigorosa. Cerca de uma hora depois de ter sido adicionada a última gota de ácido, não é necessário substituir o gelo. Uma vez terminada a reação, proceder à extração. (normalmente 24-36 horas depois)
Extração.
Há muitas opções para isto. Este ainda é um trabalho em curso, mas depois de cerca de 20 execuções, cheguei a usar este trabalho. Pode utilizar acetato de etilo (EtOAc), clorofórmio ou cloreto de metileno (diclorometano, também conhecido por DCM) para efetuar as extracções com solventes. Normalmente utilizo o DCM porque é mais agradável, uma vez que a camada orgânica desce para o fundo do funil de separação.
1. Preparação para uma destilação simples
Extração.
Há muitas opções para isto. Este ainda é um trabalho em curso, mas depois de cerca de 20 execuções, cheguei a usar este trabalho. Pode utilizar acetato de etilo (EtOAc), clorofórmio ou cloreto de metileno (diclorometano, também conhecido por DCM) para efetuar as extracções com solventes. Normalmente utilizo o DCM porque é mais agradável, uma vez que a camada orgânica desce para o fundo do funil de separação.
1. Preparação para uma destilação simples
a) Destilar, deitando fora os primeiros 5-10 ml de destilado, uma vez que este contém uma quantidade razoável de óxidos nítricos. Destilar o máximo de água possível, basicamente até o cloreto de sódio começar a saturar a camada aquosa e precipitar.
b) O restante do destilado (cerca de 700 ml) conterá aproximadamente 1 g de GBL/10 ml.
c) Tratar o resto do destilado com NaHCO3 em refluxo durante 30 minutos.
d) Ferver com cerca de 5% do volume de carvão ativado (ou seja, 0,35 ml de carvão ativado) (em comparação com o volume da solução) durante 5-10 minutos.
e) Deixar arrefecer e filtrar, lavar o carvão com água destilada. Guardar o NaGHB.
2. Com o restante do aquoso, extrair 5 vezes com porções de 625 ml de DCM.
3. Destilar o DCM (reutilizar o DCM!).
4. Destilar a GBL (sob vácuo, se disponível).
5. Reagir com NaHCO3 e água destilada e tratar com carvão ativado como anteriormente.
Normalmente, são produzidos 375 g de NaGHB a partir da GBL extraída com solvente, dos quais 100 g de NaGHB a partir do destilado aquoso. Embora a conversão seja quase quantitativa (medida por GC/MS), o rendimento global recuperado é normalmente de cerca de 70%.
3. Destilar o DCM (reutilizar o DCM!).
4. Destilar a GBL (sob vácuo, se disponível).
5. Reagir com NaHCO3 e água destilada e tratar com carvão ativado como anteriormente.
Normalmente, são produzidos 375 g de NaGHB a partir da GBL extraída com solvente, dos quais 100 g de NaGHB a partir do destilado aquoso. Embora a conversão seja quase quantitativa (medida por GC/MS), o rendimento global recuperado é normalmente de cerca de 70%.
Last edited:
