@G.Patton Я считаю, что один из нарисованных промежуточных продуктов в этом синтезе (и в оригинальной статье о родии) неверен.
(3), изображение промежуточного продукта амфетамин-формальдегид-имин имеет ту же структуру, что и фенилацетон-метиламин-имин, который можно увидеть в другом месте
Это не кажется мне правильным по двум причинам: во-первых, стандартный механизм образования иминов на субстрате дает имин, в котором двойная связь находится между N и предполагаемой метильной группой на метамфетамине, а НЕ между N и альфа-углеродом, как в приведенной структуре. И подумайте об этом: двойная связь образуется, когда одинокая пара амина отщепляет воду, образованную на кислороде формальдегида в качестве уходящей группы, что должно быть сделано на стороне формальдегида (предполагаемой метильной группы)
Во-вторых, синтез, как сообщается, стереоспецифичен в зависимости от исходного субстрата. То есть, восстановление d-амф даст d-мет и то же самое для l-изомера. Структура, как показано (3), не имеет хиральных центров, и ее восстановление эквивалентно стандартному восстановительному аминированию фенилацетона, которое дает рацемический продукт. Предложенная мной структура промежуточного продукта имеет хиральный центр, который будет таким же, как у исходного материала, и поэтому соответствует наблюдаемой стереоспецифичности реакции.
Если я прав, это прояснит вопросы относительно стереоспецифичности реакции, заданные ранее в этой теме. Если я где-то ошибся, прошу прощения, но мне было интересно, почему восстановление нехирального (3) приводит к нерацемической смеси продуктов, когда используется нерацемический исходный материал амфетамин.
(3), изображение промежуточного продукта амфетамин-формальдегид-имин имеет ту же структуру, что и фенилацетон-метиламин-имин, который можно увидеть в другом месте
Это не кажется мне правильным по двум причинам: во-первых, стандартный механизм образования иминов на субстрате дает имин, в котором двойная связь находится между N и предполагаемой метильной группой на метамфетамине, а НЕ между N и альфа-углеродом, как в приведенной структуре. И подумайте об этом: двойная связь образуется, когда одинокая пара амина отщепляет воду, образованную на кислороде формальдегида в качестве уходящей группы, что должно быть сделано на стороне формальдегида (предполагаемой метильной группы)
Во-вторых, синтез, как сообщается, стереоспецифичен в зависимости от исходного субстрата. То есть, восстановление d-амф даст d-мет и то же самое для l-изомера. Структура, как показано (3), не имеет хиральных центров, и ее восстановление эквивалентно стандартному восстановительному аминированию фенилацетона, которое дает рацемический продукт. Предложенная мной структура промежуточного продукта имеет хиральный центр, который будет таким же, как у исходного материала, и поэтому соответствует наблюдаемой стереоспецифичности реакции.
Если я прав, это прояснит вопросы относительно стереоспецифичности реакции, заданные ранее в этой теме. Если я где-то ошибся, прошу прощения, но мне было интересно, почему восстановление нехирального (3) приводит к нерацемической смеси продуктов, когда используется нерацемический исходный материал амфетамин.
Здравствуйте. Во-первых, a-углерод имеет большую электронную плотность, чем метиловый углерод. Типичный механизм, приводящий к такому промежуточному соединению (скрыт под водяным знаком Breaking Bad, извините):
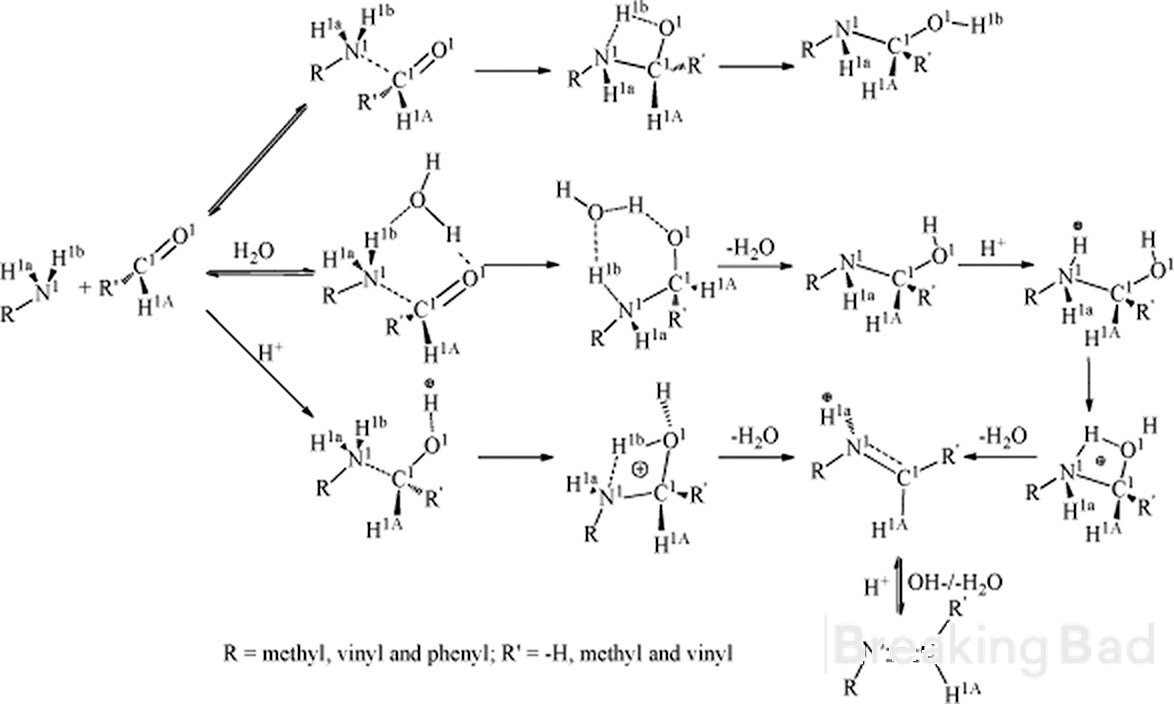
Во-вторых, есть ли у вас достоверные данные о стереоспецифичности результата этого синтеза?
Во-вторых, есть ли у вас достоверные данные о стереоспецифичности результата этого синтеза?
