G.Patton
Expert
- Joined
- Jul 5, 2021
- Messages
- 2,659
- Solutions
- 3
- Reaction score
- 2,734
- Points
- 113
- Deals
- 1
Úvod: V knize je popsán vývoj chemických látek, které jsou součástí chemického průmyslu.
Tento soubor se zabývá syntézou GHB a příbuzných sloučenin. Je velmi nebezpečné pokoušet se o syntézu GHB bez náležitých znalostí praktické organické chemie. Daleko nejjednodušší způsob výroby GHB je hydrolýza příslušného laktonu (cyklického intramolekulárního esteru) na požadovanou hydroxykyselinu. Hydrolýzu esterů lze provést dvěma způsoby: Reakce katalyzovaná kyselinou nebo reakce katalyzovaná zásadou. Reakce katalyzovaná bází je zde naší volbou, protože reakce není reverzibilní jako reakce katalyzovaná kyselinou, a proto získáme vyšší výtěžky a získáme sodnou sůl GHB, protože volná kyselina není stabilní a okamžitě se opět cyklizuje na gama-butyrolakton.
Transformace gama-butyrolaktonu na gama-hydroxy butyrát sodný (Na-GHB).
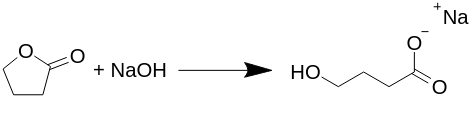
Reakce probíhá ekvimolárně (reaguje stejný počet každé molekuly) a při této reakci nevznikají žádné vedlejší produkty, jako je plynný vodík, voda nebo cokoli jiného, jak se navrhuje v několika jiných textech. Všechny publikované přípravky GHB, nebo správněji Na-GHB, refluxují butyrolakton s hydroxidem sodným v různých rozpouštědlech, obvykle ve vodném alkoholu, ale to není nutné.
Fyzikální/chemické vlastnosti.
gama-butyrolakton.
Mol hm. 86,09; mp -43,53 °C; bp 204 °C; d 1,12 g/ml
Číslo CAS: [96-48-0]
Mísitelný s vodou, rozpustný v methanolu, ethanolu, acetonu, etheru, benzenu
LD50: 1720 mg/kg (perorálně, myš) 1540 mg/kg (perorálně, potkan)
Použití: Rozpouštědlo, odstraňovač nátěrů, elektrolyt kondenzátorů, v organické chemii
Synonyma: GBL, BLO, butyrolakton, lakton kyseliny gama-hydroxy máselné, 1,2-butanolid, 1,4-butanolid, 4-butanolid, 2-oxanolon, tetrahydro-2-furanon, dihydro-2(3H)-furanon.
Sodná sůl GHB.
Mol hm. 126,09; mp 145-146 °C
Číslo CAS: [502-85-2]
LD50:2700 mg/kg (perorálně, potkan)
Synonyma: Gama-OH, oxybát sodný, gama-oxybutyrát sodný, Somatomax PM, Wy-3478, NSC-84223, Somsanit, Anetamine.
GHB draselný.
Mol hm.: 142,20
GHB vápenatý.
Mol hm. 246,16; mp 164-166 °C, 166-168 °C.
Hořečnatý GHB.
Mol hm. 230,39; mp (bezvodý) 172-174 °C; tetrahydrát 118-120 °C; pentahydrát 76-78 °C.
Mol hm. 86,09; mp -43,53 °C; bp 204 °C; d 1,12 g/ml
Číslo CAS: [96-48-0]
Mísitelný s vodou, rozpustný v methanolu, ethanolu, acetonu, etheru, benzenu
LD50: 1720 mg/kg (perorálně, myš) 1540 mg/kg (perorálně, potkan)
Použití: Rozpouštědlo, odstraňovač nátěrů, elektrolyt kondenzátorů, v organické chemii
Synonyma: GBL, BLO, butyrolakton, lakton kyseliny gama-hydroxy máselné, 1,2-butanolid, 1,4-butanolid, 4-butanolid, 2-oxanolon, tetrahydro-2-furanon, dihydro-2(3H)-furanon.
Sodná sůl GHB.
Mol hm. 126,09; mp 145-146 °C
Číslo CAS: [502-85-2]
LD50:2700 mg/kg (perorálně, potkan)
Synonyma: Gama-OH, oxybát sodný, gama-oxybutyrát sodný, Somatomax PM, Wy-3478, NSC-84223, Somsanit, Anetamine.
GHB draselný.
Mol hm.: 142,20
GHB vápenatý.
Mol hm. 246,16; mp 164-166 °C, 166-168 °C.
Hořečnatý GHB.
Mol hm. 230,39; mp (bezvodý) 172-174 °C; tetrahydrát 118-120 °C; pentahydrát 76-78 °C.
Laboratorní postupy syntézy solí GHB.
Dodržujte běžné laboratorní bezpečnostní postupy. Používejte laboratorní plášť a ochranné brýle. Budete pracovat s horkými žíravými roztoky a rozpouštědly! Uvědomte si rizika spojená s výrobou GHB! Nikdy nepracujte sami!
Sodná sůl GHB.
Postup:
Rozpusťte 130 g (3,25 molu) čistého hydroxidu sodného ve 400 ml destilované vody v 1000 ml baňce s kulatým dnem a míchejte. Rozpouštění je exotermické a roztok se zahřívá. K regulaci teploty lze použít studenou vodní lázeň. Když se vše rozpustí za vzniku čirého roztoku, pomalu přidejte 250 ml (280 g, 3,25 molu) gama-butyrolaktonu v 50 ml dávkách za dobrého míchání. Doporučuje se použít kapací nálevku. Přidávání gama-butyrolaktonu k roztoku hydroxidu sodného je rovněž exotermické, a pokud se přidává příliš rychle, roztok se začne vařit, a to nechceme. Sledujte teplotu ponořeným teploměrem. Přidávání gama-butyrolaktonu bude trvat přibližně 20-30 minut. Když je vše přidáno, nechte směs za občasného míchání reagovat dalších 10 minut.
Nyní je čas zjistit, zda reakce proběhla do konce, a to kontrolou pH pomocí univerzálního pH papírku. Naším cílem je pH 7-8. Pokud je příliš vysoké (pH > 8), přidáme 10 ml gama-butyrolaktonu a necháme reagovat ještě několik minut. Pokud je pH příliš nízké (pH < 7), přidáme několik ml koncentrovaného vodného roztoku NaOH. Takto pokračujte, dokud nebude pH v požadovaných mezích.
Roztok je dokonale čirý a chutná mírně slaně. Může být mírně žlutě zbarvený, ale ne moc, pokud byl použit dostatečně čistý butyrolakton (o tento problém se postará destilace laktonu před použitím, b.p. 204 °C). Pokud se k neutralizaci příliš zásaditého roztoku použije kyselina (namísto přidání většího množství laktonu), mohou se v roztoku vysrážet krystalky sodné soli kyseliny a chuť se výrazně zhorší. Konečný roztok bude mít asi 750 ml, 50 % NaGHB. Roztok lze koncentrovat (vyvařením přebytečné vody) na ~600 ml, aniž by při pokojové teplotě krystalizoval, ale pokud se koncentruje až na ~500 ml, vždy ztuhne.
Nyní je čas zjistit, zda reakce proběhla do konce, a to kontrolou pH pomocí univerzálního pH papírku. Naším cílem je pH 7-8. Pokud je příliš vysoké (pH > 8), přidáme 10 ml gama-butyrolaktonu a necháme reagovat ještě několik minut. Pokud je pH příliš nízké (pH < 7), přidáme několik ml koncentrovaného vodného roztoku NaOH. Takto pokračujte, dokud nebude pH v požadovaných mezích.
Roztok je dokonale čirý a chutná mírně slaně. Může být mírně žlutě zbarvený, ale ne moc, pokud byl použit dostatečně čistý butyrolakton (o tento problém se postará destilace laktonu před použitím, b.p. 204 °C). Pokud se k neutralizaci příliš zásaditého roztoku použije kyselina (namísto přidání většího množství laktonu), mohou se v roztoku vysrážet krystalky sodné soli kyseliny a chuť se výrazně zhorší. Konečný roztok bude mít asi 750 ml, 50 % NaGHB. Roztok lze koncentrovat (vyvařením přebytečné vody) na ~600 ml, aniž by při pokojové teplotě krystalizoval, ale pokud se koncentruje až na ~500 ml, vždy ztuhne.
Příprava GHB pomocí hydrogenuhličitanu sodného (jedlé sody, NaHCO3).
Přidejte 273 g NaHCO3 (3,25 molu) do 1125 ml destilované vody v trojhrdlé baňce s kulatým dnem. Roztok pomalu přiveďte k varu za stálého míchání skleněnou nebo podobnou tyčinkou. Všechna jedlá soda se rozpustí. Při varu roztoku bude patrný oxid uhličitý, který bude z roztoku odcházet. To je rozklad hydrogenuhličitanu sodného na mírně silnou zásadu, uhličitan sodný.
Snižte teplotu na mírný var a pomalu přidejte 250 ml gama- butyrolaktonu (280 g, 3,25 molu). Přídavek není okamžitě exotermický, jako v případě syntézy hydroxidu sodného. Tento roztok udržujte při mírném varu po dobu 30 minut. Zkontrolujte pH pomocí univerzálního pH papíru. Naším cílem je pH kolem 7, ale 6 až 8 je naprosto bezpečné. Pokud je pH příliš vysoké, přidejte ještě malé množství GBL a pokračujte v refluxu.
Roztok bude dokonale čirý a měl by být absolutně bezbarvý. Pokud není dokonale bezbarvý, tj. pokud byl použit mírně nečistý butyrolakton a roztok získal světle žlutou barvu, přidejte asi 100 ml aktivního uhlí. Tento roztok nechte 10 minut vařit. Roztok ochlaďte a poté přefiltrujte, přičemž aktivní uhlí dvakrát nebo třikrát promyjte 50 ml studené vody. Při této syntéze vznikne 410 g NaGHB. Tento roztok může být zahuštěn asi na 50 % NaGHB, než začne krystalizovat. Pokud si přejete prášek, zahřívejte, dokud teplota roztoku nedosáhne 150 °C, pak jej nalijte na vychladlou pyrexovou misku a nechte vychladnout a ztuhnout. Tato syntéza je ideální pro použití tam, kde není k dispozici hydroxid sodný ACS, potravinářský nebo pro elektroniku.
Roztok bude dokonale čirý a měl by být absolutně bezbarvý. Pokud není dokonale bezbarvý, tj. pokud byl použit mírně nečistý butyrolakton a roztok získal světle žlutou barvu, přidejte asi 100 ml aktivního uhlí. Tento roztok nechte 10 minut vařit. Roztok ochlaďte a poté přefiltrujte, přičemž aktivní uhlí dvakrát nebo třikrát promyjte 50 ml studené vody. Při této syntéze vznikne 410 g NaGHB. Tento roztok může být zahuštěn asi na 50 % NaGHB, než začne krystalizovat. Pokud si přejete prášek, zahřívejte, dokud teplota roztoku nedosáhne 150 °C, pak jej nalijte na vychladlou pyrexovou misku a nechte vychladnout a ztuhnout. Tato syntéza je ideální pro použití tam, kde není k dispozici hydroxid sodný ACS, potravinářský nebo pro elektroniku.
GHB draselný.
Použijte ethanolovou syntézu popsanou výše pro sodný GHB, ale nahraďte 130 g NaOH 182 g KOH (tento výpočet je založen na těžším atomu K a vyšším obsahu vody v KOH oproti NaOH). Použitím KOH získají uživatelé K-GHB onen doplněk draslíku, který je podle některých názorů v souvislosti s podáváním GHB potřebný. Mějte na paměti, že (práškový) K-GHB je o něco méně účinný (hmotnostně) než Na-GHB, protože iont K je těžší než protějšek Na. Rozdíly mezi K-GHB a Na-GHB spočívají v tom, že sůl K je lépe rozpustná ve vodě než sůl Na a chuť je spíše podobná soli/kořici namísto chuti soli/mýdla u Na-GHB.
Vápník GHB.
74 g analyticky čistého hydroxidu vápenatého se suspenduje ve 200 ml destilované vody. K této suspenzi se při pokojové teplotě po částech (každá část asi 5 až 10 ml) a za míchání přidá 160 ml 4-butyrolaktonu. Po přidání 20 ml se reakční směs zahřeje na teplotu asi 50 °C až 60 °C. Přídavek 4-butyrolaktonu se řídí tak, aby teplota zůstala mezi 50 °C a 60 °C, což trvá asi 1 hodinu. Během této doby se hydroxid vápenatý prakticky zcela rozpustí. Reakční materiál je znečištěn mírnou rezavě žlutou sraženinou. Zředí se 300 ml methanolu, nechá se čtyři hodiny odležet a poté se přefiltruje přes skládaný filtr. Čirý filtrát se opatrně zpracuje s 200 ml acetonu tak, že po každé dávce acetonu, která způsobí sraženinu, se nechá čas, aby se sraženina znovu rozpustila. Získá se čirý vodný roztok, který se dá krystalizovat. Po dvou hodinách stání se začnou usazovat bezbarvé krystaly. V tomto stavu se krystalizace urychluje průběžným přidáváním acetonu (celkem 100 ml). Doba krystalizace je 24 hodin. Krystaly se odsají a promyjí se nejprve 50 ml methanolu a poté navíc 60 ml acetonu. Krystaly se suší při teplotách od 60 °C do 80 °C v sušárně. Výtěžek: 230 g. Bod tání 166-168 °C. (ihned). Produkt je bezvodá nehygroskopická vápenatá sůl kyseliny 4-hydroxymáselné. Je rozpustný podle potřeby ve vodě, vodný roztok má hodnotu pH 7 až 7,5. Sůl lze skladovat libovolně dlouho a na vzduchu se nemění. Ani při skladování nepřitahuje vodu ze vzduchu.
Zbytek krystalizuje na hmotu bezbarvých krystalů, která se po vysušení při teplotách asi 60 °C až 80 °C. Výtěžek: asi 105 g. Teplota tání 164-166 °C. Produkt je di-(4-hydroxymáselný) vápník. Rekrystalizuje se rozpuštěním v malém množství methanolu, následným přidáním acetonu do zákalu a krystalizací za studena.
Místo methanolu lze k rekrystalizaci se stejným úspěchem použít také ethanol a isopropanol. Bez použití alkoholů obsahujících vodu jako rekrystalizačního média nebo jako přísady rekrystalizace a čištění se nezískají stabilní a zejména nehygroskopické vápenaté soli. Obsah vody v alkoholech by měl být přibližně 3-10 % objemových. Takto získaný konečný produkt se snadno rozpouští ve vodě, není hydroskopický a má příjemnou aromatickou vůni.
Zbytek krystalizuje na hmotu bezbarvých krystalů, která se po vysušení při teplotách asi 60 °C až 80 °C. Výtěžek: asi 105 g. Teplota tání 164-166 °C. Produkt je di-(4-hydroxymáselný) vápník. Rekrystalizuje se rozpuštěním v malém množství methanolu, následným přidáním acetonu do zákalu a krystalizací za studena.
Místo methanolu lze k rekrystalizaci se stejným úspěchem použít také ethanol a isopropanol. Bez použití alkoholů obsahujících vodu jako rekrystalizačního média nebo jako přísady rekrystalizace a čištění se nezískají stabilní a zejména nehygroskopické vápenaté soli. Obsah vody v alkoholech by měl být přibližně 3-10 % objemových. Takto získaný konečný produkt se snadno rozpouští ve vodě, není hydroskopický a má příjemnou aromatickou vůni.
Hořečnatý GHB .
60 g hydroxidu hořečnatého (analytické kvality) se za míchání suspenduje ve 200 ml vody z vodovodu. Proudem a za míchání se do této suspenze přimíchá 160 ml butyrolaktonu. Poté se směs za míchání zahřívá 6 hodin na vodní lázni ve dvoulitrové baňce. Hydroxid hořečnatý se prakticky úplně rozpustí. Baňka se nechá stát přes noc, přičemž se usazují kontaminanty, a roztok se bez námahy odvádí z usazených kontaminantů. Dekantát čirý jako voda se zpočátku míchá se 100 ml acetonu po dobu 10 minut. Bezbarvá sirupovitá kapalina, která se nyní stala viskóznější, se opět smíchá se 100 ml acetonu, jak je popsáno výše, aceton se opět odstraní dekantací a poměrně viskózní bezbarvý sirup se nechá sám od sebe při pokojové teplotě asi 2 až 4 hodiny. Ztuhne na bezbarvou krystalickou hmotu, která se rozdrtí v hmoždíři a několik hodin se suší na vzduchu. Bod tání 76 °C až 78 °C. Výtěžek: 314 g v analyticky čisté formě.
Tato hořečnatá sůl obsahuje asi 5 molů hydratační vody. Není hydroskopická, je stabilní a lze ji skladovat libovolně dlouhou dobu. Několikahodinovým sušením při teplotě 40 °C až 50 °C ztrácí část své krystalizační vody (1 mol) a poté taje při 118 °C až 120 °C. Bezvodý 4-hydroxybutyrát hořečnatý lze vyrobit odstraněním vody sublimací a/nebo odpařením vody za sníženého parciálního tlaku vody a při zvýšené teplotě nebo krystalizací z roztoku obsahujícího organické rozpouštědlo. Sůl bez vody taje při 172-174 °C. Chemická analýza ukazuje 10,50 % hmotnostních hořčíku (vypočteno 10,55 % hmotnostních hořčíku). Všechny modifikace jsou nehygroskopické a stabilní během skladování. 1 g hořečnaté soli se rozpouští ve 2 ml vody při pokojové teplotě, pH vodného roztoku je 7. Snadno se rozpouští ve vodě, methanolu a ethanolu, nerozpouští se v éteru a uhlovodících, není hygroskopická, je skladovatelná a má příjemnou aromatickou vůni.
Tato hořečnatá sůl obsahuje asi 5 molů hydratační vody. Není hydroskopická, je stabilní a lze ji skladovat libovolně dlouhou dobu. Několikahodinovým sušením při teplotě 40 °C až 50 °C ztrácí část své krystalizační vody (1 mol) a poté taje při 118 °C až 120 °C. Bezvodý 4-hydroxybutyrát hořečnatý lze vyrobit odstraněním vody sublimací a/nebo odpařením vody za sníženého parciálního tlaku vody a při zvýšené teplotě nebo krystalizací z roztoku obsahujícího organické rozpouštědlo. Sůl bez vody taje při 172-174 °C. Chemická analýza ukazuje 10,50 % hmotnostních hořčíku (vypočteno 10,55 % hmotnostních hořčíku). Všechny modifikace jsou nehygroskopické a stabilní během skladování. 1 g hořečnaté soli se rozpouští ve 2 ml vody při pokojové teplotě, pH vodného roztoku je 7. Snadno se rozpouští ve vodě, methanolu a ethanolu, nerozpouští se v éteru a uhlovodících, není hygroskopická, je skladovatelná a má příjemnou aromatickou vůni.
Další soli.
Lithiové a amonné soli GHB by byly nebezpečné při požití. Lithium-iont je toxický a spolu s laktonem NH3 se stává pyrrolidonem.
Otázky a odpovědi k syntéze.
Otázka: Mohu místo čistého hydroxidu sodného použít louh?
Odpověď: Ne, mohlo by to mít nepředvídatelné následky na vaše zdraví. Louh z obchodu s elektronikou nemá ani zdaleka tak přísná kritéria čistoty jako například louh potravinářský, ACS nebo louh pro elektroniku. Někteří lidé vyprávějí o úspěšných příbězích s použitím louhu, což je skutečně možné, ale jak bylo řečeno, výsledky jsou nepředvídatelné.
Otázka: Nemám skleněné nádobí, o kterém říkáte, že je potřeba, mohu místo toho roztok vařit v hrnci na sporáku?
Odpověď: Ne, nemůžete. Hydroxid sodný způsobí korozi kovu a do výrobku se dostanou různé kovové ionty. Můžete samozřejmě použít jednodušší skleněné nádobí než v mých návrzích a provést nezbytné úpravy postupu.
Otázka: Nemohu rekrystalizovat Na-GHB z ethanolu. Tvoří lepkavou kaši.
Odpověď: Váš Na-GHB není suchý nebo váš ethanol není bezvodý. Voda rekrystalizaci téměř znemožňuje. Skutečnost, že sodná sůl GHB je rozpuštěná (hygroskopická), to nijak nezlepšuje. Před pokusem o rekrystalizaci nebo jinou improvizovanou alternativou musíte GHB důkladně vysušit, nejlépe ve vakuovém exsikátoru. Ethanol, který hodláte použít (nejčastěji se dodává v čistotě 95 %, zbytek tvoří voda), musí být vysušen sušením nad bezvodým síranem vápenatým a následnou destilací z oxidu vápenatého s patřičnými opatřeními k vyloučení vlhkosti z reakce.
Otázka: Kde mohu koupit butyrolakton/je bezpečné koupit butyrolakton?
Odpověď: Netuším, jaká je situace u vás v zemi. Odpovědi na tyto otázky velmi závisí na tom, kdo jste a kde žijete. Můžete se však obrátit na některého z mnoha prodejců sad GHB, které lze nalézt na internetu.
Odpověď: Ne, mohlo by to mít nepředvídatelné následky na vaše zdraví. Louh z obchodu s elektronikou nemá ani zdaleka tak přísná kritéria čistoty jako například louh potravinářský, ACS nebo louh pro elektroniku. Někteří lidé vyprávějí o úspěšných příbězích s použitím louhu, což je skutečně možné, ale jak bylo řečeno, výsledky jsou nepředvídatelné.
Otázka: Nemám skleněné nádobí, o kterém říkáte, že je potřeba, mohu místo toho roztok vařit v hrnci na sporáku?
Odpověď: Ne, nemůžete. Hydroxid sodný způsobí korozi kovu a do výrobku se dostanou různé kovové ionty. Můžete samozřejmě použít jednodušší skleněné nádobí než v mých návrzích a provést nezbytné úpravy postupu.
Otázka: Nemohu rekrystalizovat Na-GHB z ethanolu. Tvoří lepkavou kaši.
Odpověď: Váš Na-GHB není suchý nebo váš ethanol není bezvodý. Voda rekrystalizaci téměř znemožňuje. Skutečnost, že sodná sůl GHB je rozpuštěná (hygroskopická), to nijak nezlepšuje. Před pokusem o rekrystalizaci nebo jinou improvizovanou alternativou musíte GHB důkladně vysušit, nejlépe ve vakuovém exsikátoru. Ethanol, který hodláte použít (nejčastěji se dodává v čistotě 95 %, zbytek tvoří voda), musí být vysušen sušením nad bezvodým síranem vápenatým a následnou destilací z oxidu vápenatého s patřičnými opatřeními k vyloučení vlhkosti z reakce.
Otázka: Kde mohu koupit butyrolakton/je bezpečné koupit butyrolakton?
Odpověď: Netuším, jaká je situace u vás v zemi. Odpovědi na tyto otázky velmi závisí na tom, kdo jste a kde žijete. Můžete se však obrátit na některého z mnoha prodejců sad GHB, které lze nalézt na internetu.
Prekurzory: V případě, že se jedná o GHB, můžete se obrátit na výrobce GHB.
Zřejmým prekurzorem pro syntézu GHB je gama-butyrolakton. Lze jej vyrobit z prekurzorů, jako je tetrahydrofuran (THF) s oxidanty, jako je tetroxid ruthenia, chlornan vápenatýa kyselina dusičná. Lze také použít deriváty kyseliny 4-halo-máselné (chloro, bromo, jodo). Stejně jako v níže uvedené syntéze je lze převést na gama-butyrolakton destilací s methoxidem sodným.
gama-butyrolakton z kyseliny 4-brommáselné.
K roztoku 7,8 g sodíku v 500 ml absolutního alkoholu bylo přidáno 60,5 g kyseliny 4-brommáselné. Reakční směs byla vařena pod zpětným chladičem po dobu asi pěti hodin. Během této doby se oddělil bromid sodný. Alkohol byl vydestilován z parní lázně a lakton byl oddělen od bromidu sodného extrakcí etherem. Éter se odpařil a lakton se destiloval za běžného tlaku. Výtěžek byl 21,2 g (67 %) produktu s teplotou varu 202-206 °C. Alternativou může být volná radikálová chlorace kyseliny máselné chloridem sírovým v přítomnosti peroxidů a oddělení isomerů destilací, vytvoření sodné soli kyseliny 4-chlormáselné a cyklizace na lakton jako u výše uvedeného 4-bromderivátu. gama- butyrolakton lze také vyrobit z kyseliny 4-methoxymáselné, 3-fenoxypropylkyanidu, kyseliny gama-diethylaminomáselné a beta-chlorethylvinyletheru, jakož i z mnoha dalších trochu příliš exotických chemikálií. Průmyslově se běžně vyrábí reakcí acetylenu s formaldehydem za vysokých teplot a tlaků.
Dehydrogenace 1,4-butandiolu (BDO) na gama-butyrolakton (GBL).
Směs 90,1 g (1 mol) 1,4-butandiolu, 4 g měďnatého chromitového katalyzátoru a 0,15 g práškového reagenčního hydroxidu sodného (nebo lépe KOH) byla intenzivně míchána a zahřívána pod refluxem. Při teplotě asi 200 °C došlo k živému vývinu vodíku, teplota klesla asi o 10 °C a dehydrogenace probíhala hladce. Vývoj plynu (39 l/2 mol na mol zreagovaného 1,4-butandiolu) ustal asi za 3 h. Reakční směs byla ochlazena na pokojovou teplotu, odfiltrována od katalyzátoru a destilována za sníženého tlaku za vzniku gama-butyrolaktonu ve výtěžku asi 80 % a nezreagovaného 1,4-butandiolu ve výtěžku asi 10 %.
Příprava vysoce aktivního katalyzátoru dehydrogenace chromitanem měďnatým.
Roztok 260 g trihydrátu dusičnanu měďnatého(II)v 900 ml vody z vodovodu při 80 °C byl za stálého míchání přidán k roztoku 178 g dihydrátu dichromanu sodného a 225 ml 28% NH4OH doplněného na 900 ml při 25 °C. Sraženina byla zachycena odsávací filtrací a třikrát rozpuštěna ve vodě. Chroman měďnato-amonný se sušil při teplotě 75-80 °C přes noc. Ten byl rozemlet na prášek a po malých dávkách přidán do litrové baňky s 3 hrdly vybavené nerezovým míchadlem typu Hershberg, které se škrábalo těsně u dna baňky. Baňka byla částečně ponořena do olejové lázně o teplotě 350 °C (při teplotě 300-320 °C lze dosáhnout dobrých výsledků). Doba přidávání byla 15 min (uvolňovalo se hodně výparů) a po dokončení všeho se směs míchala při 350 °C dalších 15 min. Ochlazený a černý prachový prášek se použil jako pro dehydrogenaci.
Roztok 260 g trihydrátu dusičnanu měďnatého(II)v 900 ml vody z vodovodu při 80 °C byl za stálého míchání přidán k roztoku 178 g dihydrátu dichromanu sodného a 225 ml 28% NH4OH doplněného na 900 ml při 25 °C. Sraženina byla zachycena odsávací filtrací a třikrát rozpuštěna ve vodě. Chroman měďnato-amonný se sušil při teplotě 75-80 °C přes noc. Ten byl rozemlet na prášek a po malých dávkách přidán do litrové baňky s 3 hrdly vybavené nerezovým míchadlem typu Hershberg, které se škrábalo těsně u dna baňky. Baňka byla částečně ponořena do olejové lázně o teplotě 350 °C (při teplotě 300-320 °C lze dosáhnout dobrých výsledků). Doba přidávání byla 15 min (uvolňovalo se hodně výparů) a po dokončení všeho se směs míchala při 350 °C dalších 15 min. Ochlazený a černý prachový prášek se použil jako pro dehydrogenaci.
Syntéza gama- butyrolaktonu z tetrahydrofuranu (THF).
K míchané směsi 7,2 g (0,1 mol) tetrahydrofuranu ve 100 ml vody bylo přidáno 15,1 g bromičnanu sodného a 13,6 g (0,1 mol) hydrogensíranu draselného. Pro udržení teploty roztoku v rozmezí 25-30 °C bylo nutné vnější chlazení. Míchání pokračovalo 16 hodin při pokojové teplotě, po této době byl spotřebován veškerý THF. K uhasení přebytečného vzniklého bromu byl použit kyselý roztok siřičitanu sodného [stejně dobře by měl fungovat i disiřičitan]. Bylo tedy přidáno 140-150 ml 10% roztoku a 13,6 g (0,1 mol) hydrogensíranu draselného. Reakce byla ochlazena a extrahována 5x30 ml dichlormethanu. Spojené organické vrstvy byly vysušeny nad MgSO4 a rozpouštědlo odstraněno ve vakuu. Zbytek byl vydestilován za vzniku gama-butyrolaktonu ve výtěžku 73 % (bp 204-205 °C).
Sandmeyerova reakce GABA na GBL/GHB.
Je úžasná pro chemika, který chce připravit GHB v malých množstvích a vysokých výtěžcích, a to bez přímého získávání jakýchkoli regulovaných chemických látek, jako je gama-butyrolakton (GBL) nebo 1,4-butandiol (BDO). Vyhýbá se také typicky nízkým výtěžkům, které se vyskytují při oxidaci tetrahydrofuranu (THF). Používá snadno získatelnou aminokyselinu, kyselinu gama-aminomáselnou (GABA), a dusitan sodný (NaNO2). Velmi pěkně se škáluje a funguje bez větších potíží. Nepoužívá se žádná podezřelá chemikálie.
Sandmeyerova reakce využívá kyselinu dusičnou k přeměně aminů na diazoniové soli. Tato reakce, jak se uplatňuje při přeměně GABA na GHB, je znázorněna v první reakci níže. Alifatické diazoniové soli rychle podléhají hydrolýze v přítomnosti vody, přičemž se uvolňuje plynný dusík a zůstává hydroxylová skupina. To je znázorněno ve druhém kroku. V důsledku těchto reakcí lze GABA přeměnit na GHB snadno proveditelnou reakcí v jednom hrnci.
Spuštění reakce.
Připravte 2l baňku, která je umístěna v ledové vodě na magnetickém míchadle. Nyní.
Spuštění reakce.
Připravte 2l baňku, která je umístěna v ledové vodě na magnetickém míchadle. Nyní.
- Přidejte 3mol GABA (309,4 g).
- Přidejte 3mol NaNO2 (207,0 g).
- Přidejte 700 ml vody (celkový objem je asi 1100 ml).
- Vhoďte 1" míchadlo a začněte míchat.
- Naplňte 500 ml tlakově vyrovnanou adiční nálevku 3,3 mol HCl(aq) (385,0 g 31,25 %, 334,8 ml 31,25 %).
- Přídavnou nálevku opatřete nástavcem pro výstup plynu a odvzdušněte ji.
Začněte pomalu kapat kyselinu chlorovodíkovou do směsi. Kapejte ji konstantní rychlostí přibližně 1 kapku za 2-5 sekund. Postupem času zrychlujte a podle potřeby vyměňujte led, ale nedovolte, aby se vývin hnědého jedovatého plynu stal prudkým. Přibližně po jedné hodině od přidání poslední kapky kyseliny již není třeba led vyměňovat. Jakmile je reakce ukončena, pokračujte v extrakci. (obvykle o 24-36 hodin později)
Extrakce.
Existuje mnoho možností, jak ji provést. Na tomto postupu se stále pracuje, ale po asi 20 provedeních jsem dospěl k využití této práce. K extrakci rozpouštědlem můžete použít ethylacetát (EtOAc), chloroform nebo methylenchlorid (dichlormethan alias DCM). Obvykle jsem používal DCM, protože je to příjemné, protože organická vrstva klesá na dno dělící nálevky.
1. Nastavení pro jednoduchou destilaci
Extrakce.
Existuje mnoho možností, jak ji provést. Na tomto postupu se stále pracuje, ale po asi 20 provedeních jsem dospěl k využití této práce. K extrakci rozpouštědlem můžete použít ethylacetát (EtOAc), chloroform nebo methylenchlorid (dichlormethan alias DCM). Obvykle jsem používal DCM, protože je to příjemné, protože organická vrstva klesá na dno dělící nálevky.
1. Nastavení pro jednoduchou destilaci
a) Destilujte, přičemž prvních asi 5-10 ml destilátu vyhoďte, protože bude obsahovat poměrně velké množství oxidů dusíku. Odestilujte co nejvíce vody, v podstatě dokud se chlorid sodný nezačne sytit vodnou vrstvou a srážet se.
b) Zbytek destilátu (přibližně 700 ml) bude obsahovat přibližně 1 g GBL/10 ml.
c) Zbytek destilátu ošetřete NaHCO3 při refluxu po dobu 30 minut.
d) Vařte s přibližně 5 % objemu aktivního uhlí (tj. 0,35 ml aktivního uhlí) (v porovnání s objemem roztoku) po dobu 5-10 min.
e) Nechte vychladnout a přefiltrujte, dřevěné uhlí promyjte destilovanou vodou. NaGHB uschovejte.
2. Se zbytkem vodného roztoku extrahujte 5krát 625ml porcí DCM.
3. Zbytek vodného roztoku extrahujte. Oddestilujte DCM (DCM použijte znovu!).
4. Zbytek destilujte. Destilujte GBL (ve vakuu, pokud je k dispozici).
5 . Reagujte s NaHCO3 a destilovanou vodou a ošetřete aktivním uhlím jako předtím.
Obvykle se z GBL extrahovaného rozpouštědlem vyrobí 375 g NaGHB, z toho 100 g NaGHB z vodného destilátu. Přestože konverze je téměř kvantitativní (měřeno pomocí GC/MS), celkový výtěžek je obvykle asi 70 %.
3. Zbytek vodného roztoku extrahujte. Oddestilujte DCM (DCM použijte znovu!).
4. Zbytek destilujte. Destilujte GBL (ve vakuu, pokud je k dispozici).
5 . Reagujte s NaHCO3 a destilovanou vodou a ošetřete aktivním uhlím jako předtím.
Obvykle se z GBL extrahovaného rozpouštědlem vyrobí 375 g NaGHB, z toho 100 g NaGHB z vodného destilátu. Přestože konverze je téměř kvantitativní (měřeno pomocí GC/MS), celkový výtěžek je obvykle asi 70 %.
Last edited:
