G.Patton
Expert
- Joined
- Jul 5, 2021
- Messages
- 2,659
- Solutions
- 3
- Reaction score
- 2,734
- Points
- 113
- Deals
- 1
Einleitung.
Diese Datei befasst sich mit der Synthese von GHB und verwandten Verbindungen. Es ist höchst gefährlich, eine Synthese von GHB ohne die entsprechenden Kenntnisse der praktischen organischen Chemie zu versuchen. Der weitaus einfachste Weg zur Herstellung von GHB ist die Hydrolyse des entsprechenden Lactons (eines cyclischen intramolekularen Esters) zur gewünschten Hydroxysäure. Die Esterhydrolyse kann auf zwei Arten durchgeführt werden: Eine säurekatalysierte Reaktion oder eine basenkatalysierte Reaktion. Wir entscheiden uns hier für die basenkatalysierte Reaktion, da sie nicht reversibel ist wie die säurekatalysierte Reaktion und wir daher eine höhere Ausbeute erzielen und das Natriumsalz von GHB erhalten, da die freie Säure nicht stabil ist und sofort wieder zu Gamma-Butyrolacton cyclisiert.
Umwandlung von Gamma-Butyrolacton in Natrium-Gamma-Hydroxybutyrat (Na-GHB).
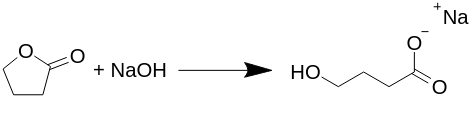
Die Reaktion verläuft äquimolar (jedes Molekül reagiert in der gleichen Anzahl), und es entstehen bei dieser Reaktion keine Nebenprodukte wie Wasserstoffgas, Wasser oder etwas anderes, wie in verschiedenen anderen Texten vorgeschlagen. Beiallen veröffentlichten Zubereitungen von GHB, oder korrekter Na-GHB, wird Butyrolacton mit Natriumhydroxid in verschiedenen Lösungsmitteln, in der Regel in wässrigem Alkohol, refluxiert, was jedoch nicht notwendig ist.
Physikalische/chemische Eigenschaften.
gamma-Butyrolacton.
Molgewicht 86,09; mp -43,53 °C; bp 204°C; d 1,12 g/ml
CAS-Nr.: [96-48-0]
Mischbar mit Wasser, löslich in Methanol, Ethanol, Aceton, Ether, Benzol
LD50: 1720 mg/kg (oral, Maus) 1540 mg/kg (oral, Ratte)
Verwendungen: Lösungsmittel, Farbentferner, Kondensatorelektrolyt, in der organischen Chemie
Synonyme: GBL, BLO, Butyrolacton, Gamma-Hydroxybuttersäurelacton, 1,2-Butanolid, 1,4-Butanolid, 4-Butanolid, 2-Oxanolon, Tetrahydro-2-furanon, Dihydro-2(3H)-furanon.
Natrium-GHB.
Mol wt 126.09; mp 145-146 °C
CAS-Nr.: [502-85-2]
LD50:2700 mg/kg (oral, Ratte)
Synonyme: Gamma-OH, Natriumoxybat, Natrium-Gamma-Oxybutyrat, Somatomax PM, Wy-3478, NSC-84223, Somsanit, Anetamin.
Kalium GHB.
Mol wt: 142.20
Calcium GHB.
Mol wt 246.16; mp 164-166 °C, 166-168 °C.
Magnesium GHB.
Mol wt 230.39; mp (wasserfrei) 172-174 °C; Tetrahydrat 118-120 °C; Pentahydrat 76-78 °C.
Molgewicht 86,09; mp -43,53 °C; bp 204°C; d 1,12 g/ml
CAS-Nr.: [96-48-0]
Mischbar mit Wasser, löslich in Methanol, Ethanol, Aceton, Ether, Benzol
LD50: 1720 mg/kg (oral, Maus) 1540 mg/kg (oral, Ratte)
Verwendungen: Lösungsmittel, Farbentferner, Kondensatorelektrolyt, in der organischen Chemie
Synonyme: GBL, BLO, Butyrolacton, Gamma-Hydroxybuttersäurelacton, 1,2-Butanolid, 1,4-Butanolid, 4-Butanolid, 2-Oxanolon, Tetrahydro-2-furanon, Dihydro-2(3H)-furanon.
Natrium-GHB.
Mol wt 126.09; mp 145-146 °C
CAS-Nr.: [502-85-2]
LD50:2700 mg/kg (oral, Ratte)
Synonyme: Gamma-OH, Natriumoxybat, Natrium-Gamma-Oxybutyrat, Somatomax PM, Wy-3478, NSC-84223, Somsanit, Anetamin.
Kalium GHB.
Mol wt: 142.20
Calcium GHB.
Mol wt 246.16; mp 164-166 °C, 166-168 °C.
Magnesium GHB.
Mol wt 230.39; mp (wasserfrei) 172-174 °C; Tetrahydrat 118-120 °C; Pentahydrat 76-78 °C.
Laborverfahren für die Synthese von GHB-Salzen.
Bitte beachten Sie die üblichen Sicherheitsmaßnahmen im Labor. Tragen Sie einen Laborkittel und eine Schutzbrille. Sie werden mit heißen ätzenden Lösungen und Lösungsmitteln arbeiten! Seien Sie sich der Risiken bewusst, die mit der Herstellung von GHB verbunden sind! Arbeiten Sie niemals allein!
Natrium GHB.
Verfahren:
Lösen Sie 130 g (3,25 mol) reines Natriumhydroxid in 400 ml destilliertem Wasser in einem 1000 ml Dreihalskolben unter Rühren auf. Die Auflösung ist exotherm und die Lösung wird sich erwärmen. Zur Temperaturregelung kann ein Kaltwasserbad verwendet werden. Wenn sich alles zu einer klaren Lösung aufgelöst hat, gibt man langsam und unter gutem Rühren 250 ml (280 g, 3,25 Mol) Gamma-Butyrolacton in 50-ml-Portionen hinzu. Die Verwendung eines Tropftrichters wird empfohlen. Die Zugabe von gamma-Butyrolacton zur Natriumhydroxidlösung ist ebenfalls exotherm, und wenn sie zu schnell erfolgt, beginnt die Lösung zu sieden, was wir nicht wollen. Behalten Sie die Temperatur mit einem Eintauchthermometer im Auge. Die Zugabe des Gamma-Butyrolactons wird etwa 20-30 Minuten dauern. Wenn alles zugegeben wurde, lassen Sie die Mischung weitere 10 Minuten unter gelegentlichem Rühren reagieren.
Jetzt ist es an der Zeit, den pH-Wert mit Universal-pH-Papier zu überprüfen, um festzustellen, ob die Reaktion abgeschlossen ist. Wir streben einen pH-Wert von 7-8 an. Wenn der pH-Wert zu hoch ist (pH > 8), fügt man 10 ml Gamma-Butyrolacton hinzu und lässt die Reaktion noch ein paar Minuten weiterlaufen. Wenn der pH-Wert zu niedrig ist (pH < 7), fügen Sie einige ml konzentrierte wässrige NaOH-Lösung hinzu. Fahren Sie auf diese Weise fort, bis der pH-Wert innerhalb der gewünschten Grenzen liegt.
Die Lösung ist vollkommen klar und schmeckt leicht salzig. Sie kann leicht gelblich gefärbt sein, aber nicht sehr stark, wenn genügend reines Butyrolacton verwendet wurde (durch Destillation des Lactons vor der Verwendung wird dieses Problem gelöst, b.p. 204 °C). Wird eine zu basische Lösung mit einer Säure neutralisiert (anstatt mehr Lacton hinzuzufügen), können Kristalle des Natriumsalzes der Säure in der Lösung ausfallen, und der Geschmack wird stark beeinträchtigt. Die endgültige Lösung wird etwa 750 ml, 50% NaGHB betragen. Die Lösung kann (durch Abkochen des überschüssigen Wassers) auf ~600 ml konzentriert werden, ohne dass sie bei Raumtemperatur kristallisiert, aber wenn man sie auf ~500 ml konzentriert, erstarrt sie unweigerlich.
Jetzt ist es an der Zeit, den pH-Wert mit Universal-pH-Papier zu überprüfen, um festzustellen, ob die Reaktion abgeschlossen ist. Wir streben einen pH-Wert von 7-8 an. Wenn der pH-Wert zu hoch ist (pH > 8), fügt man 10 ml Gamma-Butyrolacton hinzu und lässt die Reaktion noch ein paar Minuten weiterlaufen. Wenn der pH-Wert zu niedrig ist (pH < 7), fügen Sie einige ml konzentrierte wässrige NaOH-Lösung hinzu. Fahren Sie auf diese Weise fort, bis der pH-Wert innerhalb der gewünschten Grenzen liegt.
Die Lösung ist vollkommen klar und schmeckt leicht salzig. Sie kann leicht gelblich gefärbt sein, aber nicht sehr stark, wenn genügend reines Butyrolacton verwendet wurde (durch Destillation des Lactons vor der Verwendung wird dieses Problem gelöst, b.p. 204 °C). Wird eine zu basische Lösung mit einer Säure neutralisiert (anstatt mehr Lacton hinzuzufügen), können Kristalle des Natriumsalzes der Säure in der Lösung ausfallen, und der Geschmack wird stark beeinträchtigt. Die endgültige Lösung wird etwa 750 ml, 50% NaGHB betragen. Die Lösung kann (durch Abkochen des überschüssigen Wassers) auf ~600 ml konzentriert werden, ohne dass sie bei Raumtemperatur kristallisiert, aber wenn man sie auf ~500 ml konzentriert, erstarrt sie unweigerlich.
Herstellung von Natrium-GHB mit Natriumbicarbonat (Backsoda, NaHCO3).
273 g NaHCO3 (3,25 Mol) werden in einem Dreihalskolben mit rundem Boden zu 1125 mL destilliertem Wasser gegeben. Die Lösung wird unter Rühren mit einem Glasstab oder ähnlichem langsam zum Kochen gebracht. Das gesamte Natriumhydroxid löst sich auf. Beim Aufkochen der Lösung wird Kohlendioxid austreten. Dabei handelt es sichum das Natriumbicarbonat, das sich in eine etwas stärkere Base, Natriumcarbonat, auflöst.
Reduzieren Sie die Hitze auf ein leichtes Sieden und geben Sie langsam 250 ml gamma-Butyrolacton (280 g, 3,25 Mol) hinzu. Die Zugabe ist nicht sofort exotherm, wie bei der Natriumhydroxid-Synthese. Diese Lösung wird 30 Minuten lang leicht zum Sieden gebracht. Überprüfen Sie den pH-Wert mit Universal-pH-Papier. Angestrebt wird ein pH-Wert um 7, aber auch ein Wert zwischen 6 und 8 ist völlig sicher. Wenn der pH-Wert zu hoch ist, fügen Sie eine kleine Menge GBL hinzu und fahren Sie mit dem Rückfluss fort.
Die Lösung ist vollkommen klar und sollte absolut farblos sein. Ist sie nicht völlig farblos, d. h. wurde etwas unreines Butyrolacton verwendet und hat die Lösung eine hellgelbe Farbe angenommen, so gibt man etwa 100 mL Aktivkohle hinzu. Dies lässt man 10 Minuten lang kochen. Die Lösung abkühlen lassen, filtrieren und die Aktivkohle zwei- oder dreimal mit 50 ml kaltem Wasser waschen. Bei dieser Synthese werden 410 g NaGHB hergestellt. Diese Lösung kann auf etwa 50 % NaGHB konzentriert werden, bevor sie zu kristallisieren beginnt. Wenn Sie ein Pulver wünschen, erhitzen Sie die Lösung auf 150 °C, gießen sie dann in eine gekühlte Pyrex-Schale und lassen sie abkühlen und erstarren. Diese Synthese ist ideal, wenn kein ACS-, Lebensmittel- oder Elektronik-Natriumhydroxid verfügbar ist.
Die Lösung ist vollkommen klar und sollte absolut farblos sein. Ist sie nicht völlig farblos, d. h. wurde etwas unreines Butyrolacton verwendet und hat die Lösung eine hellgelbe Farbe angenommen, so gibt man etwa 100 mL Aktivkohle hinzu. Dies lässt man 10 Minuten lang kochen. Die Lösung abkühlen lassen, filtrieren und die Aktivkohle zwei- oder dreimal mit 50 ml kaltem Wasser waschen. Bei dieser Synthese werden 410 g NaGHB hergestellt. Diese Lösung kann auf etwa 50 % NaGHB konzentriert werden, bevor sie zu kristallisieren beginnt. Wenn Sie ein Pulver wünschen, erhitzen Sie die Lösung auf 150 °C, gießen sie dann in eine gekühlte Pyrex-Schale und lassen sie abkühlen und erstarren. Diese Synthese ist ideal, wenn kein ACS-, Lebensmittel- oder Elektronik-Natriumhydroxid verfügbar ist.
Kalium-GHB.
Verwenden Sie die oben beschriebene Ethanol-Synthese für Natrium-GHB, ersetzen Sie jedoch die 130 g NaOH durch 182 g KOH (diese Berechnung basiert auf dem schwereren K-Atom und dem höheren Wassergehalt von KOH gegenüber NaOH). Durch die Verwendung von KOH erhalten die Benutzer von K-GHB die Kaliumergänzung, die manche im Zusammenhang mit der Verabreichung von GHB für erforderlich halten. Es ist zu beachten, dass (pulverisiertes) K-GHB etwas weniger aktiv (nach Gewicht) ist als Na-GHB, da das K-Ion schwerer ist als das Na-Pendant. Der Unterschied zwischen K-GHB und Na-GHB besteht darin, dass das K-Salz wasserlöslicher ist als das Na-Salz und dass der Geschmack eher nach Salz/Lakritz als nach Salz/Seife wie bei Na-GHB schmeckt.
Calcium-GHB.
74 g analytisch reines Calciumhydroxid werden in 200 ml destilliertem Wasser suspendiert. 160 ml 4-Butyrolacton werden portionsweise (jede Portion etwa 5 bis 10 ml) und unter Rühren zu dieser Suspension bei Raumtemperatur gegeben. Nach Zugabe von 20 ml erwärmt sich das Reaktionsgemisch auf etwa 50 °C bis 60 °C. Die Zugabe von 4-Butyrolacton wird so gesteuert, dass die Temperatur zwischen etwa 50 °C und 60 °C bleibt, was etwa 1 Stunde dauert. In dieser Zeit hat sich das Calciumhydroxid praktisch vollständig aufgelöst. Das Reaktionsmaterial ist mit einem leichten rostgelben Niederschlag verunreinigt. Man verdünnt ihn mit 300 ml Methanol, lässt ihn vier Stunden stehen und filtriert ihn dann durch einen Faltenfilter. Das klare Filtrat wird vorsichtig mit 200 ml Aceton behandelt, und zwar in der Weise, dass man nach jeder Portion Aceton, die einen Niederschlag verursacht, Zeit lässt, damit sich der Niederschlag wieder auflöst. Man erhält eine wasserklare Lösung, die man zum Auskristallisieren aufstellt. Nach zweistündiger Standzeit beginnen sich farblose Kristalle abzusetzen. In diesem Zustand wird die Kristallisation durch kontinuierliche Zugabe von Aceton (insgesamt 100 ml) beschleunigt. Die Kristallisationszeit beträgt 24 Stunden. Die Kristalle werden abgesaugt und zunächst mit 50 ml Methanol und dann zusätzlich mit 60 ml Aceton gewaschen. Die Kristalle werden bei Temperaturen von etwa 60 °C bis 80 °C in einem Trockenschrank getrocknet. Ausbeute: 230 g. Schmelzpunkt 166-168 °C. (sofort). Das Produkt ist das wasserfreie, nicht hygroskopische Calciumsalz der 4-Hydroxybuttersäure. Es ist beliebig in Wasser löslich, die wässrige Lösung hat einen pH-Wert von 7 bis 7,5. Das Salz kann beliebig lange gelagert werden und verändert sich an der Luft nicht. Auch bei der Lagerung wird kein Wasser aus der Luft angezogen.
Der Rückstand kristallisiert zu einer Masse farbloser Kristalle aus, die bei Temperaturen von etwa 60 °C bis 80 °C getrocknet wird. Ausbeute: etwa 105 g. Schmelzpunkt 164-166 °C. Das Produkt ist Di-(4-hydroxybuttersäure)-Calcium. Es wird umkristallisiert, indem man es in etwas Methanol löst, anschließend Aceton bis zur Trübung hinzufügt und in der Kälte kristallisiert.
Anstelle von Methanol können auch Ethanol und Isopropanol mit gleichem Erfolg zur Umkristallisation verwendet werden. Ohne Verwendung von wasserhaltigen Alkoholen als Umkristallisationsmedium oder als Zusatz bei der Umkristallisation und Reinigung werden keine stabilen und insbesondere keine nichthygroskopischen Calciumsalze erhalten. Der Wassergehalt der Alkohole sollte etwa 3-10 Volumenprozent betragen. Das so erhaltene Endprodukt löst sich leicht in Wasser, ist nicht hygroskopisch und hat einen angenehmen aromatischen Geruch.
Der Rückstand kristallisiert zu einer Masse farbloser Kristalle aus, die bei Temperaturen von etwa 60 °C bis 80 °C getrocknet wird. Ausbeute: etwa 105 g. Schmelzpunkt 164-166 °C. Das Produkt ist Di-(4-hydroxybuttersäure)-Calcium. Es wird umkristallisiert, indem man es in etwas Methanol löst, anschließend Aceton bis zur Trübung hinzufügt und in der Kälte kristallisiert.
Anstelle von Methanol können auch Ethanol und Isopropanol mit gleichem Erfolg zur Umkristallisation verwendet werden. Ohne Verwendung von wasserhaltigen Alkoholen als Umkristallisationsmedium oder als Zusatz bei der Umkristallisation und Reinigung werden keine stabilen und insbesondere keine nichthygroskopischen Calciumsalze erhalten. Der Wassergehalt der Alkohole sollte etwa 3-10 Volumenprozent betragen. Das so erhaltene Endprodukt löst sich leicht in Wasser, ist nicht hygroskopisch und hat einen angenehmen aromatischen Geruch.
Magnesium-GHB .
60 g Magnesiumhydroxid (analytische Qualität) werden unter Rühren in 200 ml Leitungswasser suspendiert. In diese Suspension werden in einem Strom und unter Rühren 160 ml Butyrolacton eingemischt. Dann wird das Gemisch in einem 2-Liter-Kolben 6 Stunden lang unter Rühren auf einem Wasserbad erhitzt. Das Magnesiumhydroxid löst sich dabei praktisch vollständig auf. Der Kolben wird über Nacht stehen gelassen, wobei sich Verunreinigungen ablagern und die Lösung mühelos vom Verunreinigungsdepot dekantiert wird. Das wasserklare Dekantat wird zunächst 10 Minuten lang mit 100 ml Aceton gerührt. Die farblose, sirupartige Flüssigkeit, die nun zähflüssiger geworden ist, wird erneut mit 100 ml Aceton wie oben beschrieben vermischt, das Aceton wird erneut durch Dekantieren entfernt und der ziemlich zähflüssige, farblose Sirup wird bei Raumtemperatur etwa 2 bis 4 Stunden stehen gelassen. Er erstarrt zu einer farblosen kristallinen Masse, die in einem Mörser zerkleinert und mehrere Stunden an der Luft getrocknet wird. Schmelzpunkt 76 °C bis 78 °C. Ausbeute: 314 g in analytisch reiner Form.
Dieses Magnesiumsalz enthält etwa 5 Mol Hydratationswasser. Es ist nicht hydroskopisch, stabil und kann beliebig lange gelagert werden. Durch mehrstündiges Trocknen bei 40 °C bis 50 °C verliert es einen Teil seines Kristallwassers (1 Mol) und schmilzt dann bei 118 °C bis 120 °C. Wasserfreies Magnesium-4-hydroxybutyrat kann durch Entfernung von Wasser durch Sublimation und/oder Verdampfung von Wasser unter verringertem Partialdruck des Wassers und bei erhöhter Temperatur oder durch Kristallisation aus einer Lösung, die ein organisches Lösungsmittel enthält,hergestellt werden. Das wasserfreie Salz schmilzt bei 172-174 °C. Die chemische Analyse ergibt 10,50 Gewichtsprozent Magnesium (rechnerisch 10,55% Gewichtsprozent Magnesium). Alle Modifikationen sind nicht hygroskopisch und lagerstabil. 1 g des Magnesiumsalzes löst sich in 2 ml Wasser bei Raumtemperatur, der pH-Wert der wässrigen Lösung beträgt 7. Es löst sich leicht in Wasser, Methanol und Ethanol, löst sich nicht in Ether und Kohlenwasserstoffen, ist nicht hygroskopisch, ist lagerfähig und hat einen angenehmen aromatischen Geruch.
Dieses Magnesiumsalz enthält etwa 5 Mol Hydratationswasser. Es ist nicht hydroskopisch, stabil und kann beliebig lange gelagert werden. Durch mehrstündiges Trocknen bei 40 °C bis 50 °C verliert es einen Teil seines Kristallwassers (1 Mol) und schmilzt dann bei 118 °C bis 120 °C. Wasserfreies Magnesium-4-hydroxybutyrat kann durch Entfernung von Wasser durch Sublimation und/oder Verdampfung von Wasser unter verringertem Partialdruck des Wassers und bei erhöhter Temperatur oder durch Kristallisation aus einer Lösung, die ein organisches Lösungsmittel enthält,hergestellt werden. Das wasserfreie Salz schmilzt bei 172-174 °C. Die chemische Analyse ergibt 10,50 Gewichtsprozent Magnesium (rechnerisch 10,55% Gewichtsprozent Magnesium). Alle Modifikationen sind nicht hygroskopisch und lagerstabil. 1 g des Magnesiumsalzes löst sich in 2 ml Wasser bei Raumtemperatur, der pH-Wert der wässrigen Lösung beträgt 7. Es löst sich leicht in Wasser, Methanol und Ethanol, löst sich nicht in Ether und Kohlenwasserstoffen, ist nicht hygroskopisch, ist lagerfähig und hat einen angenehmen aromatischen Geruch.
Andere Salze.
Die Lithium- und Ammoniumsalze von GHB wären bei der Einnahme gefährlich. Lithium-Ion ist giftig und bildet zusammen mit NH3-Lacton Pyrrolidon.
Synthese F&A.
F: Kann ich anstelle von reinem Natriumhydroxid Lauge verwenden?
A: Nein, das könnte unvorhersehbare Folgen für Ihre Gesundheit haben. Die Lauge aus dem Baumarkt hat nicht annähernd die strengen Reinheitskriterien von z. B. Lebensmittelqualität, ACS-Qualität oder Elektronikqualität. Einige Leute erzählen von erfolgreichen Geschichten mit Lauge, was wirklich möglich ist, aber wie gesagt, die Ergebnisse sind unvorhersehbar.
F: Ich habe nicht die Glasgeräte, die Sie sagen, dass man sie braucht, kann ich die Lösung stattdessen in einem Topf auf dem Herd kochen?
A: Nein, das können Sie nicht. Das Natriumhydroxid würde das Metall angreifen, und verschiedene Metallionen würden in Ihr Produkt gelangen. Sie können natürlich einfachere Glasgeräte als in meinen Vorschlägen verwenden und die notwendigen Anpassungen des Verfahrens vornehmen.
F: Ich kann Na-GHB nicht aus Ethanol umkristallisieren. Es bildet eine klebrige Masse.
A: Ihr Na-GHB ist nicht trocken, oder Ihr Ethanol ist nicht wasserfrei. Wasser macht die Rekristallisation fast unmöglich. Die Tatsache, dass das Natrium-GHB zerfließt (hygroskopisch ist), macht die Sache nicht besser. Sie müssen das GHB gründlich trocknen, vorzugsweise in einem Vakuum-Exsikkator, bevor Sie eine Rekristallisation oder eine andere improvisierte Alternative versuchen. Das Ethanol, das Sie verwenden wollen (es wird meist in einer Reinheit von 95 % geliefert, der Rest ist Wasser), muss durch Trocknung über wasserfreiem Kalziumsulfat und anschließende Destillation aus Kalziumoxid getrocknet werden, wobei geeignete Maßnahmen getroffen werden müssen, um Feuchtigkeit von der Reaktion auszuschließen.
F: Wo kann ich Butyrolacton kaufen/Ist es sicher, Butyrolacton zu kaufen?
A: Ich habe keine Ahnung, wie die Situation bei Ihnen in Ihrem Land ist. Die Antworten auf diese Fragen hängen stark davon ab, wer Sie sind und wo Sie leben. Sie können sich jedoch an einen der vielen Verkäufer von GHB-Kits wenden, die Sie online finden können.
A: Nein, das könnte unvorhersehbare Folgen für Ihre Gesundheit haben. Die Lauge aus dem Baumarkt hat nicht annähernd die strengen Reinheitskriterien von z. B. Lebensmittelqualität, ACS-Qualität oder Elektronikqualität. Einige Leute erzählen von erfolgreichen Geschichten mit Lauge, was wirklich möglich ist, aber wie gesagt, die Ergebnisse sind unvorhersehbar.
F: Ich habe nicht die Glasgeräte, die Sie sagen, dass man sie braucht, kann ich die Lösung stattdessen in einem Topf auf dem Herd kochen?
A: Nein, das können Sie nicht. Das Natriumhydroxid würde das Metall angreifen, und verschiedene Metallionen würden in Ihr Produkt gelangen. Sie können natürlich einfachere Glasgeräte als in meinen Vorschlägen verwenden und die notwendigen Anpassungen des Verfahrens vornehmen.
F: Ich kann Na-GHB nicht aus Ethanol umkristallisieren. Es bildet eine klebrige Masse.
A: Ihr Na-GHB ist nicht trocken, oder Ihr Ethanol ist nicht wasserfrei. Wasser macht die Rekristallisation fast unmöglich. Die Tatsache, dass das Natrium-GHB zerfließt (hygroskopisch ist), macht die Sache nicht besser. Sie müssen das GHB gründlich trocknen, vorzugsweise in einem Vakuum-Exsikkator, bevor Sie eine Rekristallisation oder eine andere improvisierte Alternative versuchen. Das Ethanol, das Sie verwenden wollen (es wird meist in einer Reinheit von 95 % geliefert, der Rest ist Wasser), muss durch Trocknung über wasserfreiem Kalziumsulfat und anschließende Destillation aus Kalziumoxid getrocknet werden, wobei geeignete Maßnahmen getroffen werden müssen, um Feuchtigkeit von der Reaktion auszuschließen.
F: Wo kann ich Butyrolacton kaufen/Ist es sicher, Butyrolacton zu kaufen?
A: Ich habe keine Ahnung, wie die Situation bei Ihnen in Ihrem Land ist. Die Antworten auf diese Fragen hängen stark davon ab, wer Sie sind und wo Sie leben. Sie können sich jedoch an einen der vielen Verkäufer von GHB-Kits wenden, die Sie online finden können.
Vorläufer.
Der offensichtliche Ausgangsstoff für die Synthese von GHB ist Gamma-Butyrolacton. Es kann aus Vorläufern wie Tetrahydrofuran (THF) mit Oxidationsmitteln wie Rutheniumtetroxid, Calciumhypochlorit und Salpetersäure hergestellt werden. Es können auch 4-Halogenbuttersäurederivate (Chlor, Brom, Iod) verwendet werden. Sie können wie in der nachstehenden Synthese durch Destillation mit Natriummethoxid in gamma-Butyrolacton umgewandelt werden.
gamma-Butyrolacton aus 4-Brombuttersäure.
Einer Lösung von 7,8 g Natrium in 500 ml absolutem Alkohol wurden 60,5 g 4-Brombuttersäure zugesetzt. Das Reaktionsgemisch wurde unter einem Rückflusskühler etwa fünf Stunden lang gekocht. Während dieser Zeit trennte sich das Natriumbromid ab. Der Alkohol wurde über ein Dampfbad abdestilliert, und das Lacton wurde durch Extraktion mit Ether vom Natriumbromid getrennt. Der Ether wurde eingedampft, und das Lacton wurde unter Normaldruck destilliert. Die Ausbeute betrug 21,2 g (67 %) des Produkts, das bei 202-206 °C siedet. Eine Alternative ist die radikalische Chlorierung von Buttersäure mit Schwefelchlorid in Gegenwart von Peroxiden, die Trennung der Isomere durch Destillation, die Herstellung des Natriumsalzes der 4-Chlorbuttersäure und die Cyclisierung zum Lacton wie beim 4-Brom-Derivat oben. gamma-Butyrolacton kann auch aus 4-Methoxybuttersäure, 3-Phenoxypropylcyanid, gamma-Diethylaminobuttersäure und beta-Chlorethylvinylether sowie vielen anderen etwas zu exotischen Chemikalien hergestellt werden. Industriell wird es in der Regel durch Reaktion von Acetylen mit Formaldehyd unter hohen Temperaturen und Druck hergestellt.
Dehydrierung von 1,4-Butandiol (BDO) zu Gamma-Butyrolacton (GBL).
Ein Gemisch aus 90,1 g (1 Mol) 1,4-Butandiol, 4 g Kupferchromit-Katalysator und 0,15 g pulverisiertem Natriumhydroxid (oder besser KOH) in Reagenzienqualität wurde kräftig gerührt und unter Rückfluss erhitzt. Bei etwa 200 °C kam es zu einer lebhaften Wasserstoffentwicklung, die Temperatur sank um etwa 10 °C und die Dehydrierung verlief reibungslos. Die Gasentwicklung (39 l/2 mol pro Mol umgesetztes 1,4-Butandiol) hörte nach etwa 3 h auf. Das Reaktionsgemisch wurde auf Raumtemperatur abgekühlt, vom Katalysator abfiltriert und unter vermindertem Druck destilliert, um Gamma-Butyrolacton in etwa 80 % Ausbeute und nicht umgesetztes 1,4-Butandiol in etwa 10 % Ausbeute zu erhalten.
Herstellung eines hochaktiven Kupferchromit-Dehydrierungskatalysators.
Eine Lösung von 260 g Kupfer(II)nitrat-Trihydrat in 900 ml Leitungswasser bei 80 °C wurde unter Rühren zu einer Lösung von 178 g Natriumdichromat-Dihydrat und 225 ml 28%iger NH4OH gegeben und bei 25 °C auf 900 ml aufgefüllt. Der Niederschlag wurde durch Saugfiltration gesammelt und dreimal in Wasser aufgeschlämmt. Das Kupferammoniumchromat wurde über Nacht bei 75-80 °C getrocknet. Es wurde pulverisiert und in kleinen Portionen in einen 1-Liter-Dreihalskolben gegeben, der mit einem Edelstahlrührer vom Typ Hershberg ausgestattet war, der dicht am Boden des Kolbens schabte. Der Kolben wurde teilweise in ein Ölbad bei 350 °C getaucht (mit 300-320 °C kann man gute Ergebnisse erzielen). Die Zugabe dauerte 15 Minuten (es bildeten sich viele Dämpfe), und das Gemisch wurde bei 350 °C weitere 15 Minuten lang gerührt, nachdem alles fertig war. Das abgekühlte, schwarze, staubige Pulver wurde wie üblich für die Dehydrierung verwendet.
Eine Lösung von 260 g Kupfer(II)nitrat-Trihydrat in 900 ml Leitungswasser bei 80 °C wurde unter Rühren zu einer Lösung von 178 g Natriumdichromat-Dihydrat und 225 ml 28%iger NH4OH gegeben und bei 25 °C auf 900 ml aufgefüllt. Der Niederschlag wurde durch Saugfiltration gesammelt und dreimal in Wasser aufgeschlämmt. Das Kupferammoniumchromat wurde über Nacht bei 75-80 °C getrocknet. Es wurde pulverisiert und in kleinen Portionen in einen 1-Liter-Dreihalskolben gegeben, der mit einem Edelstahlrührer vom Typ Hershberg ausgestattet war, der dicht am Boden des Kolbens schabte. Der Kolben wurde teilweise in ein Ölbad bei 350 °C getaucht (mit 300-320 °C kann man gute Ergebnisse erzielen). Die Zugabe dauerte 15 Minuten (es bildeten sich viele Dämpfe), und das Gemisch wurde bei 350 °C weitere 15 Minuten lang gerührt, nachdem alles fertig war. Das abgekühlte, schwarze, staubige Pulver wurde wie üblich für die Dehydrierung verwendet.
Synthese von gamma-Butyrolacton aus Tetrahydrofuran (THF).
Zu einer gerührten Mischung von 7,2 g (0,1 mol) Tetrahydrofuran in 100 ml Wasser wurden 15,1 g Natriumbromat und 13,6 g (0,1 mol) Kaliumhydrogensulfat zugegeben. Um die Temperatur der Lösung zwischen 25-30 °C zu halten, war eine externe Kühlung erforderlich. Das Rühren wurde 16 Stunden lang bei Raumtemperatur fortgesetzt, bis das gesamte THF verbraucht war. Um überschüssiges Brom abzuschrecken, wurde eine saure Natriumsulfitlösung verwendet [Bisulfit sollte genauso gut funktionieren]. Dazu wurden 140-150 ml einer 10%igen Lösung und 13,6 g (0,1 mol) Kaliumhydrogensulfat zugegeben. Die Reaktion wurde abgekühlt und mit 5x30 ml Dichlormethan extrahiert. Die vereinigten organischen Schichten wurden über MgSO4 getrocknet und das Lösungsmittel unter Vakuum entfernt. Der Rückstand wurde destilliert und ergab Gamma-Butyrolacton in 73 % Ausbeute (bp 204-205 °C).
Sandmeyer-Reaktion von GABA zu GBL/GHB.
Die Sandmeyer-Reaktion eignet sich hervorragend für Chemiker, die GHB in kleinen Mengen und mit hoher Ausbeute herstellen wollen, ohne dabei direkt regulierte Chemikalien wie Gamma-Butyrolacton (GBL) oder 1,4-Butandiol (BDO) zu erhalten. Außerdem werden die typischerweise geringen Ausbeuten bei der Oxidation von Tetrahydrofuran (THF) vermieden. Es verwendet eine leicht zu beschaffende Aminosäure, Gamma-Aminobuttersäure (GABA), und Natriumnitrit (NaNO2). Es lässt sich sehr gut skalieren und läuft ohne allzu große Schwierigkeiten. Eswird keine einzige verdächtige Chemikalie verwendet.
Bei der Sandmeyer-Reaktion wird salpetrige Säure verwendet, um Amine in Diazoniumsalze umzuwandeln. Diese Reaktion, die bei der Umwandlung von GABA in GHB angewendet wird, ist in der ersten Reaktion unten dargestellt. Aliphatische Diazoniumsalze werden in Gegenwart von Wasser rasch hydrolysiert, wobei Stickstoffgas entsteht und eine Hydroxylgruppe zurückbleibt. Dies ist im zweiten Schritt dargestellt. Durch diese Reaktionen kann GABA in einer einfach durchzuführenden Eintopfreaktion in GHB umgewandelt werden.
Führedie Reaktion durch.
Richte einen 2-Liter-Kolben ein, der in Eiswasser auf einem Magnetrührer steht. Jetzt.
Führedie Reaktion durch.
Richte einen 2-Liter-Kolben ein, der in Eiswasser auf einem Magnetrührer steht. Jetzt.
- Gib 3mol GABA (309,4 g) hinzu.
- Füge3mol NaNO2 (207,0 g) hinzu.
- Füge700 ml Wasser hinzu (das Gesamtvolumen beträgt dann etwa 1100 ml).
- Einen 1"-Rührstab einlegen und mit dem Rühren beginnen.
- Einen 500-ml-Additionstrichter mit 3,3 mol HCl(aq) (385,0 g 31,25 %, 334,8 ml 31,25 %) befüllen.
- Der Zugabe-Trichter wird mit einem Gasauslassadapter versehen und nach außen entlüftet.
Beginne, die Salzsäure langsam in das Gemisch zu tropfen. Tröpfeln Sie etwa alle 2-5 Sekunden einen Tropfen hinein. Erhöhen Sie die Geschwindigkeit im Laufe der Zeit und ersetzen Sie das Eis nach Bedarf, aber achten Sie darauf, dass die Entwicklung des braunen Giftgases nicht zu heftig wird. Nach etwa einer Stunde, nachdem der letzte Tropfen Säure hinzugefügt wurde, muss das Eis nicht mehr ausgetauscht werden. Sobald die Reaktion abgeschlossen ist, kann mit der Extraktion begonnen werden. (normalerweise 24-36 Stunden später)
Extraktion.
Hierfür gibt es viele Möglichkeiten. Ich arbeite noch daran, aber nach etwa 20 Durchläufen bin ich dazu übergegangen, diese Methode zu verwenden. Für die Lösungsmittelextraktion können Sie Ethylacetat (EtOAc), Chloroform oder Methylenchlorid (Dichlormethan, auch DCM genannt) verwenden. Ich habe normalerweise DCM verwendet, da die organische Schicht auf den Boden des Scheidetrichters fällt.
1. Aufbau für eine einfache Destillation
Extraktion.
Hierfür gibt es viele Möglichkeiten. Ich arbeite noch daran, aber nach etwa 20 Durchläufen bin ich dazu übergegangen, diese Methode zu verwenden. Für die Lösungsmittelextraktion können Sie Ethylacetat (EtOAc), Chloroform oder Methylenchlorid (Dichlormethan, auch DCM genannt) verwenden. Ich habe normalerweise DCM verwendet, da die organische Schicht auf den Boden des Scheidetrichters fällt.
1. Aufbau für eine einfache Destillation
a) Destillieren, wobei die ersten 5-10 ml des Destillats verworfen werden, da sie eine beträchtliche Menge an Stickstoffoxiden enthalten. Destilliere so viel Wasser wie möglich ab, bis das Natriumchlorid beginnt, die wässrige Schicht zu sättigen und auszufallen.
b) Der Rest des Destillats (ca. 700 ml) enthält etwa 1 g GBL/10 ml.
c) Den Rest des Destillats 30 Min. lang mit NaHCO3 am Rückfluss behandeln.
d) Mit etwa 5 % des Volumens der Aktivkohle (d. h. 0,35 ml Aktivkohle) (im Vergleich zum Volumen der Lösung) 5-10 Minuten lang kochen.
e) Man lässt abkühlen, filtriert und wäscht die Aktivkohle mit destilliertem Wasser. Die NaGHB aufbewahren.
2. Mit dem Rest der wässrigen Lösung extrahiert man 5 Mal mit 625 ml DCM.
3. Destillieren Sie das DCM ab (verwenden Sie das DCM wieder!).
4. Destillieren Sie das GBL (unter Vakuum, falls vorhanden).
5. Reaktion mit NaHCO3 und destilliertem Wasser und Behandlung mit Aktivkohle wie zuvor.
Normalerweise werden 375 g NaGHB aus dem mit Lösungsmittel extrahierten GBL hergestellt, davon 100 g NaGHB aus dem wässrigen Destillat. Obwohl die Umwandlung nahezu quantitativ ist (gemessen durch GC/MS), beträgt die Gesamtausbeute in der Regel etwa 70 %.
3. Destillieren Sie das DCM ab (verwenden Sie das DCM wieder!).
4. Destillieren Sie das GBL (unter Vakuum, falls vorhanden).
5. Reaktion mit NaHCO3 und destilliertem Wasser und Behandlung mit Aktivkohle wie zuvor.
Normalerweise werden 375 g NaGHB aus dem mit Lösungsmittel extrahierten GBL hergestellt, davon 100 g NaGHB aus dem wässrigen Destillat. Obwohl die Umwandlung nahezu quantitativ ist (gemessen durch GC/MS), beträgt die Gesamtausbeute in der Regel etwa 70 %.
Last edited:
