G.Patton
Expert
- Joined
- Jul 5, 2021
- Messages
- 2,659
- Solutions
- 3
- Reaction score
- 2,734
- Points
- 113
- Deals
- 1
Bevezetés.
Ez a fájl a GHB és a kapcsolódó vegyületek szintézisével foglalkozik. A GHB szintézisének megkísérlése a gyakorlati szerves kémia megfelelő ismerete nélkül rendkívül veszélyes. A GHB előállításának messze legegyszerűbb módja a megfelelő lakton (egy ciklikus intramolekuláris észter) hidrolízise a kívánt hidroxisavvá. Az észter-hidrolízis kétféleképpen végezhető: Savval katalizált reakció vagy bázissal katalizált reakció. Itt a báziskatalizált reakciót választjuk, mert a reakció nem reverzibilis, mint a savkatalizált, ezért nagyobb hozamot kapunk, és a GHB nátriumsóját kapjuk, mivel a szabad sav nem stabil, és azonnal újra gamma-butilaktonná ciklizálódik.
Gamma-butilakton átalakítása nátrium-gamma-hidroxi-butiráttá (Na-GHB).
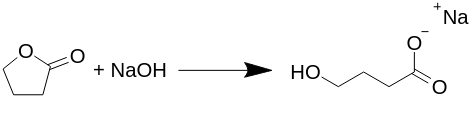
A reakció ekvimolárisan megy végbe (minden molekulából ugyanannyi reagál), és ebben a reakcióban nem keletkeznek melléktermékek, mint például hidrogéngáz, víz vagy bármi más, ahogy azt számos más szövegben javasolták. AGHB, vagy helyesebben Na-GHB minden közzétett készítménye a butilaktont nátrium-hidroxiddal különböző oldószerekben, általában vizes alkoholban refluxálja, de ez nem szükséges.
Fizikai/kémiai tulajdonságok.
gamma-butilakton.
Mol tömeg 86,09; mp -43,53 °C; bp 204°C; d 1,12 g/ml
CAS-szám: [96-48-0]
Vízzel elegyedik, oldódik metanolban, etanolban, etanolban, acetonban, éterben, benzolban
LD50: 1720 mg/kg (szájon át, egér) 1540 mg/kg (szájon át, patkány)
Felhasználás: Oldószer, festékeltávolító, kondenzátor elektrolit, a szerves kémiában
Szinonimák: GBL, BLO, butilakton, gamma-hidroxi-vajsavlakton, 1,2-butanolid, 1,4-butanolid, 4-butanolid, 2-oxanolon, tetrahidro-2-furanon, dihidro-2(3H)-furanon.
Nátrium-GHB.
Mol wt 126,09; mp 145-146 °C
CAS-szám: [502-85-2]
LD50:2700 mg/kg (szájon át, patkány)
Szinonimák: Gamma-OH, nátriumoxibát, nátrium-gamma-oxibutirát, Somatomax PM, Wy-3478, NSC-84223, Somsanit, Anetamin.
Kálium GHB.
Mol wt: 142,20
Kalcium GHB.
Mol tömeg 246,16; mp 164-166 °C, 166-168 °C.
Magnézium GHB.
Mol tömeg 230,39; mp (vízmentes) 172-174 °C; tetrahidrát 118-120 °C; pentahidrát 76-78 °C.
Mol tömeg 86,09; mp -43,53 °C; bp 204°C; d 1,12 g/ml
CAS-szám: [96-48-0]
Vízzel elegyedik, oldódik metanolban, etanolban, etanolban, acetonban, éterben, benzolban
LD50: 1720 mg/kg (szájon át, egér) 1540 mg/kg (szájon át, patkány)
Felhasználás: Oldószer, festékeltávolító, kondenzátor elektrolit, a szerves kémiában
Szinonimák: GBL, BLO, butilakton, gamma-hidroxi-vajsavlakton, 1,2-butanolid, 1,4-butanolid, 4-butanolid, 2-oxanolon, tetrahidro-2-furanon, dihidro-2(3H)-furanon.
Nátrium-GHB.
Mol wt 126,09; mp 145-146 °C
CAS-szám: [502-85-2]
LD50:2700 mg/kg (szájon át, patkány)
Szinonimák: Gamma-OH, nátriumoxibát, nátrium-gamma-oxibutirát, Somatomax PM, Wy-3478, NSC-84223, Somsanit, Anetamin.
Kálium GHB.
Mol wt: 142,20
Kalcium GHB.
Mol tömeg 246,16; mp 164-166 °C, 166-168 °C.
Magnézium GHB.
Mol tömeg 230,39; mp (vízmentes) 172-174 °C; tetrahidrát 118-120 °C; pentahidrát 76-78 °C.
Laboratóriumi eljárások a GHB-sók szintéziséhez.
Kérjük, kövesse az általános laboratóriumi biztonsági eljárásokat. Viseljen laboratóriumi köpenyt és védőszemüveget. Forró maró oldatokkal és oldószerekkel fog dolgozni! Legyen tisztában a GHB előállításával kapcsolatos kockázatokkal! Soha ne dolgozzon egyedül!
Nátrium-GHB.
Eljárás:
Oldjunk fel 130 gramm (3,25 mól) tiszta nátrium-hidroxidot 400 ml desztillált vízben egy 1000 ml-es háromnyakú, kerek aljú lombikban, kevergetés közben. Az oldódás exoterm, és az oldat felmelegszik. A hőmérséklet szabályozására hidegvizes fürdő használható. Amikor minden tiszta oldattá oldódott, lassan, 50 ml-es adagokban, jó keverés mellett adjunk hozzá 250 ml gamma-butilaktont (280 g, 3,25 mol). Cseppentölcsér használata ajánlott. A gamma-butilakton hozzáadása a nátrium-hidroxid-oldathoz szintén exoterm, és ha túl gyorsan adjuk hozzá, az oldat forrni kezd, és ezt nem szeretnénk. A hőmérsékletet merülő hőmérővel kövessük nyomon. A gamma-butilakton hozzáadása 20-30 percig fog tartani. Amikor mindent hozzáadtunk, hagyjuk az elegyet további 10 percig reagálni, időnkénti keverés mellett.
Most itt az ideje, hogy a pH-érték univerzális pH-papírral történő ellenőrzésével lássuk, hogy a reakció befejeződött-e. A pH-értéket a pH-papírral ellenőrizzük. Célunk a 7-8-as pH érték elérése. Ha túl magas (pH > 8), akkor adjunk hozzá 10 ml gamma-butilaktont, és hagyjuk még néhány percig reagálni. Ha a pH túl alacsony (pH < 7), adjunk hozzá néhány ml tömény NaOH vizes oldatot. Folytassuk így, amíg a pH a kívánt határértékeken belül nem lesz.
Az oldat tökéletesen tiszta és enyhén sós ízű. Enyhén sárga színű lehet, de nem nagyon, ha elég tiszta butilaktont használtunk (a lakton felhasználás előtti desztillációja megoldja ezt a problémát, b.p. 204 °C). Ha a túl lúgos oldat semlegesítésére savat használunk (ahelyett, hogy több laktont adnánk hozzá), a sav nátriumsójának kristályai kicsapódhatnak az oldatban, és az íz erősen romlik. A végső oldat körülbelül 750 ml, 50% NaGHB lesz. Az oldatot lehet koncentrálni (a felesleges víz leforralásával) ~600 ml-re anélkül, hogy szobahőmérsékleten kikristályosodna, de ha csak ~500 ml-re koncentráljuk, akkor óhatatlanul megszilárdul.
Most itt az ideje, hogy a pH-érték univerzális pH-papírral történő ellenőrzésével lássuk, hogy a reakció befejeződött-e. A pH-értéket a pH-papírral ellenőrizzük. Célunk a 7-8-as pH érték elérése. Ha túl magas (pH > 8), akkor adjunk hozzá 10 ml gamma-butilaktont, és hagyjuk még néhány percig reagálni. Ha a pH túl alacsony (pH < 7), adjunk hozzá néhány ml tömény NaOH vizes oldatot. Folytassuk így, amíg a pH a kívánt határértékeken belül nem lesz.
Az oldat tökéletesen tiszta és enyhén sós ízű. Enyhén sárga színű lehet, de nem nagyon, ha elég tiszta butilaktont használtunk (a lakton felhasználás előtti desztillációja megoldja ezt a problémát, b.p. 204 °C). Ha a túl lúgos oldat semlegesítésére savat használunk (ahelyett, hogy több laktont adnánk hozzá), a sav nátriumsójának kristályai kicsapódhatnak az oldatban, és az íz erősen romlik. A végső oldat körülbelül 750 ml, 50% NaGHB lesz. Az oldatot lehet koncentrálni (a felesleges víz leforralásával) ~600 ml-re anélkül, hogy szobahőmérsékleten kikristályosodna, de ha csak ~500 ml-re koncentráljuk, akkor óhatatlanul megszilárdul.
Nátrium-GHB előállítása nátrium-hidrogénkarbonát (szódabikarbóna, NaHCO3) felhasználásával.
Adjunk 273 g NaHCO3-t (3,25 mól) 1125 ml desztillált vízhez egy háromnyakú, kerek aljú lombikban. Lassan forraljuk fel az oldatot, miközben üvegpálcával vagy hasonlóval keverjük. Az összes szódabikarbóna fel fog oldódni. Az oldatból forrás közben szén-dioxid távozik. Eza nátrium-hidrogénkarbonát, amely egy kissé erős bázissá, nátrium-karbonáttá bomlik le.
Csökkentsük a hőfokot enyhe forralásra, és lassan adjunk hozzá 250 ml gamma-butilaktont (280 g, 3,25 mól). Az adalékolás nem azonnal exoterm, mint a nátrium-hidroxid szintézisnél. Tartsuk ezt az oldatot 30 percig enyhén forralva. Ellenőrizzük a pH-értéket univerzális pH-papírral. Célunk a 7 körüli pH-érték, de 6-8 közötti érték is teljesen biztonságos. Ha a pH túl magas, adjunk még egy kis GBL-t, és folytassuk a refluxot.
Az oldat tökéletesen tiszta lesz, és teljesen színtelennek kell lennie. Ha nem teljesen színtelen, azaz ha kissé tisztátalan butilaktont használtunk, és az oldat világossárga színt vett fel, adjunk hozzá kb. 100 ml aktív szenet. Hagyjuk ezt 10 percig forralni. Hűtsük le az oldatot, majd szűrjük le, az aktív szenet két-háromszor mossuk át 50 ml hideg vízzel. Ebben a szintézisben 410 g NaGHB készül. Ez az oldat körülbelül 50%-os NaGHB koncentrációra koncentrálható, mielőtt elkezdene kristályosodni. Ha porrá kívánjuk alakítani, melegítsük addig, amíg az oldat hőmérséklete eléri a 150 °C-ot, majd öntsük egy lehűtött Pyrex-edénybe, és hagyjuk kihűlni és megszilárdulni. Ez a szintézis tökéletesen használható ott, ahol nem áll rendelkezésre ACS, élelmiszer- vagy elektronikai minőségű nátrium-hidroxid.
Az oldat tökéletesen tiszta lesz, és teljesen színtelennek kell lennie. Ha nem teljesen színtelen, azaz ha kissé tisztátalan butilaktont használtunk, és az oldat világossárga színt vett fel, adjunk hozzá kb. 100 ml aktív szenet. Hagyjuk ezt 10 percig forralni. Hűtsük le az oldatot, majd szűrjük le, az aktív szenet két-háromszor mossuk át 50 ml hideg vízzel. Ebben a szintézisben 410 g NaGHB készül. Ez az oldat körülbelül 50%-os NaGHB koncentrációra koncentrálható, mielőtt elkezdene kristályosodni. Ha porrá kívánjuk alakítani, melegítsük addig, amíg az oldat hőmérséklete eléri a 150 °C-ot, majd öntsük egy lehűtött Pyrex-edénybe, és hagyjuk kihűlni és megszilárdulni. Ez a szintézis tökéletesen használható ott, ahol nem áll rendelkezésre ACS, élelmiszer- vagy elektronikai minőségű nátrium-hidroxid.
Kálium GHB.
Használja a fent leírt etanolszintézist a nátrium-GHB esetében, de a 130 gramm NaOH-t 182 gramm KOH-ra cserélje (Ez a számítás a nehezebb K atomon és a KOH magasabb víztartalmán alapul a NaOH-hoz képest). A KOH használata a K-GHB felhasználóinak biztosítja azt a kálium-kiegészítést, amelyre egyesek szerint a GHB beadásával kapcsolatban szükség van. Ne feledjük, hogy a (porított) K-GHB valamivel kevésbé aktív (tömeg szerint), mint a Na-GHB, mivel a K-ion nehezebb, mint a Na-ion megfelelője. AK-GHB és a Na-GHB közötti különbség az, hogy a K só jobban oldódik vízben, mint a Na só, és az íze inkább só/licorice ízű, a Na-GHB só/szappan íze helyett.
Kalcium-GHB.
74 g analitikusan tiszta kalcium-hidroxidot szuszpendálunk 200 ml desztillált vízben. 160 ml 4-butilaktont adagokban (minden adag kb. 5-10 ml) és kevergetés mellett adunk ehhez a szuszpenzióhoz szobahőmérsékleten. 20 ml hozzáadása után a reakcióelegyet körülbelül 50 °C és 60 °C közötti hőmérsékletre melegítjük. A 4-butilakton hozzáadását úgy szabályozzuk, hogy a hőmérséklet körülbelül 50 °C és 60 °C között maradjon, ami körülbelül 1 órát vesz igénybe. Ez idő alatt a kalcium-hidroxid gyakorlatilag teljesen feloldódott. A reakcióanyagot enyhe rozsdasárga csapadékkal szennyezik. Hígítjuk 300 ml metil-alkohollal, négy órán át hagyjuk állni, majd egy összehajtogatott szűrőn átszűrjük. A tiszta szűrletet óvatosan 200 ml acetonnal kezeljük úgy, hogy minden egyes csapadékot okozó acetonadag után időt hagyunk a csapadék újrafeloldódására. Víztiszta oldatot kapunk, amelyet kristályosításra teszünk. Két óra állás után színtelen kristályok kezdenek lerakódni. Ebben az állapotban a kristályosodást aceton folyamatos adagolásával (összesen 100 ml) gyorsítjuk. A kristályosodási idő 24 óra. A kristályokat leszívjuk, és először 50 ml metanollal, majd 60 ml acetonnal mossuk. A kristályokat kb. 60 °C és 80 °C közötti hőmérsékleten szárítószekrényben szárítjuk. Terméshozam: 230 g. Olvadáspont 166-168 °C. (azonnal). A termék a 4-hidroxi-vajsav vízmentes, nem higroszkópos kalciumsója. Tetszés szerint vízben oldható, a vizes oldat pH-értéke 7-7,5 között van. A só tetszőleges ideig tárolható, levegőn nem változik. Még tároláskor sem vonzza a levegőből a vizet.
A maradék kristályosodik színtelen kristályok tömegévé, amelyet körülbelül 60 °C és 80 °C közötti hőmérsékleten történő szárítás után szárítanak. Terméshozam: kb. 105 g. Olvadáspont 164-166 °C. A termék di-(4-hidroxi-vajsav)-kalcium. Átkristályosítása úgy történik, hogy kevés metanolban feloldjuk, majd a zavarosságig acetont adunk hozzá, és hidegben kristályosítjuk.
A metanol helyett etanol és izopropanol is használható az átkristályosításhoz, ugyanilyen sikerrel. Víztartalmú alkoholok alkalmazása nélkül átkristályosítási közegként vagy az átkristályosítás és a tisztítás adalékaként nem kapunk stabil és különösen nem higroszkópmentes kalciumsókat. Az alkoholok víztartalmának körülbelül 3-10 térfogatszázaléknak kell lennie. Az így kapott végtermék könnyen oldódik vízben, nem hidroszkópos és kellemes aromás szagú.
A maradék kristályosodik színtelen kristályok tömegévé, amelyet körülbelül 60 °C és 80 °C közötti hőmérsékleten történő szárítás után szárítanak. Terméshozam: kb. 105 g. Olvadáspont 164-166 °C. A termék di-(4-hidroxi-vajsav)-kalcium. Átkristályosítása úgy történik, hogy kevés metanolban feloldjuk, majd a zavarosságig acetont adunk hozzá, és hidegben kristályosítjuk.
A metanol helyett etanol és izopropanol is használható az átkristályosításhoz, ugyanilyen sikerrel. Víztartalmú alkoholok alkalmazása nélkül átkristályosítási közegként vagy az átkristályosítás és a tisztítás adalékaként nem kapunk stabil és különösen nem higroszkópmentes kalciumsókat. Az alkoholok víztartalmának körülbelül 3-10 térfogatszázaléknak kell lennie. Az így kapott végtermék könnyen oldódik vízben, nem hidroszkópos és kellemes aromás szagú.
Magnézium GHB .
60 g magnézium-hidroxidot (analitikai minőségű) 200 ml csapvízben kevergetés mellett szuszpendáljuk. Egy sugárban és keverés mellett 160 ml butilaktont keverünk ehhez a szuszpenzióhoz. Ezután az elegyet vízfürdőn 6 órán át kevergetés mellett 2 literes lombikban melegítjük. A magnézium-hidroxid gyakorlatilag teljesen feloldódik. A lombikot egy éjszakán át állni hagyjuk, miközben a szennyeződések lerakódnak, és az oldatot erőlködés nélkül lefejtjük a szennyeződések lerakódásáról. A víztiszta dekantátumot kezdetben 100 ml acetonnal 10 percig keverjük. Az immár viszkózusabbá vált színtelen szirupos folyadékot a fentiek szerint ismét 100 ml acetonnal keverjük össze, az acetont ismét dekantálással eltávolítjuk, és a meglehetősen viszkózus, színtelen szirupot szobahőmérsékleten kb. 2-4 órán át hagyjuk magától elfolyni. Színtelen kristályos masszává szilárdul, amelyet mozsárban aprítunk és néhány órán át levegőn szárítunk. Olvadáspontja 76 °C és 78 °C között van. Terméshozam: 314 g analitikusan tiszta formában.
Ez a magnéziumsó körülbelül 5 mól hidratációs vizet tartalmaz. Nem hidroszkópos, stabil és tetszőlegesen hosszú ideig tárolható. Több órás szárítással 40 °C és 50 °C között elveszíti kristályvizének egy részét (1 mól), majd 118 °C és 120 °C között megolvad. Vízmentes magnézium-4-hidroxibutirátot lehet előállítani a víz eltávolításával szublimációval és/vagy a víz elpárologtatásával a víz csökkent parciális nyomása mellett és megemelt hőmérsékleten, vagy szerves oldószert tartalmazó oldatból történő kristályosítással. A vízmentes só 172-174 °C-on olvad. A kémiai elemzés 10,50 tömegszázalék magnéziumot mutat (számított 10,55 tömegszázalék magnézium). Minden módosítás nem higroszkópos és tárolás közben stabil. 1 g magnéziumsó szobahőmérsékleten 2 ml vízben oldódik, a vizes oldat pH-ja 7. Vízben, metanolban és etanolban könnyen oldódik, éterben és szénhidrogénekben nem oldódik, nem higroszkópos, tárolható és kellemes aromás szaga van.
Ez a magnéziumsó körülbelül 5 mól hidratációs vizet tartalmaz. Nem hidroszkópos, stabil és tetszőlegesen hosszú ideig tárolható. Több órás szárítással 40 °C és 50 °C között elveszíti kristályvizének egy részét (1 mól), majd 118 °C és 120 °C között megolvad. Vízmentes magnézium-4-hidroxibutirátot lehet előállítani a víz eltávolításával szublimációval és/vagy a víz elpárologtatásával a víz csökkent parciális nyomása mellett és megemelt hőmérsékleten, vagy szerves oldószert tartalmazó oldatból történő kristályosítással. A vízmentes só 172-174 °C-on olvad. A kémiai elemzés 10,50 tömegszázalék magnéziumot mutat (számított 10,55 tömegszázalék magnézium). Minden módosítás nem higroszkópos és tárolás közben stabil. 1 g magnéziumsó szobahőmérsékleten 2 ml vízben oldódik, a vizes oldat pH-ja 7. Vízben, metanolban és etanolban könnyen oldódik, éterben és szénhidrogénekben nem oldódik, nem higroszkópos, tárolható és kellemes aromás szaga van.
Egyéb sók.
A GHB lítium- és ammóniumsói veszélyesek lennének lenyeléskor. A lítiumion mérgező, és az NH3-laktonnal együtt pirrolidonná válik.
Szintézis Kérdések és válaszok.
K: Használhatok lúgot a tiszta nátrium-hidroxid helyett?
V: Nem, annak kiszámíthatatlan egészségügyi következményei lehetnek. A barkácsáruházi lúgnak közel sincsenek olyan szigorú tisztasági kritériumai, mint például az élelmiszeripari, ACS minőségű vagy elektronikai minőségű lúgnak. Néhányan sikeres történetekről számolnak be a lúg használatával, ami valóban lehetséges, de mint mondtam, az eredmények kiszámíthatatlanok.
K: Nekem nincsenek üvegedényeim, amikre ön szerint szükség van, felforralhatom-e helyette az oldatot egy edényben a tűzhelyen?
V: Nem, nem lehet. A nátrium-hidroxid korrodálja a fémet, és válogatott fémionok kerülnek a termékedbe. Természetesen használhat a javaslataimnál egyszerűbb üvegedényeket, és elvégezheti az eljárás szükséges módosításait.
K: Nem tudom átkristályosítani a Na-GHB-t etanolból. Ragadós masszát képez.
V: A Na-GHB nem száraz, vagy az etanol nem vízmentes. A víz szinte lehetetlenné teszi az átkristályosítást. Attól, hogy a nátrium-GHB deliquens (higroszkópos), ez nem lesz jobb. A GHB-t alaposan meg kell szárítani, lehetőleg vákuumos exszikkátorban, mielőtt megkísérelné az átkristályosítást, vagy bármilyen más rögtönzött alternatívát. A használni kívánt etanolt (leggyakrabban 95%-os tisztaságban szállítják, a maradék víz) vízmentes kalcium-szulfáton történő szárítással kell szárítani, majd kalcium-oxidból történő desztillációval, megfelelő intézkedésekkel kizárva a nedvességet a reakcióból.
K: Hol lehet butilaktont vásárolni/biztonságos-e butilaktont vásárolni?
V: Fogalmam sincs, hogy az Ön országában milyen a helyzet. Az ezekre a kérdésekre adott válaszok nagyban függnek attól, hogy ki vagy és hol élsz. Azonbankapcsolatba léphet a GHB-készletek számos eladójának bármelyikével, amelyek online megtalálhatók.
V: Nem, annak kiszámíthatatlan egészségügyi következményei lehetnek. A barkácsáruházi lúgnak közel sincsenek olyan szigorú tisztasági kritériumai, mint például az élelmiszeripari, ACS minőségű vagy elektronikai minőségű lúgnak. Néhányan sikeres történetekről számolnak be a lúg használatával, ami valóban lehetséges, de mint mondtam, az eredmények kiszámíthatatlanok.
K: Nekem nincsenek üvegedényeim, amikre ön szerint szükség van, felforralhatom-e helyette az oldatot egy edényben a tűzhelyen?
V: Nem, nem lehet. A nátrium-hidroxid korrodálja a fémet, és válogatott fémionok kerülnek a termékedbe. Természetesen használhat a javaslataimnál egyszerűbb üvegedényeket, és elvégezheti az eljárás szükséges módosításait.
K: Nem tudom átkristályosítani a Na-GHB-t etanolból. Ragadós masszát képez.
V: A Na-GHB nem száraz, vagy az etanol nem vízmentes. A víz szinte lehetetlenné teszi az átkristályosítást. Attól, hogy a nátrium-GHB deliquens (higroszkópos), ez nem lesz jobb. A GHB-t alaposan meg kell szárítani, lehetőleg vákuumos exszikkátorban, mielőtt megkísérelné az átkristályosítást, vagy bármilyen más rögtönzött alternatívát. A használni kívánt etanolt (leggyakrabban 95%-os tisztaságban szállítják, a maradék víz) vízmentes kalcium-szulfáton történő szárítással kell szárítani, majd kalcium-oxidból történő desztillációval, megfelelő intézkedésekkel kizárva a nedvességet a reakcióból.
K: Hol lehet butilaktont vásárolni/biztonságos-e butilaktont vásárolni?
V: Fogalmam sincs, hogy az Ön országában milyen a helyzet. Az ezekre a kérdésekre adott válaszok nagyban függnek attól, hogy ki vagy és hol élsz. Azonbankapcsolatba léphet a GHB-készletek számos eladójának bármelyikével, amelyek online megtalálhatók.
Prekurzorok.
A GHB szintézisének nyilvánvaló prekurzora a gamma-butilakton. Ez olyan prekurzorokból állítható elő, mint a tetrahidrofurán (THF) oxidálószerekkel, mint a ruténiumtetroxid, kalcium-hipoklorit és salétromsav. Használhatók 4-halo-vajsav-származékok (klór, bróm, jód) is. Az alábbi szintézishez hasonlóan nátrium-metoxiddal történő desztillációval gamma-butilaktonná alakíthatók.
gamma-butilakton 4-brom-vajsavból.
7,8 g nátrium 500 ml abszolút alkoholban lévő oldatához 60,5 g 4-brom-vajsavat adtunk. A reakcióelegyet reflux kondenzátor alatt kb. öt órán át forraljuk. Ez idő alatt a nátrium-bromid elvált. Az alkoholt gőzfürdőből desztilláltuk, és a laktont a nátrium-bromidtól éterrel történő extrakcióval választottuk el. Az étert bepároltuk, és a laktont közönséges nyomáson desztilláltuk. A hozam 21,2 gramm (67%) 202-206 °C-on forrásban lévő termék volt. Alternatív megoldás lehet a vajsav szabad gyökös klórozása kén-kloriddal peroxidok jelenlétében, és az izomereket desztillációval elválasztani, a 4-klór-vajsav nátriumsóját előállítani, és a laktonhoz ciklizálni, mint a fenti 4-brom-származék esetében. A gamma-butilakton szintén előállítható 4-metoxi-vajsavból, 3-fenoxipropilcianidból, gamma-dietil-aminovajsavból és béta-klór-etil-viniléterből, valamint sok más, kicsit túl egzotikus vegyszerből. Ipari felhasználásakor általában acetilén és formaldehid magas hőmérsékleten és nyomáson történő reakciójával állítják elő.
Az1,4-butándiol (BDO) dehidrogénezése gamma-butilaktonná (GBL).
90,1 g (1 mól) 1,4-butándiol, 4 g rézkromit katalizátor és 0,15 g porított, reagens minőségű nátrium-hidroxid (vagy jobb KOH) keverékét erőteljesen kevertetjük és reflux alatt melegítjük. Kb. 200 °C-on élénk hidrogénfejlődés következett be, majd a hőmérséklet kb. 10 °C-kal csökkent, és a dehidrogénezés zavartalanul folyt. A gázfejlődés (39 L/2 mol/mol reagált 1,4-butándiol) körülbelül 3 óra alatt megszűnt. A reakcióelegyet szobahőmérsékletre hűtöttük, a katalizátortól leszűrtük és csökkentett nyomáson desztilláltuk, így körülbelül 80%-os hozammal gamma-butilaktont és körülbelül 10%-os hozammal nem reagált 1,4-butándiolt kaptunk.
Nagy aktivitású rézkromit dehidrogénező katalizátor előállítása.
260 g réz(II)nitrát-trihidrát 900 ml csapvízben 80 °C-on lévő oldatát kevergetés közben 178 g nátriumdikromát-dihidrát és 225 ml 28%-os NH4OH 900 ml-re kiegészített oldatához adtuk 25 °C-on. A csapadékot szívószűréssel összegyűjtöttük, és háromszor vízben felitattuk. A rézammónium-kromátot 75-80 °C-on egy éjszakán át szárítottuk. Ezt porítottuk, és kis adagokban egy egyliteres, 3 nyakú lombikba adtuk, amely rozsdamentes acél Hershberg típusú keverővel volt felszerelve, amely a lombik aljához közel kapart. A lombikot részben 350 °C-os olajfürdőbe merítettük (300-320 °C-on jó eredményeket lehet elérni). Az adalékolás ideje 15 perc volt (sok gőz keletkezett), és az elegyet 350 °C-on további 15 percig kevertettük, miután minden elkészült. A lehűtött, és fekete porszerű port úgy használtuk fel, ahogy van a dehidrogénezéshez.
260 g réz(II)nitrát-trihidrát 900 ml csapvízben 80 °C-on lévő oldatát kevergetés közben 178 g nátriumdikromát-dihidrát és 225 ml 28%-os NH4OH 900 ml-re kiegészített oldatához adtuk 25 °C-on. A csapadékot szívószűréssel összegyűjtöttük, és háromszor vízben felitattuk. A rézammónium-kromátot 75-80 °C-on egy éjszakán át szárítottuk. Ezt porítottuk, és kis adagokban egy egyliteres, 3 nyakú lombikba adtuk, amely rozsdamentes acél Hershberg típusú keverővel volt felszerelve, amely a lombik aljához közel kapart. A lombikot részben 350 °C-os olajfürdőbe merítettük (300-320 °C-on jó eredményeket lehet elérni). Az adalékolás ideje 15 perc volt (sok gőz keletkezett), és az elegyet 350 °C-on további 15 percig kevertettük, miután minden elkészült. A lehűtött, és fekete porszerű port úgy használtuk fel, ahogy van a dehidrogénezéshez.
gamma-butilakton szintézis tetrahidrofuránból (THF).
7,2 g (0,1 mol) tetrahidrofurán 100 ml vízben kevert keverékéhez 15,1 g nátrium-bromátot és 13,6 g (0,1 mol) kálium-hidrogén-szulfátot adtunk. Külső hűtésre volt szükség, hogy az oldat hőmérsékletét 25-30 °C között tartsuk. A keverést 16 órán át folytattuk szobahőmérsékleten, mire az összes THF elfogyott. A keletkezett felesleges bróm elfojtására savas nátrium-szulfit-oldatot használtunk [a biszulfit ugyanilyen jól működik]. Így 140-150 ml 10%-os oldatot adtunk hozzá és 13,6 g (0,1 mol) kálium-hidrogén-szulfátot. A reakciót lehűtöttük és 5x30 ml diklórmetánnal extraháltuk. Az egyesített szerves rétegeket MgSO4 felett szárítottuk, és az oldószert vákuumban eltávolítottuk. A maradékot desztilláltuk, így 73%-os termeléssel gamma-butilaktont kaptunk (bp 204-205 °C).
GABA Sandmeyer-reakciója GBL/GHB-vé.
Fantasztikus egy olyan vegyész számára, aki kis mennyiségben és nagy hozammal szeretne GHB-t előállítani, méghozzá úgy, hogy nem kell közvetlenül szabályozott vegyi anyagokat, például gamma-butilaktont (GBL) vagy 1,4-butándiolt (BDO) beszereznie. Ezzel elkerülhető a tetrahidrofurán (THF) oxidációjánál jellemzően tapasztalt alacsony hozam is. Egy könnyen beszerezhető aminosavat, a gamma-aminovajsavat (GABA) és nátrium-nitritet (NaNO2) használ. Nagyon szépen skálázódik és túl sok gond nélkül fut. Egyetlen gyanús vegyi anyagot sem használ.
A Sandmeyer-reakció salétromsavat használ az aminok diazónium-sókká alakításához. Ezt a reakciót, ahogyan a GABA GHB-vá alakítására vonatkozik, az alábbi első reakció mutatja be. Az alifás diazónium-sók víz jelenlétében gyorsan hidrolízisnek mennek át, nitrogéngázt bocsátva ki, és hidroxilcsoportot hagyva maguk után. Ezt mutatja a második lépés. E reakciók eredményeképpen a GABA könnyen elvégezhető egytégelyes reakcióban GHB-vé alakítható.
A reakció lefuttatása.
Állítsunk fel egy 2 literes lombikot, amely jeges vízben áll egy mágneses keverő tetején. Most.
A reakció lefuttatása.
Állítsunk fel egy 2 literes lombikot, amely jeges vízben áll egy mágneses keverő tetején. Most.
- Adjunk hozzá 3 mol GABA-t (309,4 g).
- Adjunk hozzá 3mol NaNO2-t (207,0 g).
- Adjunk hozzá 700 ml vizet (a teljes térfogat kb. 1100 ml lesz).
- Dobjunk bele egy 1"-os keverőpálcát, és kezdjük el keverni.
- Töltsünk egy 500 ml-es nyomáskiegyenlített adaléktölcsért 3,3 mol HCl(aq) (385,0 g 31,25%, 334,8 ml 31,25%).
- Szerelje fel az addíciós tölcsért egy gázelvezető adapterrel, és szellőztesse ki a külső térbe.
Kezdjük el lassan csepegtetni a sósavat a keverékbe. Csepegtessük állandó ütemben, kb. 2-5 másodpercenként 1 cseppet. Az idő előrehaladtával gyorsítsa fel, és szükség szerint cserélje ki a jeget, de ne engedje, hogy a barna mérges gáz fejlődése erőteljes legyen. Az utolsó csepp sav hozzáadása után körülbelül egy órával már nem kell a jeget cserélni. Ha a reakció befejeződött, folytassa a kivonást. (Általában 24-36 órával később)
Extrakció.
Erre számos lehetőség van. Ez még mindig folyamatban lévő munka, de körülbelül 20 futtatás után eljutottam oda, hogy ezt a munkát fel kell használni. Az oldószeres extrakciók elvégzéséhez etil-acetátot (EtOAc), kloroformot vagy metilén-kloridot (diklórmetán, más néven DCM) használhat. Én általában DCM-et használtam, mivel az kellemes, mivel a szerves réteg az elválasztó tölcsér aljára esik.
1. Egyszerű desztilláció beállítása
Extrakció.
Erre számos lehetőség van. Ez még mindig folyamatban lévő munka, de körülbelül 20 futtatás után eljutottam oda, hogy ezt a munkát fel kell használni. Az oldószeres extrakciók elvégzéséhez etil-acetátot (EtOAc), kloroformot vagy metilén-kloridot (diklórmetán, más néven DCM) használhat. Én általában DCM-et használtam, mivel az kellemes, mivel a szerves réteg az elválasztó tölcsér aljára esik.
1. Egyszerű desztilláció beállítása
a) Desztilláljunk, az első 5-10 ml, vagy úgy 5-10 ml desztillátumot kidobva, mivel az meglehetősen sok nitrogén-oxidot tartalmaz. Desztilláljunk le annyi vizet, amennyit csak lehet, alapvetően addig, amíg a nátrium-klorid el nem kezdi telíteni a vizes réteget és ki nem csapódik.
b) A maradék desztillátum (kb. 700 ml) kb. 1 g GBL/10 ml-t fog tartalmazni.
c) Kezeljük a maradék desztillátumot NaHCO3-mal 30 percig refluxon.
d) Forraljuk körülbelül 5 % térfogatú aktív szénnel (azaz .35 ml aktív szénnel) (az oldat térfogatához képest) 5-10 percig.
e) Hagyjuk kihűlni és szűrjük le, mossuk ki a szenet desztillált vízzel. Tegyük félre a NaGHB-t.
2. A maradék vizes oldattal 5 alkalommal extraháljunk 625 ml DCM adaggal.
3. Desztilláljuk le a DCM-et (használjuk újra a DCM-et!).
4 . Desztilláljuk a GBL-t (vákuumban, ha van).
5 . Reagáljunk NaHCO3-mal és desztillált vízzel, és kezeljük aktív szénnel, mint korábban.
Az oldószerrel extrahált GBL-ből általában 375 g NaGHB készül, ebből 100 g NaGHB a vizes desztillátumból. Bár a konverzió majdnem mennyiségi (GC/MS-sel mérve), a visszanyert teljes hozam általában 70% körüli.
3. Desztilláljuk le a DCM-et (használjuk újra a DCM-et!).
4 . Desztilláljuk a GBL-t (vákuumban, ha van).
5 . Reagáljunk NaHCO3-mal és desztillált vízzel, és kezeljük aktív szénnel, mint korábban.
Az oldószerrel extrahált GBL-ből általában 375 g NaGHB készül, ebből 100 g NaGHB a vizes desztillátumból. Bár a konverzió majdnem mennyiségi (GC/MS-sel mérve), a visszanyert teljes hozam általában 70% körüli.
Last edited:
